
2.已知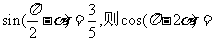 ( )
( )
A.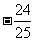 B.
B.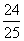 C.
C.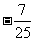 D.
D.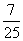
1.设函数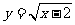 的定义域为集合M,集合
的定义域为集合M,集合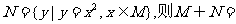 ( )
( )
A.M B.N C. D.
D.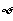
(三)条件:有难溶物质(沉淀)或挥发性物质(气体)或弱电解质(如水)生成,以及离子或分子得失电子。
[思考感悟]
电解质一定能导电吗?某物质的水溶液能导电,该物质一定是电解质吗?
电解质只有电离后才能导电。固体电解质不能导电。有的物质本身不是电解质,但溶于水生成电解质溶液而导电,如NH3变为NH3·H2O,CO2变为H2CO3等,所以水溶液能导电的物质不一定是电解质。
[基础训练]
1、下列说法正确的是( C )
A、HR溶液导电性较弱,HR属于弱酸
B、某化合物溶解于水导电,则该化合物为电解质
C、根据电解质在其水溶液中能否完全电离,将电解质分成强电解质与弱电解质
D、食盐是电解质,食盐的水溶液也是电解质
2、下列关于纯净物、混合物、强电解质、弱电解质和非电解质的正确组合是( B )
|
|
纯净物 |
混合物 |
强电解质 |
弱电解质 |
非电解质 |
|
A |
盐酸 |
水煤气 |
硫酸 |
醋酸 |
干冰 |
|
B |
氢氧化钡 |
蔗糖溶液 |
硫酸钡 |
醋酸 |
三氧化硫 |
|
C |
胆矾 |
石灰水 |
苛性钾 |
水 |
碳酸钙 |
|
D |
重钙 |
普钙 |
氯化钠 |
氢氧化铁 |
氢气 |
3、下列说法正确的一组是( C )
①不溶于水的盐(CaCO3、BaSO4等)都是弱电解质
②可溶于水的盐都是强电解质
③0.5mol·L-1所有一元酸中氢离子浓度都是0.5mol·L-1
④强酸溶液中氢离子浓度一定大于弱酸溶液中氢离子浓度
⑤电解质溶液导电的原因是溶液中有自由移动的阴阳离子
⑥液态的电解质都能导电
A、①③⑤⑥ B、②④⑤⑥ C、只有⑤ D、只有⑥
[高考模拟]
4、(2007广东理基)某溶液中可能含有SO42-、CO32-、Cl-。为了检验其中是否含有SO42-,除BaCl2溶液外,还需要的溶液是( B )
A、H2SO4 B、HCl C、NaOH D、NaNO3
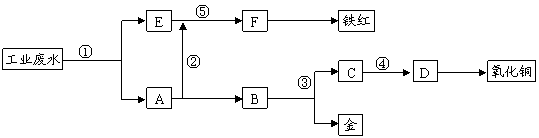
5、(2008宁夏理综26)某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。有人设计了图中的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。
 填写下列空白:
填写下列空白:
(1)图中标号处需加入的相应物质分别是①铁屑、②稀硫酸、③稀硝酸、④氢氧化钠、⑤氢氧化钠。
(2)写出①处发生反应的离子方程式Fe+2H+=Fe2++H2↑,2Fe3++Fe=3Fe2+,Cu2++Fe=Cu+Fe2+,2Au3++3Fe=2Au+3Fe2+;写出③处发生反应的化学方程式3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(3)铁红的化学式为Fe2O3;分别写出铁红和氧化铜在工业上的一种用途:铁红用作红色涂料;氧化铜用作制造铜盐的原料。
[作业]
(二)实质:离子的种类或数量发生变化。
(一)概念:化合物在水溶液或在熔化时,有离子参加或有离子生成的反应。
(二)导电能力的强弱:在恒定电压作用下,取决于电解质溶液中离子浓度和离子所带电荷数,离子浓度越高,导电能力越强,离子所带的电荷数越多,导电能力越强,与电解质的强弱无关。
(一)电解质溶液导电的原因:电解质在溶剂水作用下,电离出自由移动的离子,在外加电源的作用下,阴、阳离子定向移动。
(三)表示方法--电离方程式:
1、强电解质:用“=”连接,如H2SO4:H2SO4=2H++SO42-。
2、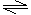 弱电解质(包括弱酸的酸式酸根):用“ ”连接,如:
弱电解质(包括弱酸的酸式酸根):用“ ”连接,如:
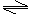 CH3COOH:CH3COOH CH3COO-+H+。
CH3COOH:CH3COOH CH3COO-+H+。
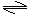
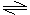 (1)多元弱酸分步电离,如H2CO3:H2CO3 HCO3-+H+,HCO3- CO32-+H+。
(1)多元弱酸分步电离,如H2CO3:H2CO3 HCO3-+H+,HCO3- CO32-+H+。
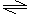 (2)多元弱碱一步写完,如Fe(OH)3:Fe(OH)3 Fe3++3OH-。
(2)多元弱碱一步写完,如Fe(OH)3:Fe(OH)3 Fe3++3OH-。
(二)电离的条件:溶解(离子化合物或共价化合物)或熔化(离子化合物)。
(一)概念:电解质在水溶液或熔融时,离解成能够自由移动的离子的过程。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com