
23.(10分)已知Co(H2O)62+显粉红色,CoCl42-显蓝色。CoCl2晶体在不同的盐酸溶液中会显示不同的颜色:①在很稀的盐酸中呈粉红色,②在浓盐酸中呈蓝色,③在一定浓度的盐酸中会呈紫色。
(1)某同学将一定量的氯化钴晶体溶于浓盐酸中,然后在该溶液中加入大量水,溶液的颜色如何变化? ▲ ,其原因为 ▲ 。(请用相关的离子方程式和适当的文字进行说明)。写出对应平衡的平衡常数表达式K= ▲ 。
 (2)某同学将盛有③获得的溶液的试管置于热水中,溶液变为蓝色,则说明该平衡的ΔH
(2)某同学将盛有③获得的溶液的试管置于热水中,溶液变为蓝色,则说明该平衡的ΔH
 ▲ 0(填“<”、“>”或“=”),此时,平衡常数K ▲ (填“变大”、“变小”或“不变”)。
▲ 0(填“<”、“>”或“=”),此时,平衡常数K ▲ (填“变大”、“变小”或“不变”)。
 (3)已知Fe(OH)3的Ksp=1.0×10-38,Co(OH)2的Ksp=1.6×10-15。若0.1mol·L-1的CoCl2溶液中含有Fe3+,调节pH使Fe3+沉淀完全[即c(Fe3+)<10-5 mol·L-1]时的pH=
(3)已知Fe(OH)3的Ksp=1.0×10-38,Co(OH)2的Ksp=1.6×10-15。若0.1mol·L-1的CoCl2溶液中含有Fe3+,调节pH使Fe3+沉淀完全[即c(Fe3+)<10-5 mol·L-1]时的pH=
 ▲ ,此时Co2+是否开始沉淀? ▲ (填“是”或“否”)。
▲ ,此时Co2+是否开始沉淀? ▲ (填“是”或“否”)。
22.(8分)镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用,其充、放电反应按下式进行:
Cd(OH)2+2Ni(OH)2 Cd+2NiO(OH)+2H2O。
Cd+2NiO(OH)+2H2O。
(1)该电池中的电解质溶液显 ▲ 性(填写“酸性”、“中性”或“碱性”)
(2)当该电池放电时,负极上发生的电极反应式是 ▲ 。
(3)放电过程中正极处溶液的pH ▲ (填“增大”、“减小”或“不变”)。
(4)若用该电池电解AlCl3和H2SO4的混合溶液,它们的物质的量之比为3:4,则下列说法错误的是 ▲ 。
A.阴极自始至终只有H2析出 B.阳极先析出Cl2后析出O2
C.电解最后阶段为电解水 D.溶液中先有白色沉淀生成后沉淀又全部溶解
21.(8分)科学家认为,氢气是一种高效而无污染的理想能源。为减少CO对大气的污染,某研究性学习小组拟研究CO和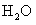 反应转化为绿色能源
反应转化为绿色能源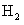 。
。
 已知:在101kPa下,2CO(g)+O2 (g)=2CO2(g) △H=-566kJ·mol-1
已知:在101kPa下,2CO(g)+O2 (g)=2CO2(g) △H=-566kJ·mol-1
 2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1
 H2O(g)=H2O(l) △H=-44kJ·mol-1
H2O(g)=H2O(l) △H=-44kJ·mol-1
 (1)CO的标准燃烧热△H= ▲ 。
(1)CO的标准燃烧热△H= ▲ 。
 (2)右图为1molH2与足量O2反应生成液态水和气态水的能量变化关系图,则图中的△H= ▲ 。在该反应中加入催化剂,反应速率加快,则E1 ▲ (填“变大”、“变小”或“不变”,本小题下同) ,E2 ▲ ,△H ▲ 。
(2)右图为1molH2与足量O2反应生成液态水和气态水的能量变化关系图,则图中的△H= ▲ 。在该反应中加入催化剂,反应速率加快,则E1 ▲ (填“变大”、“变小”或“不变”,本小题下同) ,E2 ▲ ,△H ▲ 。
(3)写出CO和H2O(g)作用生成CO2和H2的热化学方程式 ▲ 。
20.各取1mL两种酸加水稀释过程中的c(H+)变化情况如右下图所示,则有关说法正确的是
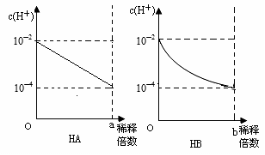
A.HA是弱酸,HB是强酸
B.稀释前,c(HA)=10-2mol·L-1,
c(HB)>10-2mol·L-1
C.a=b=100
D.取稀释后溶液,中和同体积同浓度的
NaOH溶液,消耗酸的体积V(HA) <V(HB)
19.中和滴定的误差要求小于0.1%,若用0.2000 mol·L-1盐酸滴定0.2000 mol·L-1氢氧化钠溶液,则中和滴定曲线中发生突变时的pH范围是(lg2=0.3)
A.4.3-9.7 B.3.7-10.3 C.4.0-10.0 D.无法确定
18.下列不能用勒夏特列原理解释的是
A.在温热气候条件下的浅海地区往往发现有厚层的石灰岩沉积,而在深海地区却很少见到
B.在夏天喝冰镇碳酸饮料,容易打嗝
C.用双氧水处理伤口时,伤口处易出现很多气泡
D.钾肥(草木灰)与铵态氮肥(肥田粉)不能混用
17.已知:①101kPa下,2C(石墨,s)+O2(g)=2CO(g) ΔH=-221kJ·mol-1
②C(石墨,s)=C(金刚石,s) ΔH=-1.91 kJ·mol-1
③在稀溶液中,H+(aq) +OH-(aq) =H2O(l) ΔH=-57.3kJ·mol-1,下列有关说法正确的是
A.金刚石比石墨稳定 B.石墨的热值比9.2kJ·g-1大
C.所有强酸与强碱反应生成1molH2O时放出的热量都为57.3kJ
D.1mol醋酸与1mol氢氧化钠在稀溶液中完全反应时,放出的热量大于57.3kJ
16. 下图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,
下图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,
 下列有关说法不正确的是
下列有关说法不正确的是
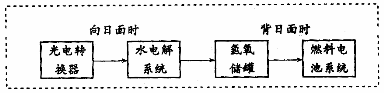



 A.该能量转化系统中的水可以循环利用
A.该能量转化系统中的水可以循环利用
 B.燃料电池系统产生的能量实际上来自于太阳能
B.燃料电池系统产生的能量实际上来自于太阳能
 C.水电解系统中是将电能转化为化学能的过程
C.水电解系统中是将电能转化为化学能的过程
D.背日面时,燃料电池系统负极发生的反应为:O2+4e-+2H2O=4OH-
15.已知反应C(s)+H2O(g)  CO(g)+H2(g) ΔH>0在一定温度下能自发进行,其原因为
CO(g)+H2(g) ΔH>0在一定温度下能自发进行,其原因为
A.是吸热反应 B.是熵减反应
C.能量效应大于熵变效应 D.熵变效应大于能量效应
14.亚硝酸钠俗称“工业盐”,其外观与食盐相似,有咸味。亚硝酸钠进入人体后,可将血液中的低铁血红蛋白氧化成高铁血红蛋白,失去输送氧气的功能,致使组织缺氧,出现青紫而中毒。美蓝是亚硝酸盐中毒的有效解毒剂。下列有关说法中不正确的是
A.在中毒过程中血红蛋白被还原
B.药品美蓝在解毒过程中作还原剂
C.中毒时亚硝酸钠发生还原反应
D.可用稀硝酸、AgNO3溶液区分亚硝酸钠与食盐
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com