
1.(07年山东理综·10)物质的量浓度相同时,下列既能跟NaOH溶液反应,又能跟盐酸反应的溶液中,pH最大的是
A.Na2CO3溶液 B.NH4HCO3溶液 C.NaHCO3溶液 D.NaHSO4溶液
答案:C
解析:A中碳酸钠能和盐酸反应,不与氢氧化钠反应,排除;B中碳酸氢铵二者都能反应;C中碳酸氢钠二者均能反应;D中硫酸氢钠能和氢氧化钠反应,不与盐酸反应,排除。故此题中实际是比较碳酸氢铵和碳酸氢钠溶液同浓度时pH值大小的比较,碳酸氢铵是弱碱弱酸盐,而碳酸氢钠是强碱弱酸盐,对比可知答案选C。
3、某化学课外小组用海带为原料制取了少量碘水。现用CCl4从碘水中萃取碘并用分液漏斗分离两种溶液。其实验操作可分解为如下几步:
A、把盛有溶液的分液漏斗放在铁架台的铁圈中;
B、把50mL碘水和15mLCCl4加入分液漏斗中,并盖好玻璃塞;
C、检验分液漏斗活塞和上口玻璃塞是否漏液;
D、倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E、放开活塞,用烧杯接收溶液;
F、从分液漏斗上口倒出上层水溶液;
G、将漏斗上口的玻璃塞打开使溶液上的凹槽或小孔对准漏斗口上的小孔;H、静置、分层。
就此实验,完成下列填空: (1)正确操作步骤的顺序是(用上述各操作的编号字母填空): _____→_____→_____→ A → G →_____→ E → F。 (2)上述E步骤的操作中应注意_____。上述G步骤操作的目的是_____。 (3)能选用CCl4从碘水中萃取碘的原因是_____。
课后作业:随堂练习

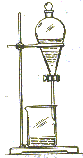
2、下列实验设计中,能达到预期目的的是( )
A、将氯化钠和硝酸钾的混合物用溶解、过滤的方法分离
B、将氢气和氧气的混合气体通过灼热的氧化铜除去氢气
C、用碳酸钠溶液区分氯化钠溶液、氯化钡溶液及硝酸钙溶液
D、将氯化钾和二氧化锰的混合物用溶解、过滤、蒸发的方法分离
1、下列物质的分离方法不正确的是( )
A、用过滤的方法除去食盐水中的泥沙
B、用蒸馏的方法将自来水制成蒸馏水
C、用酒精萃取碘水中的碘
D、用淘洗的方法从沙里淘金
4、从这个实验中,大家可以看出蒸馏适用于什么类型的混合物的分离?
[投](4)蒸馏的使用范围:
液态混合物中,沸点不同,除去难挥发或不挥发的物质。
[思考]蒸馏与蒸发的区别:
(加热是为了获得溶液的残留物时,要用蒸发;加热是为了收集蒸气的冷凝液体时,要用蒸馏)
[过渡]在日常生活中,有时我们的衣服粘了油渍,可以用汽油擦洗,这就是萃取的应用。接下来我们学习另外的一种分离方法,叫做萃取与分液。
[板书]2、萃取
[过]我们先来认识这个新的仪器:分液漏斗。
[展示仪器]分液漏斗的组成,分液漏斗的活塞、盖子同漏斗本身是配套的。使用漏斗前要检验漏斗是否漏水。方法为:关闭活塞,在漏斗中加少量水,盖好盖子,用右手压住分液漏斗口部,左手握住活塞部分,把分液漏斗倒转过来用力振荡,看是否漏水
[投](1)定义:利用某溶质在互不相溶的溶剂中的溶解度不同,用一种溶剂把溶质从它与另一种溶剂组成的溶液中提取出来,在利用分液的原理和方法将它们分离开来。
[讲解+实验演示]我们通过实验来解释萃取的定义,我们知道碘单质在水中的溶解度不大,碘水呈黄棕色。碘是溶质,水是溶剂。取10ml饱和碘水,倒入分液漏斗中。接着,按照萃取的定义,我们要用另一种溶剂加把溶质碘从碘水中提取出来,这另外一种溶剂的选择要符合一些条件,
[投](2)萃取剂的选择:
a.溶质在萃取剂的溶解度要比在原溶剂(水)大。
b.萃取剂与原溶剂(水)不互溶。
c.萃取剂与溶液不发生发应。
[讲解+实验演示]那么,我们根据这些条件可以选择了四氯化碳,由于碘在四氯化碳的溶解度比较大,所以我们加入4ml就可以了,进行振荡。请大家注意振荡的操作:用右手压住分液漏斗口部,左手握住活塞部分,把分液漏斗倒转过来用力振荡,注意放气怎么(强调放气的重要性)。振荡后将分液漏斗放在铁架台上静置。
[讲解]静置后,大家发现漏斗中的液体分为两层,下层为紫红色,这一层为碘的四氯化碳的溶液。上层溶液颜色变淡了,证明碘水中的碘已经被萃取到四氯化碳中了,达到了碘和水分离的目的,这就是萃取。
[引导]大家想想,萃取后,如何分离?比如汤上面的油层是怎样弄走的?
(勺子舀,吸管吸,。。。。。)
[讲]我们试想一下,可不可以想办法使汤使下面流走,让油刚好留在容器中。容器下面有通道,汤从下面流走,在汤刚好流完时,关闭通道,这样汤和油不就分开了吗,这正好符合分液漏斗的结构。
[板书]3、分液
[讲解+实验演示]最后一步,就是把四氯化碳层和水层分开,这就是分液。首先,打开盖子(塞子),为什么?(平衡大气压)将活塞打开,使下层液体慢慢流出。漏斗下端口靠烧杯壁。上层液体从上口倒出,为什么?(防止上层液体混带有下层液体)
[投影总结]
(1)定义:把两种互不相溶的液体(且密度不同)分开的操作
[板书]萃取与分液的步骤:
a.检验分液漏斗是否漏水
b.加入溶液,加入萃取剂,振荡
c.静置分层
d.分液
[小结]通过这个实验,大家要掌握的是萃取剂的选择(三个条件),以及掌握萃取与分液的操作步骤。(四个步骤)
[自我评价]
3、在日常生活中,我们应用蒸馏的方法可以将海水淡化,或制造无水酒精。若采用蒸馏的方法分离酒精和水的混合物,先蒸馏出来的物质是什么?
(酒精沸点低,先蒸出的是酒精。)
2、为什么温度计水银球的顶端要与圆底烧瓶支管下沿处于同一水平线?
(对于蒸馏来说,只有精确控制蒸馏的温度才能达到分离提纯的目的,而蒸馏烧瓶支管口的温度正是被蒸馏变为气体某组分的温度,故温度计水银球顶端要与圆底烧瓶支管下沿处于同一水平线)
1、为什么冷却水通入方向与被冷凝蒸气流向相反
(为了使蒸馏出的蒸气与冷却水长时间充分接触,带走尽可能多的热量)
1、进行化学实验必须注意安全,下列说法不正确的是:
A.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛
B. 酒精着火时,可用水将其扑灭。
C. 实验室中进行可燃性气体燃烧性质实验时,必须先验纯、后点燃
D. 配制稀硫酸时,可先在量筒中加一定体积的水,再在搅拌下慢慢加入浓硫酸
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com