
4、(2003,北京)取标准状况下CH4和过量O2的混合气体840mL点燃,将燃烧后的气体用过量碱石灰吸收,碱石灰增重0.600g,计算:
(1)碱石灰吸收后所剩气体的体积(标准状况下)
(2)原混合气体中CH4跟O2的体积比。
3、(2000,上海)有效地利用现有能源和开发新能源已受到各国的普遍重视。
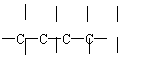
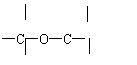

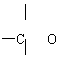 (1)可用改进汽油组成的办法来改改善汽油的燃烧性能。例如,加入CH3OC(CH3)3来生产“无铅汽油”。CH3OC(CH3)3分子中必存在的原子间连接形式有 (填写编号)
(1)可用改进汽油组成的办法来改改善汽油的燃烧性能。例如,加入CH3OC(CH3)3来生产“无铅汽油”。CH3OC(CH3)3分子中必存在的原子间连接形式有 (填写编号)
① ② ③ ④
(2)天然气的燃烧产物无毒、热值高,而且管道输送方便,将成为我国西部开发的重点之一。天然气常和石油伴生,其主要的成分是 。能说明它是正四面体而非正方形平面结构的理由是 (填写编号)
①其一氯取代物不存在同分异构体
②其二氯取代物不存在同分异构体
③它是非极性分子
④它的键长和键角都相等
(3)1980年我国首次制得一辆燃氢汽车,乘员12人,以50km/h行驶了40km。为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发又较经济的制氢方法是 (填写编号)
①电解水 ②锌和稀硫酸反应 ③光解海水
其次,制得纯氢气后还需要解决的问题是 (写出其中一个)。
2、 (2001,上海)目前上海大部分城市居民所使用的燃料主要是管道煤气,浦东新区居民开始使用东海天然气作为民用燃料,管道煤气的主要成分是CO、H2和少量烃类,天燃气的主要成分是CH4,它们的燃烧反应如下:
(2001,上海)目前上海大部分城市居民所使用的燃料主要是管道煤气,浦东新区居民开始使用东海天然气作为民用燃料,管道煤气的主要成分是CO、H2和少量烃类,天燃气的主要成分是CH4,它们的燃烧反应如下:
2CO+O2 2CO2

2H2+O2 2H2O

CH4+2O2 CO2+2H2O
根据以上化学方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是 。因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进方法是 进风口(填“增大”或“减小”),如不作改进可能产生的不良结果是 。管道煤气中含有的烃类,除甲烷外,还有少量乙烷、丙烷、丁烷等,它们的某些性质见下表:
|
|
乙烷 |
丙烷 |
丁烷 |
|
熔点(℃) |
-183.3 |
-189.7 |
-138.4 |
|
沸点(℃) |
-88.6 |
-42.1 |
-0.5 |
试根据以上某个关键数据解释冬天严寒的季节有时管道煤气火焰很小,并且呈断续状态的原因是 .
1、(2005,北京)CO、CH4均为常见的可燃性气体。
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是 。
(2)已知在101kPa时,CO的燃烧热是283kj/mol。相同条件下,若2molCH4完全燃烧生成液态水,所放出的热量为1molCO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是 。
(3)120℃、101kPa下,a mL由CO、CH4组成的混合气体在b mLO2完全燃烧后,恢复到原温度和压强。
①若混合气体与O2恰好完全反应,产生bmLCO2,则混合气体中CH4的体积分数为 (保留2位小数)。
②若燃烧后气体体积缩小了 mL,则a与b关系的数学表示式是
。
mL,则a与b关系的数学表示式是
。
6、已知天然气的主要成分CH4是一种会产生“温室效应”的气体,等物质的量的CH4和CO2产生的“温室效应”相比,前者大。下面是有关天然气的几种叙述:①天然气与煤、汽油相比是较清洁的能源;②等质量的CH4和CO2产生的“温室效应”是前者大;③燃烧天然气也是酸雨的成因之一。其中正确的是( )
A、①②③ B、只有① C、①和② D、只有③
高考聚焦:
5、为了减少大气污染,许多城市推广使用清洁燃料。目前,使用的清洁燃料主要有两类:一类是压缩天然气(CNG)另一类是液化石油气。这两类燃料的主要成份是( )
A、碳水化合物 B、碳氢化合物 C、氢气 D、醇类
4、甲烷分子中的四个氢原子都可以被取代。若甲烷分子中的四个氢原子被苯

基取代得到的物质结构如右所示 ,对所得分子的描述中不正确的是( )
A、分子式为C25H20 B、其一氯代物共有三种
C、所有碳原子一定都在同一平面内 D、此物质属于芳香烃类物质
3、有一类组成最简单的有机硅化合物叫硅烷,它的分子组成与烷烃相似。下列有关说法错误的是( )
A、硅烷的分子通式可表示为SinH2n+2
B、甲硅烷燃烧生成SiO2和H2O
C、甲硅烷的密度小于甲烷
D、甲硅烷的热稳定性强于甲烷
2、有下列物质①CH4 ②CCl4 ③CH2Cl2 ④CH3Cl ⑤金刚石⑥晶体硅 其中的键角不是109.5°的物质是( )
A、②⑥ B、③④ C、①⑤ D、③④⑥
1、有四种物质:①金刚石②甲烷③四氯化碳④白磷,其中具有正四面体构型的是( )
A、①②③ B、①③④ C、②③ D、①②③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com