
33.(1) 完成并配平化学方程式(在空格内填入系数或化合物的分子式)
□KMnO4+□KNO2+□ ====== == □MnSO4+□K2SO4+□KNO3+□H2O
(2) 工业废气和汽车尾气排出的氮的氧化物,是空气的重要污染源。目前治理NO污染的方法之一是在400℃左右,有催化剂存在的条件下用NH3将NO还原为 N2和H2O。写出配平后的化学反应方程式: 。
(3) 科学家发现NO除了① 形成酸雨 ② 破坏臭氧层 ③ 与人体血红蛋白化合④ 形
成光化学烟雾外,少量的NO 还是有益的。NO 曾被美国杂志评为“明星分子”,近年来
发现少量的NO 在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,
而成为生命科学研究的热点。
在含 Cu + 的酶的活化中心,亚硝酸根离子可转化为NO。写出 Cu + 和亚硝酸根离子在酸性溶液中的反应的离子方程式(Cu + 被氧化为Cu 2+)。
。
31一定的条件下, 可逆反应: A2(气) + 3B2(气)  2C(气) 达到了化学平衡状态, 测得平衡时 [A2] = 0.5 mol/L, [B2]
= 0.1 mol/L, [C] = 1.6 mol/L. 若A2、B2、C 的起始浓度分别为 a mol/L, b mol/L, c mol/L, 试回答:
2C(气) 达到了化学平衡状态, 测得平衡时 [A2] = 0.5 mol/L, [B2]
= 0.1 mol/L, [C] = 1.6 mol/L. 若A2、B2、C 的起始浓度分别为 a mol/L, b mol/L, c mol/L, 试回答:
(1) a 和 b 应该满足的关系是 _______________________
(2) a 的取值范围是 ____________.
32. As2S3与稀HNO3反应产生砷酸,反应式为:
3 As2S3 + 28 HNO3 + 4 H2O ======= 6 H3AsO4 + 9 H2SO4 +28NO ,
在此反应中, HNO3表现了 性。若有0.3mol As2S3参加反应,共有_______ mol电子发生转移。
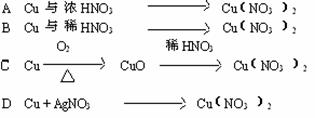
30.从经济效益和环境保护的观点出发,由铜制取硝酸铜最适宜的方法是…( )
29.反应速度v 和反应物浓度的关系是用实验的方法测定的, 化学反应: H2 + Cl2 =
2HCl 的反应速度v 可以表示为: 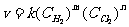 , 式中的k 为常数, m
和 n 值可以用下列表中数据确定之.
, 式中的k 为常数, m
和 n 值可以用下列表中数据确定之.
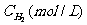 |
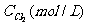 |
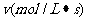 |
|
1.0 |
1.0 |
1.0k |
|
2.0 |
1.0 |
2.0k |
|
2.0 |
4.0 |
4.0k |
由此可以推得, m 和 n 的值正确的是: ………………………………………( )
A. m = 1,n = 2 B. m = 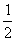 ,n =
,n = 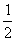 C. m
=
C. m
= 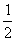 ,n = 1
D. m = 1,n =
,n = 1
D. m = 1,n = 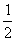
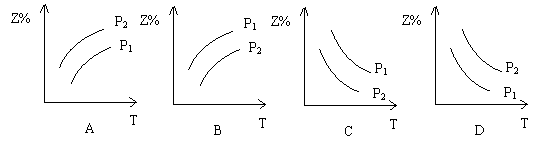
28.反应:X(g) + 3Y(g) 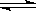 2Z(g) (正反应为放热反应),在不同温度、不同压强(P1>P2)下,达到平衡时,混和气体中Z的百分含量随温度变化的曲线应为……………………………………………………………………( )
2Z(g) (正反应为放热反应),在不同温度、不同压强(P1>P2)下,达到平衡时,混和气体中Z的百分含量随温度变化的曲线应为……………………………………………………………………( )
27.已知某可逆反应:mA(g)+nB(g) 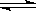 xC(g) (正反应为放热反应),在密闭容器中进行,右图表示反应在不同时间t ,温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则下列说法正确的是…………………………
( )
xC(g) (正反应为放热反应),在密闭容器中进行,右图表示反应在不同时间t ,温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则下列说法正确的是…………………………
( )
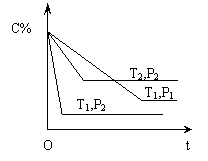 A T1>T2 ,P1>P2 ,m+n>x ,正反应为放热反应
A T1>T2 ,P1>P2 ,m+n>x ,正反应为放热反应
B T1<T2 ,P1<P2 ,m+n<x ,正反应为吸热反应
C T1>T2 ,P1<P2 ,m+n<x ,正反应为放热反应
D T1<T2 ,P1>P2 ,m+n>x ,正反应为吸热反应
26.铜与1mol/L的HNO3溶液反应,如果NO3ˉ下降了0.2mol/L,则H+ 同时下降………………………………………………………………………………( )
A 0.2 mol/L B 0.4 mol/L
C 0.3 mol/L D 0.8 mol/L
25. 如图所示,平衡混合物中X的质量分数(w)在不同的压强下,随温度(T)变化的情况,在下述的哪个平衡体系中,X可以代表用横线标明的物质(反应中各物质均为气态)…………………………( )
如图所示,平衡混合物中X的质量分数(w)在不同的压强下,随温度(T)变化的情况,在下述的哪个平衡体系中,X可以代表用横线标明的物质(反应中各物质均为气态)…………………………( )
A N2
+3H2 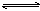 2NH3(正反应为放热反应)
2NH3(正反应为放热反应)
B H2
+ I2 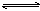 2HI(正反应为放热反应)
2HI(正反应为放热反应)
C
2SO3 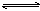 2SO2 +
O2(正反应为吸热反应)
2SO2 +
O2(正反应为吸热反应)
D
4NH3 + 5O2 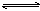 4NO +
6H2O (正反应为放热反应)
4NO +
6H2O (正反应为放热反应)
24.在装有活塞的密闭容器中盛有22.4ml NO,若通入11.2ml O2(均为标准状况),保持温度不变,考虑可逆反应2NO2 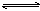 N2O4,则容器内气体的密度…………………………………………………………………………( )
N2O4,则容器内气体的密度…………………………………………………………………………( )
A等于1.369g/L B等于2.054g/L
C在 1.369g/L和2.054g/L之间 D大于2.054g/L
23.如图所示,在一盛有蒸馏水的烧杯中有一悬浮的小球,当向烧杯中加入(或通入)下列物质后,小球沉到水底的是………………………( )
A HCl B NH3 C 浓H2SO4 D 浓HNO3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com