
21.2008年北京奥委会根据近几年我国居民的收入水平制定了下列奥运会票务计划。请根据表格内容,用简洁的语言把你对表格蕴涵的内容的理解表述出来。(不要出现具体数字)(4分)
2008年北京奥运会门票价格表(单位:人民币)
|
门票分类 |
最高价 |
最低价 |
|
预赛门票 |
300元 |
30元 |
|
决赛门票 |
1000元 |
60元 |
|
开幕式门票 |
5000元 |
200元 |
|
闭幕式门票 |
3000元 |
150元 |
|
特殊定价门票 |
鼓励中国青少年到现场观看比赛。预赛票价为5元,决赛票价为10元。这部分门票约占可售票总量的14%。 |
①_______________________________________________________________________
②_______________________________________________________________________
20.注意下列句子相互间用语的逻辑性,把它们组合成语意连贯的一段话。(只填序号)(4分)
①据说在德国的讲台上授课,政府也规定一律都得用德语,
②全球化已成为当今不可遏止的世界趋势。
③而在许多最需使用本民族语言的国际讲坛上,我们却听到了中国代表的满口洋话。
④长期在美国教书的法国人德里达来北京大学作演讲时,开始应我们的学生要求打算用英语,
⑤面对强势文化的入侵,各民族应该怎样对待自己的语言和文化呢?
⑥但法国大使馆坚持要他用法语,因为他是法国人。
____________________________________________________________________
(1)质量守恒定律
参加反应的各种物质的质量总和等于反应后生成的各物质的质量总和。这一定律是书写化学方程式和化学计算的依据。
例5:m molC2H2跟n molH2在密闭容器中反应,当其达到平衡时,生成p mol C2H4。将平衡混合气体完全燃烧生成CO2和H2O,所需氧气的物质量是
A、3m+n B、5/2m+n/2-p/3 C、3m+n+2p D、5m/2+n/2
解析:本题如果按传统的方法也能得出正确结果,但费时多,而利用质量守恒定律解题快而简洁。C~CO2~O2, 4H~2H2O~O2
因此,m molC2~2m molO2 (2m+2n)molH ~(2m+2n)/4 mol O2
总氧气量:2m+(2m+2n)/4=5m/2+n/2 答案为D。
(2)阿佛加德罗定律
在相同温度和压强下,同体积的任何气体都含有相同数目的分子。
阿佛加德罗定律的应用:
①标准状况下气体的体积(L)=22.4mol/L×物质的量(mol)
气体摩尔质量(g/mol)=22.4mol/L×标准状况下气体的密度(g/L)
②同温同压下任何气体的体积比等于其分子个数之比,也等于其物质的量之比
③同温同压下任何气体的密度比等于其相对分子质量之比,也等于同体积的质量之比。
④在温度和体积一定时,气体的压强与物质的量成正比;若温度和压强一定时,气体的体积与物质的量成正比。
⑤在温度与气体的物质的量一定时,其气体的压强与体积成反比。
例6:A容器中盛有体积百分比为80%的H2和20%的O2,试求:
(1)混合气体中H2和O2的分子数之比、质量之比各为多少?
(2)混合气体的平均分子量是多少?它在标准状况下的密度是多少?
(3)在1500C时,引燃混合气体,反应结束后恢复到1500C,则反应后混合气体的平均分子量是多少?引燃前后,,A容器内的压强有什么变化?密度是否变化?
解析:(1)分子数之比等于体积比等于物质的量比,所以
H2和O2的分子数之比为:80%:20%=4:1
质量之比为:4×2:1×32=1:4
(2)混合气体的平均分子量M=2×80%+32×20%=8
在标准状态下r=8/22.4=0.357(g/L)
(3) 2H2 + O2 = 2 H2O
2mol 1mol 2mol
可见,4molH2和1molO2反应后,得到了2mol H2O和2molH2的混合气体,所以
反应后的平均分子量为:18×2/4+2×2/4=10;
在保持温度和体积不变的条件下,气体的压强之比等于物质的量之比
所以 P前:P后=(4+1):(2+2)=5:4。
反应后压强变小,根据质量守恒定律,反应前后的质量不变。
A容器的体积不变,所以混合气体的密度不变。
3、气体摩尔体积:在相同的温度和压强下,1摩尔任何气体所占有的体积在数值上近似相等。人们将一定的温度和强下,单位物质的量的气体所占的体积叫做气体摩尔体积,它的常用单位是:L/mol。
1摩尔任何气体在标准状况下(00C,1.01×105Pa)所占的体积约是22.4L,这个体积叫做标准状况下气体的摩尔体积。记作Vm,其数值为22.4mol/L。
这个概念要同时具备3个要点:①在标准状况下,②1摩尔任何气体,③体积约是22.4L。
例2:下列说法正确的是(NA表示阿伏加德罗常数的值)( )
A.在常温常压下,11.2LN2含有的分子数为0.5NA
B.在常温常压下,1molNe含有的原子数为NA
C.71gCl2所含原子数为2NA
D.在同温同压下,相同体积的任何气体单质所含的原子数相同
答案:B、C
例3:同温同压下,某容器真空时的质量为201克,当它盛满甲烷时的质量为203·4克,而盛满气体Y时质量为205·5克,则Y气体的式量为多少?
解析:本题是考查的内容是气体的特征:即同温同压下,同体积的气体有相同的分子数
(203·4-201)/16=(203·4-201)/M
M=32
知识延伸:混合气体平均分子量:
M=M1×n1%+M2×n2%+M3×n3%
M1、M2、M3、 是每一种气体的相对分子质量;n1% 、n2% 、n3%是混合气体中每一种气体的物质的量分数。
例4:某固体A在一定的温度下分解生成气体B、C、D:2A=B+2C+3D,若测得生成气体的质量是相同体积的H2质量的15倍,则:
(1)生成的混合气体的摩尔质量为多少?
(2)固体A的摩尔质量是多少?
解析:混合气体的平均分子量:M=2×15=30
根据质量守恒定律:2MA=MB+2MC+3MD
而混合气体的平均分子量:M=(MB+2MC+3MD)×1/6=2MA×1/6=30
所以:MA=90
各物理量的相互关系

2、摩尔质量:人们将单位物质的量的物质所具有的质量叫做摩尔质量,它的常用单位为g/mol。物质的量(n)、物质的质量(m)和物质的摩尔质量(M)之间存在着以下关系:
n=m/M
1、物质的量、摩尔:物质的量是国际单位制的七种基本量之一,摩尔是物质的量的单位。每摩尔物质含有阿佛加德罗常数个微粒,阿伏加德罗常数:其数值为0.012 kg 12C 所含的碳原子数,大约为6.02×1023,单位:mol-1
其中微粒指微观粒子如:分子、原子、离子、质子、电子或其它粒子或它们的特定组合。
例1:下列关于物质的量的说法中不正确的是
A.物质的量是国际单位制的7个基本单位之一
B.物质的量实际上表示含有一定数目的粒子集体
C.物质的量的单位是“摩尔”
D.是表示物质数量的单位
解析:不正确的说法是D。
⒈同分异构现象与同分异构体
⑴定义:
⑵存在:①无机物与无机物 ②无机物与有机物 ③有机物与有机物
⑶判断:分子式相同,结构不同
⒉“五同”的比较:
同位素:
同素异形体:
同系物:
同分异构体:
同一物质:(CH2Cl2、H4SiO4)
⒊同分异构体的类别:
⑴C链异构:
同种物质间由于主链碳原子数不同引起的异构现象。如正戊烷、异戊烷、新戊烷。
⑵官能团位置异构:
由于官能团在分子中的位置不同引起的异构现象。如是1-丙醇和 2-丙醇,邻二甲苯、间二甲苯和对二甲苯等。
⑶官能团种类异构:
常见的官能团异构有:
①烯烃和环烷烃:通式为 ②二烯烃和炔烃:通式为
③饱和一元醇和醚:通式为 ④饱和一元醛、酮和烯醇:通式为
⑤饱和一元羧酸、酯和羟基醛:通式为 ⑥芳香醇、芳香醚和酚:通式为
⑦硝基化合物和氨基酸:通式为 ⑧葡萄糖和果糖:分子式为
⑨蔗糖和麦芽糖:分子式为 。
⒋同分异构体的书写:
顺序:先写C链异构,再写官能团位置异构,最后考虑其它官能团种类异构。
⑴烷烃:n<7的烷烃
⑵烯烃:C4H8
⑶烃的含氧衍生物:C5H12O
⒌其它异构:烯烃的顺反异构、烷烃的手性异构
[例1] ⑴由2个C原子、1个O原子、1个N原子和若干个H原子组成的共价化合物,H的原子数目最多为 个,试写出其中一例的结构简式 。
⑵若某共价化合物分子只含有C、N、H三种元素,且以n(C)和n(N)分别表示C和N的原子数目,则H原子数目最多等于 。
⑶若某共价化合物分子中只含有C、N、O、H四种元素,且以n(C),n(N)和n(O)分别
表示C、N和O的原子数目,则H原子数目最多等于 。
[例2]下列物质中,一定是同系物的是( )
A.C2H4和C4H8 B.CH3Cl和CH2Cl2
C.C4H10和C7H16 D.硬脂酸和油酸
[例3]羟酸A(分子式为C5H10O2)可由醇B氧化而得,A与B可生成酯,符合此条件的酯可能有几种?
[例4]为金刚烷的空间结构(碳架)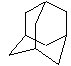
它的一氯代物、二氯代物各有几种?
3.常见有机物的组成、结构、杂化形式、空间构型:
|
|
分子式 |
结构简式 |
空间构形 |
杂化形式 |
化学键 |
|
⑴甲烷 |
|
|
|
|
|
|
⑵乙烯 |
|
|
|
|
|
|
⑶乙炔 |
|
|
|
|
|
|
⑷苯 |
|
|
|
|
|
⒈有机物中C原子的成键特点:
⑴每个C不但可与其它原子形成 个共价键,而且C与C间也可成共价键;
⑵C原子间不仅可以形成C-C,还可以形成 与 ;
⑶多个C原子间可以形成长短不一的C链,C链中带有支链;还可以结合成C环,且C链与C环也可结合;
⑷原子种类、数目相同的分子,原子间有多种结合方式,可出现不同结构的分子,即存在同分异构体。
有机物种类繁多主要是由 和 决定的。
2.有机物的组成与结构的表示方法:
⑴表示有机物组成的化学式:分子式、最简式(实验式)
⑵表示有机物结构的化学式:
电子式、结构式、结构简式(示性式)、键线式(骨架式)
结构简式:结构式的简写形式,省略部分或全部C-C、C-H后的式子,双、三键不省。
键线式:省略CH元素符号,用“-”表示碳碳键,每个拐点或终点均表示一个C原子,
其它元素符合和化学键不省的式子。
⑶表示有机物结构的模型:球棍模型、比例模型
假设你是李华,是广州的一名高中生。你很喜欢学习英语,但是你对英式英语和美式英语的区别不是特别清楚。有些同学说你说美式英语,但有有些人认为你说的是英式英语。你很想知道自己说的是哪种英语以及这两者究竟有什么不同。写一封信给玛丽女士,请她回信解释这两者的主要区别。
注意:1。注意书信格式
2.写信日期是九月十四日
3.字数至少100个

|
|
版权所有:()
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com