
6.已知向量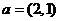 ,
,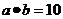 ,
,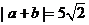 ,则
,则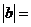
(A)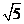 (B)
(B) 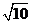 (C) 5 (D) 25
(C) 5 (D) 25
答案:C
解析:将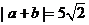 平方即可
平方即可
5.已知正四棱柱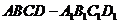 中,
中,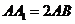 ,E为
,E为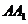 中点,则异面直线BE与
中点,则异面直线BE与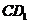 所成角的余弦值为
所成角的余弦值为
(A)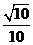 (B)
(B) 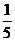 (C)
(C) 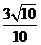 (D)
(D) 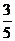
解析:平移成三角形用余弦定理解,或建立坐标系解,注意线线角不大于900
答案:C
4.3.已知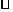 ABC中,cotA=
ABC中,cotA=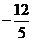 ,则cosA=
,则cosA=
(A)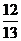 (B)
(B)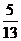 (C)
(C)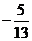 (D)
(D)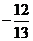
解析:同角三角函数基本关系并注意所在象限的符号
答案:D
3.函数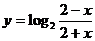 的图像
的图像
A 关于原点对称 B 关于直线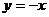 对称 C 关于
对称 C 关于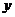 轴对称 D关于直线
轴对称 D关于直线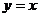 对称
对称
解析:函数奇偶性及对数式定义域及运算
答案:A
2.函数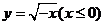 的反函数是
的反函数是
A 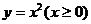 B
B 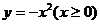 C
C 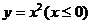 D
D 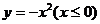
解析:反函数概念
答案:B
1.已知全集U={1,2,3,4,5,6,7,8},M={1,3,5,7},N={5,6,7}
则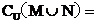
A {5,7} B {2,4} C {2,4,8} D {1,3,5,7}
解析:集合的并补运算
答案:C
31.(4分)下表为NH4Cl、NaCl、KNO3在不同温度下的溶解度,根据表中数据,回答下列问题:
|
|
0℃ |
10℃ |
20℃ |
30℃ |
40℃ |
50℃ |
60℃ |
70℃ |
80℃ |
|
NH4Cl |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
60.2 |
65.6 |
|
NaCl |
35.7 |
35.8 |
36 |
36.3 |
36.6 |
37 |
37.3 |
37.8 |
38.4 |
|
KNO3 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
169 |
⑴写出NH4C1和NaCI具有相同溶解度的温度范围(限相邻两个温度之间) ;
⑵60℃时,配制硝酸钾溶液溶质质量分数最大为 ;
⑶若硝酸钾中含有少量氯化钠,应采取的结晶分离方法是 。
⑷20℃取100克NaCl溶液,温度保持不变,若蒸发10克水,则析出1克食盐,若再若蒸发10克水,则会析出晶体 克。
30.(5分)10g氯化钾溶于90 g水中,将所得溶液平均分成4份,那么第一份溶液中的质量分数为① ,将第二份溶液稀释至100 g,则其溶质的质量分数为② ,欲使第三份溶液的质量分数减小为原来的一半,可加水③ ,欲使第四份溶液的质量分数增大一倍,可加入氯化钾④ 或蒸发掉水⑤ 。
29.(5分)已知硝酸钾溶解度如下:
|
温度(℃) |
0 |
20 |
40 |
60 |
80 |
100 |
|
溶解度(g/100g水) |
13.3 |
31.6 |
63.9 |
110 |
169 |
246 |
⑴ 若将25g硝酸钾晶体放入80g水,配成饱和溶液,温度必须达到什么要求?试计算说明。
⑵ 在60℃时,若有33g硝酸钾晶体与40g水混合,要使之仍在60℃时成为饱和溶液,可采用哪两个方法,试计算说明。
28.(9分)化学反应往往伴随着一些现象发生,但CO2与NaOH溶液的反应没有明显的现象。为了通过一些现象说明CO2与NaOH发生了反应,某班同学分两组作了如下探究实验:
(1)第一组同学把一支收集有CO2的试管倒立在装有饱和NaOH溶液的烧杯中(如右图所示),看到试管内液面上升。这种现象是因为试管内外产生 ( )
A.温度差 B.重力差 C.压强差 D.浮力差
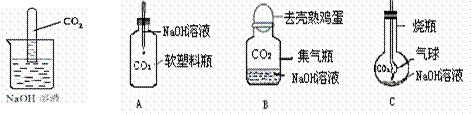
(2)第二组同学从中得到启发,也设计了如下实验装置进行探究:
A现象为 ,B现象为 ,C现象为 。你认为以上设计能达到实验要求的是 (填序号)。
(3)同学们经过分析讨论,认为第一组的实验中产生液面上升现象的原因可能有两种。一种是因为CO2与溶液中的NaOH反应,消耗了CO2,你认为另一种原因是_________________,为了进一步证实CO2与NaOH溶液已经发生了反应,他们设计了如下方案:取上述实验后的溶液,第一组同学滴加 ,现象为 ; 第二组同学滴加 _______ ,现象为 。他们虽然看到的现象不同,但都可以证实CO2与NaOH溶液已经发生了反应。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com