
5.(2006 长沙)根据下列化合物与单质相互转化的关系,回答: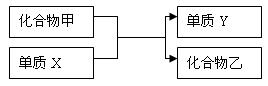
(1)若乙的溶液为浅绿色,Y是红色固体,则X是 。
(2)若在常温下乙是气体,则X是 。
4.某生在实验室发现一没有瓶塞的试剂瓶,里面装有白色固体试剂,瓶上标签已经严重腐蚀,看不清上面的字迹,但可以判断里面所盛试剂由三种元素组成。为确定该白色固体的成分,他取少量该固体配成无色溶液A,然后进行了以下实验:
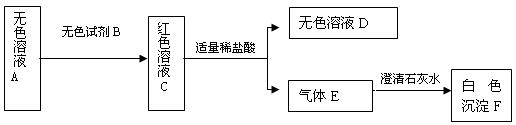
(1)无色试剂B是 (填名称),气体E是 (填化学式,下同),白色沉淀F是 。
(2)若无色溶液D中只含一种溶质NaCl(不考虑前面加入的B试剂),则无色溶液A中一定含有 。
(3)结合题目所给信息判断:原试剂瓶内所盛白色固体可能是 或 。
3.有一包白色固体粉末,可能含有CuSO4、BaCl2、Na2SO4、Na2CO3、KCl中的一种或几种,某同学对其组成进行了探究,过程如下:
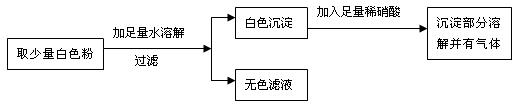
根据以上实验推断,这包白色粉末中一定含有 ;一定不含有 ;可能含有 。
例1 由二种可溶性正盐组成的混合物,为了确定各自成分,某同学设计了以下实验:
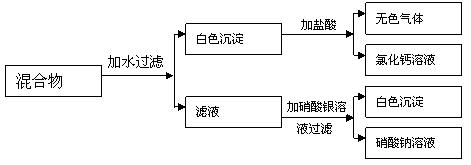
根据以上实验推断,这包白色粉末是什么物质?
2.(2007 十堰中考)实验室有一包由两种盐(不含氢元素)组成的白色粉末和一瓶标签破损的未知酸溶液。为了确定各自成分,某同学设计了以下实验:

已知A是绿色植物光合作用的原料,固体B是农业上常用的两种元素组成的钾肥。
则:气体A是 ;未知酸溶液是 ;组成白色粉末的两种盐是 ;发生反应的化学方程式是 。
例2:已知A、B、C、D、E、F6种物质的转化关系如下:
(1)A+B→C+H2O (2)C+KOH→D↓(蓝色)+E (3)B+D→C+H2O (4)E+BaCl2→F↓(白色,不溶于稀硝酸)+KCl
根据上述变化关系,推断有关物质的化学式:
A ________;B _______;C _______;D________ ;E __________;F _________。
练习:
1,有属于酸、碱、盐的5种常见物质A、B、C、D、E,它们之间可以发生如下反应:
(1)A+B→C+H2O (2)C+H2SO4→D↓+A (3)E+AgNO3→AgCl↓+C
根据上述反应,推断下列各物质的化学式:
A________;B________;C_______;D________;E ____________。
2,(2005 湖南益阳)A、B、C、D是常见的化合物,A中含有钾元素。他们之间的转化关系如下:
①2A+B=C+2H2O ②C+D=BaSO4↓+2A ③D+CuSO4= BaSO4↓+Cu(OH)2↓
根据以上信息,推断A、B两物质化学式:A B ;
写出反应②的化学方程式 。
例1, 某固体混合物可能含有氯化镁、碳酸钙、硫酸铜、碳酸钾和硝酸钠中的一种或几种。现进行以下实验:
(1)将该混合物放入足量水中,得无色透明溶液;
(2)向(1)的溶液 中加入氢氧化钠溶液无明显现象;
(3)在上述(1)的溶液中加入盐酸,有气泡产生。
据上可推断原混合物中肯定有 ,肯定没有 ,可能有 。
用化学方程式表示上述实验中肯定发生的反应。
例2、某固体混合物可能含有氯化钾、碳酸钠、硫酸铜、硫酸钾和硝酸钡。现进行以下实验:(1)将该混合物放入足量水中,产生白色沉淀,得无色透明溶液;
(2)再加入足量的稀硝酸,沉淀全部溶解,逸出无色气体,所得溶液澄清透明;
(3)最后加入稀硫酸,又立刻出现白色沉淀。
据上可推断原混合物中肯定有 ,肯定没有 ,可能有 。用化学方程式表示上述实验中肯定发生的反应。
例3.有一包白色混合物,可能含有硫酸铜、硫酸钡、碳酸钠、氯化钙、硝酸钠、氯化钾中的一种或几种,现做如下实验:
①将混合物放入足量水中,得到无色透明液体
②在上述溶液中加入盐酸,有气泡产生
③在完全反应后的②中滴入硝酸银溶液,有白色沉淀生成。
则原混合物中一定有: 混合物中一定没有 ,可能含有 。
肯定发生的化学方程式是:(1) (2)
练习:1,有一包固体粉末,可能由碳酸钙、硫酸钾、硝酸钠、氯化铁、氯化钡中的一种或几种组成,做实验得到以下结论:
(1) 将此固体粉末加到水中,得到白色沉淀,上层溶液为无色。
(2) 该白色沉淀部分溶于稀硝酸,且有气体放出。
从实验可判断出,该粉末中一定含有____,一定不含有____。
2,有一包固体粉末, 可能含有炭粉、氧化铜、氧化铁、碳酸钙中的一种或几种。进行如下实验: ①取样, 加热至高温产生一种气体, 该气体能使澄清的石灰水变浑浊。②把适量稀盐酸滴入冷却后的固体残渣中, 残存固体全部溶解, 同时产生一种可燃性气体。试推断:
(1) 该固体粉末中一定含有 , 一定没有 。
(2) 该固体粉末中可能含有 , 为证实该物质是否存在, 可选用的试剂是 。
3. 有一包白色固体,可能含有氯化钡、硝酸钾、硫酸铜、氯化钠、碳酸钠、硫酸钠中某几种。(1)取该固体混合物溶于水,有白色沉淀生成,经过滤,得到无色滤液;(2)在白色沉淀中加稀硝酸,沉淀部分溶解;(3)在滤液中滴入硝酸银溶液,生成不溶于稀硝酸的白色沉淀。由此可见:
①混合物中一定有 ;肯定没有 ,可能有 。
②写出(1)(2)反应中的化学方程式:________________________________
4, 有一混合气体由HCl、CO、H2、H2O、CO2组成,将其依次通过①足量氢氧化钠溶液,②浓硫酸,③灼热氧化铜后,剩余气体是 ( )
A、没有气体剩余 B、只有CO2剩余 C、只有H2O 剩余 D、H2O和CO2
5,有一气体可能有CO、CO2、H2、HCL气体的混合物,依次通过(1)澄清的石灰水时无沉淀,(2)通过灼热的氧化铜,黑色粉末变红但无水出现。将剩余气体通过澄清石灰水时,有白色沉淀生成。由此可见:①混合物气体中一定有: ;肯定没有:
6,甲乙两车间的废水中含有Na+、Ag+、Cu2+、CO32-、OH-、NO3- 六种离子:
(1)乙车间的废水呈蓝色,其中的阴离子 为 _______,如果加入足量的铁可以回收的金属有______;
(2)甲车间的废水含有的三种离子是_________;
(3)如果将甲乙两车间的废水混合,可以使废水的某些离子转化为沉淀,经过滤后的废水中含有_______;
(4)写出检验其中一车间废水中含有OH-的方法。
22.下列反应的离子方程式正确的是( )
A.用氨水吸收少量二氧化硫: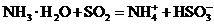
B.碳酸氢钠溶液中加入少量烧碱: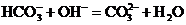
C.碳酸亚铁固体加入稀硝酸: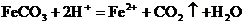
D.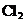 溶解在水中:
溶解在水中: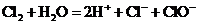
21.下列反应的离子方程式正确的是( )
A.碳酸氢钠溶液跟过量的饱和石灰水反应
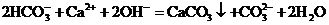
B.向氢氧化钠溶液中加入稀醋酸
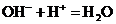
C.向氯化铁溶液中加入铁粉
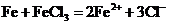
D.向硝酸镁溶液中加过量氨水
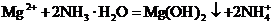
20.下列各组离子中能在水溶液中大量共存,且溶液显酸性的是( )
A.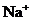 、
、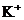 、
、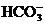 、
、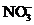 B.
B.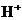 、
、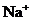 、
、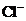 、
、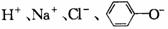
C.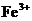 、
、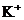 、
、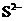 、
、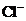 D.
D.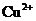 、
、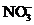 、
、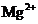 、
、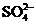
19.下列离子方程式正确的是( )
A.NaHS水解反应: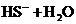

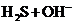
B.石灰石溶于醋酸: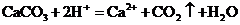
C.Al投入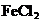 溶液中:
溶液中: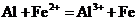
D.往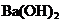 溶液中滴入
溶液中滴入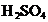 溶液:
溶液: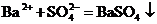
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com