
26. (本题共12分)
(本题共12分)
 (1)a d
(1)a d
 (2)② ③ ④
(2)② ③ ④
 (3)品红溶液褪色:瓶壁有淡黄色粉末和无色的小液滴
(3)品红溶液褪色:瓶壁有淡黄色粉末和无色的小液滴
 (4)
(4)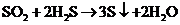 变大
变大
 (5)b
(5)b
 (6)S H2O
(6)S H2O
25. (本题共8分)
(本题共8分)
 (1)
(1)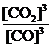

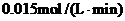
 (2)①CO或(CO2)的生成速率与消耗速率相等;②CO(或CO2)的质量不再改变
(2)①CO或(CO2)的生成速率与消耗速率相等;②CO(或CO2)的质量不再改变
 (合理即给分)
(合理即给分)
 (3) b
(3) b
 (4)
(4)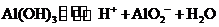 盐酸
(合理即给分)
盐酸
(合理即给分)
24. (本题共8分)
(本题共8分)
 (1)AsH3
(1)AsH3
 (2)Br2
(2)Br2
 (3)a c
(3)a c
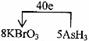
 (4)
(4) 
23. (本题共8分)
(本题共8分)
 (1)
(1)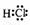 非极性
非极性
 (2)S Cl F 三 IA
(2)S Cl F 三 IA
 (3)a
(3)a
 (4)①不一定容易 ②除F2外,键长增长,键能减小 (合理即给分)
(4)①不一定容易 ②除F2外,键长增长,键能减小 (合理即给分)
18. B、D 19.A、D 20.A、B 21.C 22.A、D
B、D 19.A、D 20.A、B 21.C 22.A、D
 第Ⅱ卷(共84分)
第Ⅱ卷(共84分)
12. B 13.B 14.B 15.A 16.B 17.A
B 13.B 14.B 15.A 16.B 17.A
6. D 7.A 8.D 9.C 10.B 11.C
D 7.A 8.D 9.C 10.B 11.C
1. B 2.D 3.C 4.B 5.C
B 2.D 3.C 4.B 5.C
31. 烟气中
烟气中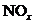 是NO和
是NO和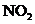 的混合物(不含
的混合物(不含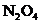 )。
)。
 (1)根据废气排放标准,
(1)根据废气排放标准,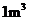 烟气最高允许含400mg
烟气最高允许含400mg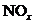 。若
。若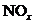 中NO质量分数为0.85,则
中NO质量分数为0.85,则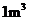 烟气中最高允许含NO__________L(标准状况,保留2位小数)。
烟气中最高允许含NO__________L(标准状况,保留2位小数)。
 (2)工业上通常用溶质质量分数为0.150的
(2)工业上通常用溶质质量分数为0.150的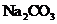 水溶液(密度1.16g/mL)作为
水溶液(密度1.16g/mL)作为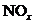 吸收剂,该碳酸钠溶液物质的量浓度为____________mol/L(保留2位小数)。
吸收剂,该碳酸钠溶液物质的量浓度为____________mol/L(保留2位小数)。
 (3)已知:
(3)已知: 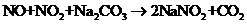 ①
①

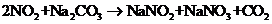 ②
②

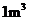 含2000mg
含2000mg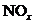 的烟气用质量分数为0.150的碳酸钠溶液吸收。若吸收率为80%,吸收后的烟气_______排放标准(填“符合”或“不符合”),理由:____________________。
的烟气用质量分数为0.150的碳酸钠溶液吸收。若吸收率为80%,吸收后的烟气_______排放标准(填“符合”或“不符合”),理由:____________________。
 (4)加入硝酸可改变烟气中NO和NO2的比,反应为:
(4)加入硝酸可改变烟气中NO和NO2的比,反应为:
 NO+2HNO3→3NO2+H2O
NO+2HNO3→3NO2+H2O
 当烟气中
当烟气中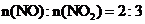 时,吸收率最高。
时,吸收率最高。

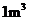 烟气含2000mg
烟气含2000mg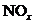 ,其中
,其中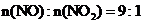 。
。
 计算:(i)为了达到最高吸收率,
计算:(i)为了达到最高吸收率,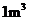 烟气需用硝酸的物质的量(保留3位小数)。
烟气需用硝酸的物质的量(保留3位小数)。
 (ii)
(ii)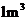 烟气达到最高吸收率90%时,吸收后生成NaNO2的质量(假设上述吸收反应中,反应①比反应②迅速。计算结果保留1位小数)。
烟气达到最高吸收率90%时,吸收后生成NaNO2的质量(假设上述吸收反应中,反应①比反应②迅速。计算结果保留1位小数)。
答案:
 (1)0.25
(1)0.25
 (2)1.64
(2)1.64
 (3)不符合 因吸收后烟气总体积减小,
(3)不符合 因吸收后烟气总体积减小,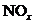 含量仍超过
含量仍超过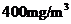
 (4)(i)
(4)(i)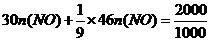
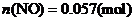

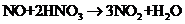

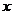
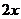
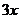

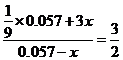
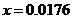
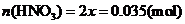
 (ii)
(ii)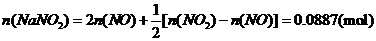

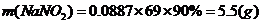
解析:(1)1L烟气中最高允许含NO质量为400×10-3g×0.85=0.34g
其体积为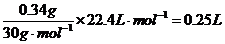
(2)此题考查物质的量浓度与质量分数的换算,可直接利用公式求解。
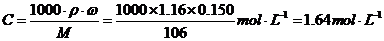
(3)若烟气中的其他成分不被吸收,刚好达到排放标准,但烟气中的CO2等酸性气体也能被吸收,所以吸收后烟气中NOx的含量仍超标。
























 上海 化学参考答案
上海 化学参考答案
 第I卷(共66分)
第I卷(共66分)
30. 臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧:
臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧: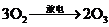
 (1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为______g/mol
(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为______g/mol
 (保留一位小数)。
(保留一位小数)。
 (2)将8L氧气通过放电管后,恢复到原状况,得到气体6.5L,其中臭氧为_____________L。
(2)将8L氧气通过放电管后,恢复到原状况,得到气体6.5L,其中臭氧为_____________L。
 (3)实验室将氧气和臭氧的混合气体0.896L(标准状况)通入盛有20.0g铜粉的反应器中,充分加热后,粉末的质量变为21.6g。则原混合气中臭氧的体积分数为__________________。
(3)实验室将氧气和臭氧的混合气体0.896L(标准状况)通入盛有20.0g铜粉的反应器中,充分加热后,粉末的质量变为21.6g。则原混合气中臭氧的体积分数为__________________。
答案:
 (1)35.6
(1)35.6  (2)3
(2)3  (3)0.5
(3)0.5
[解析](1)假设有1mol O2,则
3O2 2O3
开始 1mol 0
反应 0.3mol 0.2mol
平衡 0.7mol 0.2mol
所以平均摩尔质量为: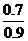 ×32g·mol-1+
×32g·mol-1+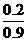 ×48g·mol-1=35.6g·mol-1
×48g·mol-1=35.6g·mol-1
(2)此题应根据差量法计算
3O2  2O3
2O3 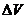
开始 8L 0
反应 4.5L 3L 1.5L
(3)n(混合气体)=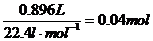
设臭氧的体积分数为a,则根据氧原子守恒0.04mol·a·2+0.04mol·(1-a)·3=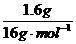
解得a=0.5

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com