
8. 在下列给定条件的溶液中,一定能大量共存的离子组是
在下列给定条件的溶液中,一定能大量共存的离子组是
A.无色溶液: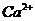 、、H+、
、、H+、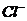 、
、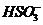
B.能使pH试纸呈红色的溶液:Na+、NH+4、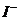 、
、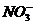
C.FeCl2溶液:K+、、Na+、、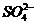 、、
、、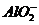
D.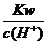 =0.1 mol/L的溶液:Na+、K+、
=0.1 mol/L的溶液:Na+、K+、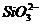 、
、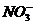
答案D
 [解析]A项中H+与HSO3-不能大量共存;B项隐含条件是酸性溶液NO3-在酸性条件下具有强氧化性,可氧化I-,C项中Fe2+和AlO2-可发生双水解而不能大量共存。 D项为碱性条件,可大量存在。
[解析]A项中H+与HSO3-不能大量共存;B项隐含条件是酸性溶液NO3-在酸性条件下具有强氧化性,可氧化I-,C项中Fe2+和AlO2-可发生双水解而不能大量共存。 D项为碱性条件,可大量存在。
 [考点分析]离子共存
[考点分析]离子共存
7.下列有关物质检验的实验结论正确的是
|
选项 |
实 验 操 作 及 现 象 |
实 验 结 论 |
|
A |
向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 |
该溶液中一定含有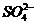 |
|
B |
向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入几滴新制的氯水,溶液变为红色 |
该溶液中一定含有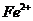 |
|
C |
将某气体通入品红溶液中,品红溶液褪色 |
该气体一定是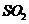 |
|
D |
将少量某物质的溶液滴加到新制的银氨溶液中,水浴加热后有银镜生成 |
该物质一定属于醛类 |
答案B
[解析]A项可能受到Ag+影响生成AgCl沉淀;C能够使品红溶液褪色的气体不一定就是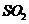 还可能是其他气体比如氯气;D、能发生银镜反应的官能团为醛基,而醛基还可能存在与甲酸或甲酸某酯、甲酸盐中。
还可能是其他气体比如氯气;D、能发生银镜反应的官能团为醛基,而醛基还可能存在与甲酸或甲酸某酯、甲酸盐中。
[考点分析]常见离子检验、物质鉴别综合运用
6.开发新材料是现代科技发展的方向之一。下列有关材料的说法正确的是
A. 氮化硅陶瓷是新型无机非金属材料
B. C60属于原子晶体,用于制造纳米材料
C. 纤维素乙酸酯属于天然高分子材料
D. 单晶硅常用于制造光导纤维
答案A
[解析]B、C60为分子晶体;B、纤维素为天然高分子化合物,而纤维素硝酸酯是人工合成的、D、二氧化硅是制造光导纤维的主要材料。
[考点分析]本题主要考查化学与生活、化学基本概念.
28. 答案
答案 (1)FeS2
(1)FeS2

 (2)
(2)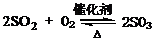

 (3)a b d
(3)a b d

 (4)SO3(g) + H2O(l)
= H2SO4(l);ΔH=-130.3kJ/mol
(4)SO3(g) + H2O(l)
= H2SO4(l);ΔH=-130.3kJ/mol

 (5)①SO2
+ Br2 + 2H2O = 4H+ + 2Br- + SO42-
(5)①SO2
+ Br2 + 2H2O = 4H+ + 2Br- + SO42-

 ②14.56 2.31g
②14.56 2.31g


 [解析]本题主要考查硫酸工业、热化学方程式的书写、计算等。
[解析]本题主要考查硫酸工业、热化学方程式的书写、计算等。
 (1)根据原子守恒即可判断该物质为FeS2。
(1)根据原子守恒即可判断该物质为FeS2。
 (2)SO2和O2在接触室发生反应生成SO3:2SO2 + O2
(2)SO2和O2在接触室发生反应生成SO3:2SO2 + O2
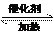 2SO3。
2SO3。
 (3)选项a,将黄铁矿粉碎更增加反应接触面积而加快反应速率。选项b,增加空气(O2)浓度能提高SO2的转化率。选项c,催化剂对转化率无影响。选项d,矿渣中含有Fe2O3,可用于冶炼铁。
(3)选项a,将黄铁矿粉碎更增加反应接触面积而加快反应速率。选项b,增加空气(O2)浓度能提高SO2的转化率。选项c,催化剂对转化率无影响。选项d,矿渣中含有Fe2O3,可用于冶炼铁。
 (4)160g SO3(g)与H2O(l)反应生成H2SO4(l)放出260.6kJ热量,则1mol SO3(g)与H2O(l)反应生成H2SO4(l)放出130.3kJ热量,则相关热化学方程式为: SO3(g) + H2O(l)=H2SO4(l);△H=-130.3kJ/mol。
(4)160g SO3(g)与H2O(l)反应生成H2SO4(l)放出260.6kJ热量,则1mol SO3(g)与H2O(l)反应生成H2SO4(l)放出130.3kJ热量,则相关热化学方程式为: SO3(g) + H2O(l)=H2SO4(l);△H=-130.3kJ/mol。
 (5)10g时说明铵盐不足,20g时说明氢氧化钠不足,由10.00g和20.00g 时浓硫酸增加的质量相同说明铵盐有酸式根产生的氨气, 氢氧化钠的物质的量浓度为Cmol/L
(5)10g时说明铵盐不足,20g时说明氢氧化钠不足,由10.00g和20.00g 时浓硫酸增加的质量相同说明铵盐有酸式根产生的氨气, 氢氧化钠的物质的量浓度为Cmol/L
 设10克中有Xmol的 (NH4)2SO4 和ymol的NH4HSO4则
设10克中有Xmol的 (NH4)2SO4 和ymol的NH4HSO4则
 132X + 115y=10…………………………………………………….(1)
132X + 115y=10…………………………………………………….(1)
 10g时说明铵盐不足由N守恒知
10g时说明铵盐不足由N守恒知
 n(NH3)=2X + y
n(NH3)=2X + y
 20g时铵盐已经过量,氢氧化钠先和酸式根反应,则(NH4)2SO4为2Xmol,2ymol的NH4HSO4
20g时铵盐已经过量,氢氧化钠先和酸式根反应,则(NH4)2SO4为2Xmol,2ymol的NH4HSO4
 HSO4-
+ OH-
= SO42- + H2O
HSO4-
+ OH-
= SO42- + H2O
 1 1
1 1
 2y 2y
2y 2y
 NH4+ + OH- = NH3 +
H2O
NH4+ + OH- = NH3 +
H2O
 1
1
1
1
 50C×10-3-2y 50C×10-3-2y
50C×10-3-2y 50C×10-3-2y
 由于产生的氨气一样多
由于产生的氨气一样多
 n(NH3)=2X
+ y=50C×10-3-2y………………………………….(2)
n(NH3)=2X
+ y=50C×10-3-2y………………………………….(2)
 30g时铵盐过量,则(NH4)2SO4为3Xmol,3ymol的NH4HSO4 n(NH3)=0.68/17=0.04mol
30g时铵盐过量,则(NH4)2SO4为3Xmol,3ymol的NH4HSO4 n(NH3)=0.68/17=0.04mol
 HSO4- + OH- = SO42- + H2O
HSO4- + OH- = SO42- + H2O
 1 1
1 1
 3y 3y
3y 3y
 NH4+ + OH- =
NH3
+ H2O
NH4+ + OH- =
NH3
+ H2O
 1
1
1
1
 50C×10-3-3y
0.04
50C×10-3-3y
0.04
 所以
所以
 50C×10-3-3y=0.04…………………………………………………….(3)
50C×10-3-3y=0.04…………………………………………………….(3)
 联立(1) (2) (3)解得
联立(1) (2) (3)解得
 X=0.02mol
y=0.064mol
C=4.64mol/L
X=0.02mol
y=0.064mol
C=4.64mol/L
 氮的质量百分含量=
氮的质量百分含量=  ×100%=(0.04+0.064)
×14/10×100%=14.56%
×100%=(0.04+0.064)
×14/10×100%=14.56%
 15g时铵盐已经过量,则(NH4)2SO4为1.5Xmol,1.5 ymol的NH4HSO4
15g时铵盐已经过量,则(NH4)2SO4为1.5Xmol,1.5 ymol的NH4HSO4
 HSO4- + OH- = SO42-
+ H2O
HSO4- + OH- = SO42-
+ H2O
 1
1
1
1
 1.5y 1.5y
1.5y 1.5y
 NH4+ + OH- =
NH3
+ H2O
NH4+ + OH- =
NH3
+ H2O
 1
1
1
1
 50C×10-3-1.5y 50C×10-3-1.5y
50C×10-3-1.5y 50C×10-3-1.5y
 n(NH3)=
50C×10-3-1.5y=50×4.64×10-3-1.5×0.064=0.136mol
n(NH3)=
50C×10-3-1.5y=50×4.64×10-3-1.5×0.064=0.136mol
 m(NH3)=0.136×17=2.31g
m(NH3)=0.136×17=2.31g


28. (15分)
(15分)
 以黄铁矿为原料生产硫酸的工艺流程图如下:
以黄铁矿为原料生产硫酸的工艺流程图如下:


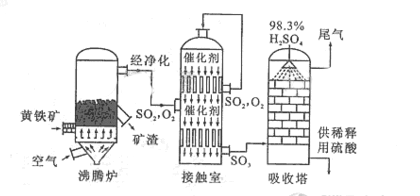

 (1)将燃烧黄铁矿的化学方程式补充完整
(1)将燃烧黄铁矿的化学方程式补充完整
 4 +11
4 +11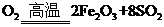
 (2)接触室中发生反应的化学方程式是 。
(2)接触室中发生反应的化学方程式是 。
 (3)依据工艺流程图判断下列说法正确的是(选填序号字母)
。
(3)依据工艺流程图判断下列说法正确的是(选填序号字母)
。
 a. 为使黄铁矿充分燃烧,需将其粉碎
a. 为使黄铁矿充分燃烧,需将其粉碎
 b. 过量空气能提高
b. 过量空气能提高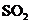 的转化率
的转化率
 c. 使用催化剂能提高
c. 使用催化剂能提高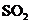 的反应速率和转化率
的反应速率和转化率
 d. 沸腾炉排出的矿渣可供炼铁
d. 沸腾炉排出的矿渣可供炼铁
 (4)每160g
(4)每160g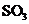 气体与
气体与 化合放出260.6kJ的热量,该反应的热化学方程是 。
化合放出260.6kJ的热量,该反应的热化学方程是 。
 (5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的
(5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的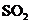 和铵盐。
和铵盐。
 ①
①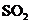 既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的
既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的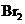 。
。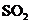 吸收
吸收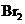 的离子方程式是 。
的离子方程式是 。
 ②
为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的
②
为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的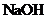 溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。
溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。
 部分测定结果;
部分测定结果;
 铵盐质量为10.00g和20.00g 时,浓硫酸增加的质量相同;铵盐质量为30.00g时,浓硫酸增加的质量为0.68g;铵盐质量为40.00g时,浓硫酸的质量不变。
铵盐质量为10.00g和20.00g 时,浓硫酸增加的质量相同;铵盐质量为30.00g时,浓硫酸增加的质量为0.68g;铵盐质量为40.00g时,浓硫酸的质量不变。
 计算:该铵盐中氮元素的质量分数是
%; 若铵盐质量为15.00g。
浓硫酸增加的质量为 。
(计算结果保留两位小数)
计算:该铵盐中氮元素的质量分数是
%; 若铵盐质量为15.00g。
浓硫酸增加的质量为 。
(计算结果保留两位小数)
27. 答案
答案 (1)3mol/L稀硝酸、浓硝酸、氢氧化钠溶液
(1)3mol/L稀硝酸、浓硝酸、氢氧化钠溶液

 (2)通入CO2一段时间,关闭弹簧夹,将装置⑤中导管末端伸入倒置的烧瓶内
(2)通入CO2一段时间,关闭弹簧夹,将装置⑤中导管末端伸入倒置的烧瓶内

 (3)Cu + 4HNO3(浓)= Cu(NO3)2 + 2NO2↑ + 2H2O
(3)Cu + 4HNO3(浓)= Cu(NO3)2 + 2NO2↑ + 2H2O

 (4)将NO2转化为NO 3NO2 +
H2O =2HNO3 + NO
(4)将NO2转化为NO 3NO2 +
H2O =2HNO3 + NO

 (5)装置③中液面上方气体仍为无色,装置④中液面上方气体由无色变为红棕色
(5)装置③中液面上方气体仍为无色,装置④中液面上方气体由无色变为红棕色

 (6)a c d
(6)a c d

 [解析]本题主要考查HNO3的性质、化学基本实验设计和评价能力。(1)根据装置特点和实验目的,装置⑤是收集NO,装置⑥中盛放NaOH溶液吸收NO2,因为要验证稀HNO3不能氧化NO,所以装置③中应该盛放稀硝酸。
[解析]本题主要考查HNO3的性质、化学基本实验设计和评价能力。(1)根据装置特点和实验目的,装置⑤是收集NO,装置⑥中盛放NaOH溶液吸收NO2,因为要验证稀HNO3不能氧化NO,所以装置③中应该盛放稀硝酸。
 (2)由于装置中残存的空气能氧化NO而对实验产生干扰,所以滴加浓HNO3之前需要通入一段时间CO2赶走装置中的空气,同时也需将装置⑤中导管末端伸入倒置的烧瓶内防止反应产生的NO气体逸出。
(2)由于装置中残存的空气能氧化NO而对实验产生干扰,所以滴加浓HNO3之前需要通入一段时间CO2赶走装置中的空气,同时也需将装置⑤中导管末端伸入倒置的烧瓶内防止反应产生的NO气体逸出。
 (3)Cu与浓HNO3反应生成Cu(NO3)2、NO2、H2O:Cu + 4HNO3(浓)=Cu(NO3)2 + 2NO2↑ +2 H2O。
(3)Cu与浓HNO3反应生成Cu(NO3)2、NO2、H2O:Cu + 4HNO3(浓)=Cu(NO3)2 + 2NO2↑ +2 H2O。
 (4)装置②中盛放H2O,使NO2与H2O反应生成NO:3NO2 + H2O=2HNO3 + NO。
(4)装置②中盛放H2O,使NO2与H2O反应生成NO:3NO2 + H2O=2HNO3 + NO。
 (5)NO通过稀HNO3溶液后,若无红棕色NO2产生,说明稀HNO3不能氧化NO,所以盛放稀HNO3装置的液面上方没有颜色变化即可说明之。装置④中盛放的是浓HNO3,若浓HNO3能氧化NO则装置④液面的上方会产生红棕色气体。
(5)NO通过稀HNO3溶液后,若无红棕色NO2产生,说明稀HNO3不能氧化NO,所以盛放稀HNO3装置的液面上方没有颜色变化即可说明之。装置④中盛放的是浓HNO3,若浓HNO3能氧化NO则装置④液面的上方会产生红棕色气体。
 (6)要证明是Cu(NO3)2浓度过低或是溶解了NO2导致装置①中溶液呈绿色,一是可设计将溶解的NO2赶走(a、c方案)再观察颜色变化。二是增加溶液中Cu(NO3)2溶液的浓度(d方案)观察反应后的颜色变化。
(6)要证明是Cu(NO3)2浓度过低或是溶解了NO2导致装置①中溶液呈绿色,一是可设计将溶解的NO2赶走(a、c方案)再观察颜色变化。二是增加溶液中Cu(NO3)2溶液的浓度(d方案)观察反应后的颜色变化。
27. (14分)
(14分)
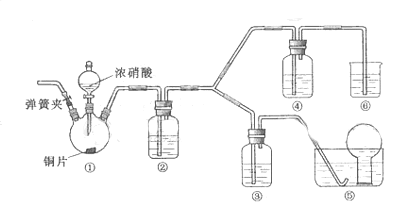
 某学习小组探究浓、稀硝酸氧化性的相对强弱的,按下图装置进行试验(夹持仪器已略去)。实验表明浓硝酸能将
某学习小组探究浓、稀硝酸氧化性的相对强弱的,按下图装置进行试验(夹持仪器已略去)。实验表明浓硝酸能将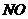 氧化成
氧化成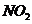 ,而稀硝酸不能氧化
,而稀硝酸不能氧化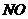 。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
。由此得出的结论是浓硝酸的氧化性强于稀硝酸。

 可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
 已知:氢氧化钠溶液不与
已知:氢氧化钠溶液不与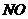 反应,能与
反应,能与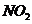 反应
反应

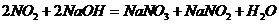
(1)  实验应避免有害气体排放到空气中,装置③、④、⑥中乘放的药品依次是
实验应避免有害气体排放到空气中,装置③、④、⑥中乘放的药品依次是
(2)  滴加浓硝酸之前的操作时检验装置的气密性,加入药品,打开弹簧夹后
滴加浓硝酸之前的操作时检验装置的气密性,加入药品,打开弹簧夹后
(3)  装置①中发生反应的化学方程式是
装置①中发生反应的化学方程式是
(4)  装置②的作用是
,发生反应的化学方程式是
装置②的作用是
,发生反应的化学方程式是
(5)  该小组得出的结论一局的试验现象是
该小组得出的结论一局的试验现象是
(6)  试验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别涉及了一下4个试验来判断两种看法是否正确。这些方案中可行的是(选填序号字母)
试验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别涉及了一下4个试验来判断两种看法是否正确。这些方案中可行的是(选填序号字母)
a.
 加热该绿色溶液,观察颜色变化
加热该绿色溶液,观察颜色变化
b.
 加水稀释绿色溶液,观察颜色变化
加水稀释绿色溶液,观察颜色变化
c.
 向该绿色溶液中通入氮气,观察颜色变化
向该绿色溶液中通入氮气,观察颜色变化
d.
 向饱和硝酸铜溶液中通入浓硝酸与铜反映产生的气体,观察颜色变化
向饱和硝酸铜溶液中通入浓硝酸与铜反映产生的气体,观察颜色变化
26. (15分)
(15分)
 以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略);
以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略);
 I 从废液中提纯并结晶处FeSO4·7H2O。
I 从废液中提纯并结晶处FeSO4·7H2O。
 II将
II将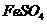 溶液与稍过量的
溶液与稍过量的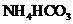 溶液混合,得到含
溶液混合,得到含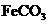 的浊液
的浊液
 IV 将浊液过滤,用90°C热水洗涤沉淀,干燥后得到
IV 将浊液过滤,用90°C热水洗涤沉淀,干燥后得到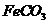 固体
固体
 V煅烧
V煅烧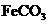 ,得到
,得到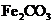 固体
固体
 已知:
已知: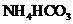 在热水中分解
在热水中分解
(1)
 I中,加足量的铁屑出去废液中的
I中,加足量的铁屑出去废液中的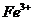 ,该反应的离子方程式是
,该反应的离子方程式是
(2)
 II中,需加一定量硫酸,运用化学平衡原理简述硫酸的作用
II中,需加一定量硫酸,运用化学平衡原理简述硫酸的作用
(3)
 III中,生成
III中,生成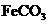 的离子方程式是
。若
的离子方程式是
。若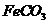 浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是
。
浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是
。
(4)
 IV中,通过检验
IV中,通过检验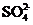 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验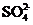 操作是是
。
操作是是
。
(5)
 已知煅烧
已知煅烧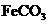 的化学方程式是
的化学方程式是 ,现煅烧464.0kg的
,现煅烧464.0kg的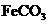 ,得到316.8kg产品,若产品中杂质只有
,得到316.8kg产品,若产品中杂质只有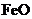 ,则该产品中
,则该产品中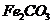 的质量是
kg(摩尔质量/g·
的质量是
kg(摩尔质量/g·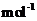 ;
;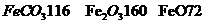 )
)
 答案.
答案.  (1)Fe +
2Fe3+ = 3Fe2+
(1)Fe +
2Fe3+ = 3Fe2+

 (2)加入硫酸,H+浓度增大,使Fe2+ + 2H2O
(2)加入硫酸,H+浓度增大,使Fe2+ + 2H2O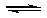 Fe(OH)2 + 2H+的平衡向逆反应方向移动,从而抑制FeSO4的水解
Fe(OH)2 + 2H+的平衡向逆反应方向移动,从而抑制FeSO4的水解

 (3)Fe2+ + 2HCO3-
= FeCO3↓+ CO2
↑ + H2O
(3)Fe2+ + 2HCO3-
= FeCO3↓+ CO2
↑ + H2O

 4FeCO3 + 6H2O
+ O2 = 4Fe(OH)3 ↓+ 4CO2
4FeCO3 + 6H2O
+ O2 = 4Fe(OH)3 ↓+ 4CO2

 (4)取少量洗涤后的滤液放入试管中,滴加酸化的BaCl2溶液,若无白色沉淀产生,则沉淀洗涤干净
(4)取少量洗涤后的滤液放入试管中,滴加酸化的BaCl2溶液,若无白色沉淀产生,则沉淀洗涤干净

 (5)288.0
(5)288.0
 [解析]本题考查化学实验基本操作、物质的制备、化学反应原理、计算等。(1)Fe3+具有氧化性,能氧化Fe生成Fe2+:2Fe3+ + Fe=3Fe2+。
[解析]本题考查化学实验基本操作、物质的制备、化学反应原理、计算等。(1)Fe3+具有氧化性,能氧化Fe生成Fe2+:2Fe3+ + Fe=3Fe2+。
 (2)由于Fe2+水解,加入H2SO4可阻止其水解。
(2)由于Fe2+水解,加入H2SO4可阻止其水解。
 (3)Fe2+与HCO3―在溶液中发生双水解生成FeCO3:Fe2+ + 2HCO3―=FeCO3↓+ CO2↑+ H2O。FeCO3在被O2氧化最终生成Fe(OH)3而出现红褐色:4FeCO3 + O2 + H2O=Fe(OH)3 ↓+ 4CO2↑。
(3)Fe2+与HCO3―在溶液中发生双水解生成FeCO3:Fe2+ + 2HCO3―=FeCO3↓+ CO2↑+ H2O。FeCO3在被O2氧化最终生成Fe(OH)3而出现红褐色:4FeCO3 + O2 + H2O=Fe(OH)3 ↓+ 4CO2↑。
 (4)SO42―的检验一般采用BaCl2溶液,根据溶液与BaCl2溶液反应是否有白色沉淀产生来判断溶液中是否存在SO42―。
(4)SO42―的检验一般采用BaCl2溶液,根据溶液与BaCl2溶液反应是否有白色沉淀产生来判断溶液中是否存在SO42―。
 (5)464kg FeCO3中含有Fe元素4×103mol,设产品中FeO xmol ,Fe2O3ymol,则有:x + 2y=4×103,72x + 160y=316.8×103,解得x=2.2×103mol,y=1.8×103mol,故Fe2O3的质量=1.8×103mol×160g/mol=288.0kg。
(5)464kg FeCO3中含有Fe元素4×103mol,设产品中FeO xmol ,Fe2O3ymol,则有:x + 2y=4×103,72x + 160y=316.8×103,解得x=2.2×103mol,y=1.8×103mol,故Fe2O3的质量=1.8×103mol×160g/mol=288.0kg。
25. (16分)
(16分)

 丙烯可用于合成是杀除根瘤线虫的农药(分子式为
丙烯可用于合成是杀除根瘤线虫的农药(分子式为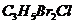 )和应用广泛的DAP树脂;
)和应用广泛的DAP树脂;


 已知脂与酯克发生如下酯交换反应:
已知脂与酯克发生如下酯交换反应:

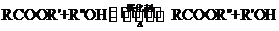 (R,R’ R’’代表羟基)
(R,R’ R’’代表羟基)
 (1)农药
(1)农药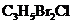 分子中每个碳原子上均连有卤原子。
分子中每个碳原子上均连有卤原子。
 ①A的结构简式是
①A的结构简式是
 A 含有的官能团名称是
;
A 含有的官能团名称是
;
 ②由丙烯生成A的反应类型是
②由丙烯生成A的反应类型是
 (2)A水解可得到D,该水解反应的化学方程式是
。
(2)A水解可得到D,该水解反应的化学方程式是
。
 (3)C蒸汽密度是相同状态下甲烷密度的6.25倍,C中各元素的质量分数分别为
(3)C蒸汽密度是相同状态下甲烷密度的6.25倍,C中各元素的质量分数分别为
 碳60%,氢8%,氧32% ,C的结构简式是
。
碳60%,氢8%,氧32% ,C的结构简式是
。
 (4)下列说法正确的是(选填序号字母)
(4)下列说法正确的是(选填序号字母)
 a.能发生聚合反应,还原反映和氧化反映
a.能发生聚合反应,还原反映和氧化反映
 b.C含有两个甲基的羟酸类同分异构体有4个
b.C含有两个甲基的羟酸类同分异构体有4个
 c D催化加氢的产物与B具有相同的相对分子质量
c D催化加氢的产物与B具有相同的相对分子质量
 d E有芳香气味,易溶于乙醇
d E有芳香气味,易溶于乙醇
 (5)E的水解产物经分离子最终的到甲醇和B,二者均可循环利用DAP树脂的制备。其中将甲醇与H分离的操作方法是
(5)E的水解产物经分离子最终的到甲醇和B,二者均可循环利用DAP树脂的制备。其中将甲醇与H分离的操作方法是
 (6)F的分子式为
(6)F的分子式为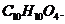 DAP单体为苯的二元取代物,且两个取代基部处于对位,
DAP单体为苯的二元取代物,且两个取代基部处于对位,
 该单体苯环上的一溴取代物只有两种。D和F反应生成DAP单体的化学方程式
该单体苯环上的一溴取代物只有两种。D和F反应生成DAP单体的化学方程式
 。
。
 答案.
答案. (1)①
(1)①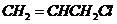 碳碳双键、氯原子 ②取代反应
碳碳双键、氯原子 ②取代反应


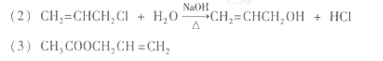

 (4)a c d
(4)a c d

 (5)蒸馏
(5)蒸馏



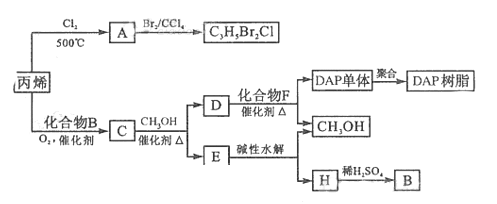
 [解析]本题考查有机推断、典型有机反应类型、同分异构、有机结构与性质。(1)CH3CH=CH2在500℃时与Cl2发生取代反应生成A(ClCH2CH=CH2),
[解析]本题考查有机推断、典型有机反应类型、同分异构、有机结构与性质。(1)CH3CH=CH2在500℃时与Cl2发生取代反应生成A(ClCH2CH=CH2),
 ClCH2CH=CH2与Br2发生加成反应生成ClCH2CHBr-CH2Cl。ClCH2CH=CH2含有碳碳双键和氯原子两种官能团。
ClCH2CH=CH2与Br2发生加成反应生成ClCH2CHBr-CH2Cl。ClCH2CH=CH2含有碳碳双键和氯原子两种官能团。
 (2)ClCH2CH=CH2在NaOH溶液中发生水解反应生成HOCH2CH=CH2,其反应方程式为:ClCH2CH=CH2 + H2O
(2)ClCH2CH=CH2在NaOH溶液中发生水解反应生成HOCH2CH=CH2,其反应方程式为:ClCH2CH=CH2 + H2O
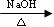 CH2=CHCH2OH + HCl。
CH2=CHCH2OH + HCl。
 (3)C的相对分子质量=16×6.25=100,C:H:O=
(3)C的相对分子质量=16×6.25=100,C:H:O=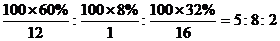 ,C的分子式为C5H8O2。C与CH3OH发生酯交换反应生成D、E,E能发生水解反应,说明E为酯,H为羧酸的钠盐,B为羧酸,结合C和丙烯的分子式,推知B为CH3COOH,C为CH3COOCH2CH=CH2,D为CH2=CHCH2OH。
,C的分子式为C5H8O2。C与CH3OH发生酯交换反应生成D、E,E能发生水解反应,说明E为酯,H为羧酸的钠盐,B为羧酸,结合C和丙烯的分子式,推知B为CH3COOH,C为CH3COOCH2CH=CH2,D为CH2=CHCH2OH。
 (4)选项A,C中含有碳碳双键,所以能发生聚合、氧化、还原反应。选项B,符合条件的同分异构体有如下两种:CH3-CH=CH(CH3)-COOH、(CH3)2C=CH-COOH。选项B,CH3CH2CH2OH和CH3COOH相对分子质量为60。选项D,CH3COOCH3是具有芳香气味的酯,且易溶于乙醇中。
(4)选项A,C中含有碳碳双键,所以能发生聚合、氧化、还原反应。选项B,符合条件的同分异构体有如下两种:CH3-CH=CH(CH3)-COOH、(CH3)2C=CH-COOH。选项B,CH3CH2CH2OH和CH3COOH相对分子质量为60。选项D,CH3COOCH3是具有芳香气味的酯,且易溶于乙醇中。
 (5)H为沸点很高的CH3COONa,CH3OH沸点较低,故可采用蒸馏方法分离。
(5)H为沸点很高的CH3COONa,CH3OH沸点较低,故可采用蒸馏方法分离。
 (6)DAP苯环上只有两个取代基,且取代基不处于对位,只有两个相同的取代基处于邻位时,其苯环上的一溴代物有两种。D为CH2=CHCH2OH,CH2=CHCH2OH与C10H10O4发生酯交换反应生成CH3OH和DAP单体,推知F为
(6)DAP苯环上只有两个取代基,且取代基不处于对位,只有两个相同的取代基处于邻位时,其苯环上的一溴代物有两种。D为CH2=CHCH2OH,CH2=CHCH2OH与C10H10O4发生酯交换反应生成CH3OH和DAP单体,推知F为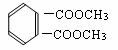 ,生成DAP单体的化学方程式为:2CH2=CHCH2OH +
,生成DAP单体的化学方程式为:2CH2=CHCH2OH + 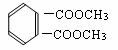
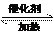
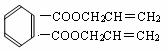 + 2CH3OH。
+ 2CH3OH。
12.
 由短周期元素组成的中学常见无机物A、B、C、D、E、X
由短周期元素组成的中学常见无机物A、B、C、D、E、X
 存在如在右图转化关系(部分生成物和反应条件略去)
存在如在右图转化关系(部分生成物和反应条件略去)
 下列推断不正确的是
下列推断不正确的是
 A.若X是
A.若X是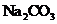 ,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应
,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应
 B.若A是单质,B和D的反应是
B.若A是单质,B和D的反应是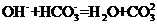 ,则E一定能还原
,则E一定能还原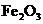

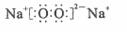 C.若D为CO,C能和E反应,则A一定为
C.若D为CO,C能和E反应,则A一定为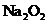 ,其电子式是
,其电子式是
 D.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
D.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
 答案. A
答案. A
 [解析]本题考查元素及其化合物的转化关系。选项A,X是Na2CO3,C为CO2,当A为NO2,B为HNO3,D为NaHCO3也不合转化关系。选项B,根据B、D反应的离子方程式OH― + HCO3―=H2O + CO32―,A为活泼金属Na(或K等),B为NaOH、E为H2,X为CO2,C为Na2CO3,D为NaHCO3,H2在加热时能还原Fe2O3。选项C,A为Na2O2,B为O2,E为NaOH,X为C,C为CO2,D为CO,符合转化关系,正确。选项D,D为摩尔质量为78g/mol的Al(OH)3,A为摩尔质量为78g/mol 的Na2O2,X为铝盐,C为偏铝酸盐,铝盐和偏铝酸盐在溶液中发生双水解反应生成Al(OH)3,符合转化关系,正确。
[解析]本题考查元素及其化合物的转化关系。选项A,X是Na2CO3,C为CO2,当A为NO2,B为HNO3,D为NaHCO3也不合转化关系。选项B,根据B、D反应的离子方程式OH― + HCO3―=H2O + CO32―,A为活泼金属Na(或K等),B为NaOH、E为H2,X为CO2,C为Na2CO3,D为NaHCO3,H2在加热时能还原Fe2O3。选项C,A为Na2O2,B为O2,E为NaOH,X为C,C为CO2,D为CO,符合转化关系,正确。选项D,D为摩尔质量为78g/mol的Al(OH)3,A为摩尔质量为78g/mol 的Na2O2,X为铝盐,C为偏铝酸盐,铝盐和偏铝酸盐在溶液中发生双水解反应生成Al(OH)3,符合转化关系,正确。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com