
29.答案:AD
解析:由弱电解质的概念知弱电解质溶于水只能部分电离。其中A中甲酸溶液若完全电离c(H+)=1 mol·L-1,pH=0;而现在pH=2,说明只部分电离;D中在相同条件弱电解质部分电离,溶液中离子少,导电性弱于强电解质,故选AD。而B表示溶解性与电解质强弱无关;C中完全反应与强弱无关。
28.答案:B
解析:该平衡为溶解平衡。若使Ca(OH)2减少,只须使平衡正向移动。选项中Na2S、NaOH溶液显碱性,使平衡逆移;CaCl2溶液完全电离出Ca2+也使平衡逆移。而B项为AlCl3溶液与OH-作用生成难溶Al(OH)3,消耗OH-使平衡正向移动而使Ca(OH)2固体不断电离而减少。
27.答案:AC
解析:HCl溶于水完全电离,而CH3COOH溶于水存在电离平衡:CH3COOH CH3COO-+H+,加水该平衡向右移动,H+物质的量增大,需加更多的水才能与盐酸c(H+)相同;加CH3COONa时,c(CH3COO-)增大,上述平衡向左移动。c(H+)降低,pH变大,而盐酸加NaCl后pH基本不变。故A、C符合题意。B只能说明盐酸和醋酸具有挥发性,D只说明c(H+)相同,速率相同,与醋酸是否完全电离均无关,故B、D不符合题意。
CH3COO-+H+,加水该平衡向右移动,H+物质的量增大,需加更多的水才能与盐酸c(H+)相同;加CH3COONa时,c(CH3COO-)增大,上述平衡向左移动。c(H+)降低,pH变大,而盐酸加NaCl后pH基本不变。故A、C符合题意。B只能说明盐酸和醋酸具有挥发性,D只说明c(H+)相同,速率相同,与醋酸是否完全电离均无关,故B、D不符合题意。
26.答案:D
解析:A、C均呈中性;B项氨水有剩余,显碱性;D项醋酸有剩余,显酸性。
25.答案:B
解析:强酸中c(H+)=10-a
mol·L-1,强碱中c(OH-)=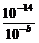 =10-14+b mol·L-1=
=10-14+b mol·L-1=
10-14+12-a mol·L-1=10-2-a mol·L-1,混合后pH=7,即n(H+)=n(OH-),故V(碱)=102V(酸)
24.答案:B
解析:该溶液中离子有SO 、Al3+、H+、K+,已知前三者的浓度,由溶液中阴离子带的负电荷数一定等于阳离子带的正电荷数即可求出K+的浓度。
、Al3+、H+、K+,已知前三者的浓度,由溶液中阴离子带的负电荷数一定等于阳离子带的正电荷数即可求出K+的浓度。
23.答案:D
解析:本题既可采用常规计算法,也可采用估算法:由题知当碱与酸体积比为1∶10时,所得混合液的pH=7,现pH=11,显碱性,故碱酸体积比应大于1∶10,即选D。
22.答案:D
解析:本题关键在加着重号的几个字,溶液所含离子、分子总数应包括水分子,由各溶液的浓度可知,水分子的数目比其他离子和分子的数目要多得多,故溶液体积越大,水分子数目越多,离子和分子总数也就越多。
21.答案:B
解析:温度不变时,c(H+)和c(OH-)的乘积为常数,故排除C;稀释时电离程度增大,OH-的物质的量增大,故排除D;稀释时,NH3·H2O的物质的量减小,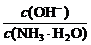 =
= ,可知该分数值增加,故排除A选B。
,可知该分数值增加,故排除A选B。
20.答案:A
解析:无论在什么条件下,纯水中c(H+)=c(OH-)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com