
3、(四川省绵阳中学2009届高三二诊模拟试题 学)在一定温度、一定体积的密闭容器中有如下平衡:H2(g)+I2(g)
学)在一定温度、一定体积的密闭容器中有如下平衡:H2(g)+I2(g)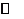 2HI(g),已知H2和I2的起始浓度均为amol/L,达平衡时HI的浓度为bmol/l;若H2和I2的起始浓度均为2amol/L,则平衡时H2的物质的量浓度是( C )
2HI(g),已知H2和I2的起始浓度均为amol/L,达平衡时HI的浓度为bmol/l;若H2和I2的起始浓度均为2amol/L,则平衡时H2的物质的量浓度是( C )
A.bmol/L B.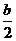 mol/L C.(2a-b)mol/L D.(a-
mol/L C.(2a-b)mol/L D.(a-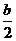 )mol/L
)mol/L
2.[双流县2009届高中毕业班理科综合能力测试]在一定条件下,将3 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g),反应达到平衡时压强为原来的0.9倍。下列判断错误的是[D]
xC(g)+2D(g),反应达到平衡时压强为原来的0.9倍。下列判断错误的是[D]
A.x=1
B.若混合气体的平均相对分子质量不变,则表明该反应达到平衡状态
C.若维持温度不变,在容积为2 L的体积可变的密闭容器中充入3 mol A和1 mol B两种气体,平衡时B的转化率大于40%
D.在相同条件下,若起始加入1.2 mol A、0.4 mol B、0.6 mol C和1.2 mol D达到平衡时,n(D)>1.2 mol
1、[四川梓潼一中高2009级高考模拟理科综合考试(A-1)]一定条件下,体积为10L的密闭容器中,1mol X和1mol Y进行反应:2X(g)+Y(g)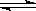 Z(g),经60s达到平衡,生成0.3mol Z。下列说法正确的是(
D )
Z(g),经60s达到平衡,生成0.3mol Z。下列说法正确的是(
D )
A.以X浓度变化表示的反应速率为0.01mol/(L·S)
B.将容器体积变为20L,Z的平衡浓度变为原来的1/2
C.若增大压强,则物质Y的转化率减小
D.若升高温度,X的体积分数增大,则该反应的△H<0
22.[河北冀州中学08-2009学年度高 三上学期期末考试]下列说法正确的是( D )
①硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
③活性炭、SO2和HClO都具有漂白作用,且漂白的化学原理相同
④硫酸厂厂址的选择应靠近原料产地
⑤碳酸氢根离子的电离方程式: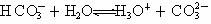
⑥从上到下,卤族元素的非金属性逐渐减弱,故氢卤酸的酸性依次减弱
⑦因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S
⑧NaCl晶体中每个Na+同时吸引着6个Cl-,CsCl晶体中每个Cl-同时吸引着
6个Cs+[B]
A.①②④⑦ B.②⑤ C.②③④⑧ D.①⑤⑥
21. [河北冀州中学08-2009学年度高
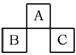
三上学期期末考试]下图是元素周期表中短周期的一部分,B原子与C原子核外电子数之和是A的4倍,则下列推断正确的是[C]
[河北冀州中学08-2009学年度高
三上学期期末考试]下图是元素周期表中短周期的一部分,B原子与C原子核外电子数之和是A的4倍,则下列推断正确的是[C]
A.A、B、C三者均为非金属元素
B.A、B、C三者可以共同形成一种离子化合物
C.A、B、C三者核电核数之和为32
D.B的氢化物比C的氢化物稳定
19.[河南运城市2008-2009学年高三第一学期期末调研测试](10分)A、B、C 、D、E是原子序数依次增大的五种短周期元素:A原子的电子层数与它的核外层电子数相同。A与C、B与D分别为同主族,B和C的最外层电子数之和与E的最外层电子数相向。A与E形成的化合物化学式为AE,其分子中含18个电子。请回答下列问题:
(1)A和B两元素也可以形成与AE等电子数的化合物M,则M的结构式为___________
(2)由C和E所形成的化合物属于___________晶体(填晶体女型)。
(3)由A、B、C、D四种元素所形成的两种化合物相互之间反应的离子方程式为_________
________________________
(4)B、C、E三种元素形成一种盐,此盐中三种原子个数比为l:1:1,将该盐溶液在空气中露置一段时间后(充分光照,不考虑水分的挥发),溶液的PH近似为7,则该过程的总反应方程式为__________________________________________
答案..(10分)(1)H-O一O一H(2分)(2)离子(2分)
(3) 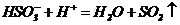 (3分)(4)
(3分)(4) 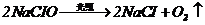 (3分)
(3分)
20[西南师大附中高2009级第五次月考]几种短周期元素的原子半径和主要化合价见下表:[A]
|
元素代号 |
X |
Y |
Z |
L |
M |
Q |
|
原子半径/nm |
0.160 |
0.143 |
0.102 |
0.099 |
0.077 |
0.074 |
|
主要化合价 |
+ 2 |
+ 3 |
+ 6、– 2 |
+ 7、– 1 |
+ 4、– 4 |
– 2 |
下列说法正确的是
A.在化学反应中,M原子既不容易失去电子,又不容易得到电子
B.等物质的量的X、Y的单质与足量盐酸反应,生成H2一样多
C.Y与Q形成的化合物不可能跟氢氧化钠溶液反应
D.Z的氢化物的稳定性强于L的氢化物的稳定性
18.[重庆市主城区(五区)2009届普通高中高三联合考试](12分)现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大。室温下E元素的单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜;D元素原子核外M电子层与K电子层上的电子数相等;A可分别与B、F形成A2B,A2B2、AF等共价化合物;C可分别与B、F形成C2B、C2B2、CF等离子化合物。
请回答下列问题:
(1)以上六种元素中,金属性最强的是(填元素符号) ,F原子的结构示意图为 。
(2)以上元素形成的简单离子中,核外电子数相等的是(填真实的离子符号) 。
(3)C2B2的电子式为 ,该物质中存在的化学键有 。
(4)A2B与C2B2反应的化学方程式是 。
答案.)(1)Na (1分) 氯原子的结构示意图略 (1分)
(2)O2-、Na+、Mg2+、Al3+ (4分)
(3)过氧化钠的电子式略 (2分) 离子键、非极性键 (2分)
(4)2H2O + 2Na2O2 = 4NaOH + O2↑ (2分)
16.[重庆市主城区(五区)2009届普通高中高三联合考试]已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是[C]
A.原子半径A>B>D>C B.原子序数d>c>b>a
C.离子半径C>D>B>A D.单质的还原性A>B>D>C
17[重庆市主城区(五区)2009届普通高中高三联合考试].右表为元素周期表前四周期的一部分,下列有关X、W、Y、R、Z五种元素的叙述中,正确的是[A]
|
|
|
||
|
X |
|
|
|
|
W |
Y |
|
R |
|
|
|
Z |
|
A.常温常压下,五种元素的单质中有两种是气态
B.Y、Z的阴离子电子层结构都与R原子的相同
C.W的氢化物比X的氢化物稳定
D.Y元素最高价氧化物对应水化物的酸性比W元素的弱
15.[西安中学2009届高三第三次年级统考](9分)现有X、Y、Z、A、B、C、D几种元素:
①X、Y、Z是原子核外有3层电子的金属元素,原子半径X<Y<Z。
②A、B是非金属元素,它们可与氢化合形成气态氢化物H2A和HB。室温时,A的单质为淡黄色固体,B的单质为液态。
③C是元素周期表中氧化性最强的元素。
④D的单质是常温下呈液态的金属。利用上述已知条件请回答下列问题:
(1)Y在周期表中的位置是 ;H2A的名称为 ;
(2)B 单质的颜色为 。
(3)用电子式表示化合物YB2的形成过程 。
(4)C单质与水反应的化学方程式为 。
(5)D单质的蒸气扩散到空气中会对人体产生危害,通常在洒落的D单质上覆盖硫磺进行处理,写出反应的化学方程式 。
答案..(9分)(1)第三周期第IIA族 硫化氢(2)深红棕色
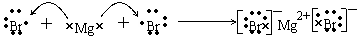
(3)
(4)2F2+2H2O=4HF+O2 (5)Hg+S=HgS
14.[西安中学2009届高三第三次年级统考]现有X、Y两种第ⅤA族元素,下列事实不能说明X的非金属性比Y强的是[C]
A.两种元素所形成的酸的酸性:H3XO4>H3YO4
B.两种元素所形成的气态氢化物的稳定性:XH3>YH3
C.两种元素所形成的最高价氧化物的稳定性:X2O5>Y2O5
D.两种元素所形成的气态氢化物的还原性:YH3>XH3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com