
2.[四川省乐山市2009届高三上学期第一次调研考试]下列离子方程式的书写中,不正确的是[B]
 A.将氯气通入 NaOH溶液中:Cl2+2OH- = Cl-+ClO-+H2O
A.将氯气通入 NaOH溶液中:Cl2+2OH- = Cl-+ClO-+H2O
 B.向氯化铝溶液中加入足量的氨水:
B.向氯化铝溶液中加入足量的氨水:
 Al3++4NH3·H2O=AlO2-+2H2O+4NH4+
Al3++4NH3·H2O=AlO2-+2H2O+4NH4+
 C.向溴化亚铁溶液中通入足量的氯气:
C.向溴化亚铁溶液中通入足量的氯气:
 2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
 D.向足量Ca(HCO3)2溶液中加入少量Ca(OH)2溶液:
D.向足量Ca(HCO3)2溶液中加入少量Ca(OH)2溶液:
 Ca2++HCO3-+OH-=CaCO3↓+H2O
Ca2++HCO3-+OH-=CaCO3↓+H2O
1.[四川梓潼一中高2009级高考模拟理科综合考试(A-1)]下列各组离子一定能大量共存的是( B )
A.在含大量Fe3+的溶液中: 、
、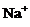 、
、 、
、
B.在强碱性溶液中: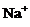 、
、 、
、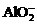 、
、
C.在pH=1的溶液中: 、
、 、
、 、
、
D.在无色透明溶液中: 、
、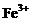 、
、 、
、
6.[河南运城市2008-2009学年高三第一学期期末调研测试]下列有关反应热的叙述正确的是 ( B )
A.已知 ,
,
则氢气的燃烧热为241。8Kj/mol
B.C(s,石墨)=C(s,金刚石);△H=1.9kJ﹒mol-1说明石墨比金刚石稳定
C.X(g)+Y(g)  Z(g)十W(s);△H>0恒温恒容条件下达到平衡后加入X,
Z(g)十W(s);△H>0恒温恒容条件下达到平衡后加入X,
上述反应的△H增大
D.已知 ,则△H1>△H2
,则△H1>△H2
7[河南运城市2008-2009学年高三第一学期期末调研测试] (15分) 把氯气通入稀氨水中,NH3分子上的一个H被Cl取代生成氯氨,然后加入过量的氨和氯氨作用,得到联氨(N2H4)。写出上述反应的化学方程式:
__________________________________________________________________________________________________________________________________________________________
(1) 联氨是一种可燃性液体,可用作火箭燃料。已知32.0g N2H4和H2O2反应生成氮气和水(气态),放出热量642kJ,该反应的热化学方程式是:
__________________________________________________________________________
(2) 联氨的水溶液显弱碱性,用离子方程式表示其显弱碱性的原因:
__________________________________________________________________________
(3) 联氨-空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液。联氨-空气燃料电池放电生成N2和H2O,其电极反应式是:
正极_____________________________________________________________________
负极_____________________________________________________________________
5.[广东梅州五华县横陂中学2009届高考模拟测试.2月]14.已知在25℃ 、1.01kPa下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨) + O2 (g) → CO2(g) + 393.51kJ/mol
C(金刚石)+ O2 (g) → CO2(g) + 395.41kJ/mol
据此判断,下列说法中正确的是 (A )
A.由石墨制备金刚石是吸热反应;石墨的能量比金刚石的低
B.由石墨制备金刚石是吸热反应;石墨的能量比金刚石的高
C.由石墨制备金刚石是放热反应;石墨的能量比金刚石的低
D.由石墨制备金刚石是放热反应;石墨的能量比金刚石的高
4、 (四川省绵阳中学2009届高三二诊模拟试题
(四川省绵阳中学2009届高三二诊模拟试题 学)(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),
学)(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),
|

(2)右图是一个电化学过程示意图。
①锌片上发生的电极反应是________________________。
②假设使用肼一空气燃烧电池作为本过程中的电源,铜片的质量
变化是128g,则肼一空气燃料电池理论上消耗标准状况下的空气_____L
(假设空气中氧气体积含量为20%)
 (3)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式是_____________________________________。
(3)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式是_____________________________________。
(4)1998年希腊亚里斯多德大学的Marnellos和Stoukides采用高质子导电性的SCY陶瓷(能传递H+),实现了高温常压下高转化率的电化学合成氨,其实验装置如图,阴极的电极反应式为______________。
答案:(1)N2H4+O2=N2+2H2O △H=-624KJ/mol;
(2)Cu2++2e-=Cu 112L(3)ClO-+2NH3=N2H4+Cl-+H2O (4)N2+6e-+6H+=2NH3
3.[双流县2009届高中毕业班理科综合能力测试]甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)===CO2(g)+3H2(g);△H=+49.0 kJ·mol
②CH3OH(g)+ O2(g)===CO2(g)+2H2(g);△H=-192.9 kJ·mol
O2(g)===CO2(g)+2H2(g);△H=-192.9 kJ·mol
下列说法正确的是[C]
A.CH3OH转变成H2的过程一定要吸收能量
B.CH3OH的燃烧热为192.9 kJ·mol
C.在相同条件下,1 mol CH3OH蒸气与1 mol水蒸气的能量总和小于1 mol CO2与3 mol H2的能量总和
D.根据②推知反应CH3OH(l)+ O2(g)===CO2(g)+2H2(g)的△H<-192.9 kJ·mol
O2(g)===CO2(g)+2H2(g)的△H<-192.9 kJ·mol
2.[四川省乐山市2009届高三上学期第一次调研考试]下列叙述都与反应热有关,其中不正确的是[C]
A.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则稀H2SO4和Ba(OH)2发生中和反应的热化学方程式为
1/2H2SO4(aq)+1/2Ba(OH)2(aq)=1/2BaSO4(aq)+H2O(l);△H=-57.3kJ/mol
B.CO(g)的燃烧热是283.0kJ/mol,则表示CO燃烧的热化学方程为
CO (g)+1/2O2(g)===CO2 (g);△H=-283.0kJ/mol
C.对于反应2NO2(g) N2O4(g);△H<0,升高温度,正逆反应的速率都增大,但正反应的增速大于逆反应增速
N2O4(g);△H<0,升高温度,正逆反应的速率都增大,但正反应的增速大于逆反应增速
D.实验测得C(s)与O2(g)反应生成CO2及CO与O2反应生成CO2的反应热分别是-393.5kJ·mol-1 与-283.0kJ·mol-1,则C(s)与O2(g)反应生成CO(g)的反应热为△H=-110.5kJ/mol
1.[四川梓潼一中高2009级高考模拟理科综合考试(A-1)]有3个热化学方程式:H2(g)+1/2O2(g)=H2O(g);△H =a kJ/mol
H2(g)+1/2O2(g)=H2O(l);△H =bkJ/mol
2H2(g)+O2(g)=2H2O(l);△H =ckJ/mol
关于它们的下列表述正确的是( D )
A.a+b=c B.1mol H2O由气态变为液态吸收(a-b)kJ热量
C.氢气的燃烧热为c/2 kJ D.1molH2 O由液态变为气态吸收 (a -c/2) kJ热量
10.[广西南宁武鸣高中09届高中化学2月调研试卷](10分)有机物X(分子式为C4H6O5)广泛存在于许多水果中,尤以苹果、葡萄、西瓜、山楂内为多。经测定该有机物具有下列性质(见下表),请根据题目要求填空:
|
|
X的性质 |
推测X结构中有关官能团的结论 |
|
① |
X与足量的金属钠反应产生氢气。 |
|
|
② |
X与醇或羧酸在浓硫酸加热条件下均能生成有香味的产物。 |
|
|
③ |
在一定条件下X的分子脱水产物(不是环状化合物)可与溴水发生加成反应。 |
|
|
④ |
33.5g X与100mL的5mol·L-1氢氧化钠溶液恰好完全中和。 |
|
|
X的可能 结构简式 |
I ; Ⅱ ;Ⅲ |
答案②有机物X中存在有羧基(1分)和醇羟基(或羟基)(1分)
④有机物X中存在有2个羧基(2分)
X的可能结构简式:
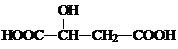
 I. Ⅱ.
I. Ⅱ.

Ⅲ.
(每个2分,共6分)
9、[2009学年丽水高中新课程水平测试高三化学试题](12分)阿斯匹林是常用的解热镇痛药,其有效成分是乙酰水杨酸,结构如下图。欲测定阿斯匹林中乙酰水杨酸的含量,取1片药研碎,加入过量的0.01mol/L氢氧化钠溶液20.00mL使之充分水解;再用0.01mol/L盐酸滴定过量的氢氧化钠,消耗盐酸17.00mL。过程如下:

请回答下列问题:
(1)乙酰水杨酸分子中呈酸性的官能团的名称是 。
(2)乙酰水杨酸的分子式是 。
(3)写出乙酰水杨酸与乙醇反应的化学方程式 。
(4)滴定到终点时,指示剂颜色的变化是___________________________,滴定过程中除了用到滴定管外,主要玻璃仪器还有 。
(5)乙酰水杨酸与NaOH反应的方程式如下。则每片阿斯匹林含有效成分是 mg。
答案、(1)羧基 (2)C9H8O4
 (4)由红色变为无色 锥形瓶
(4)由红色变为无色 锥形瓶
(5) 1.8
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com