
2.ЕШПЩФмЪТМўЕФИХТЪ(ЙХЕфИХТЪ)ЃК P(A)=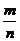 ЁЃРэНтетРяmЁЂnЕФвтвхЁЃШч(1)НЋЪ§зж1ЁЂ2ЁЂ3ЁЂ4ЬюШыБрКХЮЊ1ЁЂ2ЁЂ3ЁЂ4ЕФЫФИіЗНИёжаЃЌУПИёЬювЛИіЪ§зжЃЌдђУПИіЗНИёЕФБъКХгыЫљЬюЪ§зжОљВЛЯрЭЌЕФИХТЪЪЧ______(Д№ЃК
ЁЃРэНтетРяmЁЂnЕФвтвхЁЃШч(1)НЋЪ§зж1ЁЂ2ЁЂ3ЁЂ4ЬюШыБрКХЮЊ1ЁЂ2ЁЂ3ЁЂ4ЕФЫФИіЗНИёжаЃЌУПИёЬювЛИіЪ§зжЃЌдђУПИіЗНИёЕФБъКХгыЫљЬюЪ§зжОљВЛЯрЭЌЕФИХТЪЪЧ______(Д№ЃК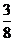 )ЃЛ(2)Щш10МўВњЦЗжага4МўДЮЦЗЃЌ6Мўе§ЦЗЃЌЧѓЯТСаЪТМўЕФИХТЪЃКЂйДгжаШЮШЁ2МўЖМЪЧДЮЦЗЃЛЂкДгжаШЮШЁ5МўЧЁга2МўДЮЦЗЃЛЂлДгжагаЗХЛиЕиШЮШЁ3МўжСЩйга2МўДЮЦЗЃЛЂмДгжавРДЮШЁ5МўЧЁга2МўДЮЦЗЁЃ(Д№ЃКЂй
)ЃЛ(2)Щш10МўВњЦЗжага4МўДЮЦЗЃЌ6Мўе§ЦЗЃЌЧѓЯТСаЪТМўЕФИХТЪЃКЂйДгжаШЮШЁ2МўЖМЪЧДЮЦЗЃЛЂкДгжаШЮШЁ5МўЧЁга2МўДЮЦЗЃЛЂлДгжагаЗХЛиЕиШЮШЁ3МўжСЩйга2МўДЮЦЗЃЛЂмДгжавРДЮШЁ5МўЧЁга2МўДЮЦЗЁЃ(Д№ЃКЂй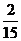 ЃЛЂк
ЃЛЂк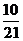 ЃЛЂл
ЃЛЂл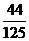 ЃЛЂм
ЃЛЂм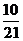 )ЁЁ
)ЁЁ 
1ЃЎЫцЛњЪТМў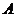 ЕФИХТЪ
ЕФИХТЪ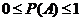 ЃЌЦфжаЕБ
ЃЌЦфжаЕБ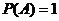 ЪБГЦЮЊБиШЛЪТМўЃЛЕБ
ЪБГЦЮЊБиШЛЪТМўЃЛЕБ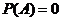 ЪБГЦЮЊВЛПЩФмЪТМўP(A)=0ЃЛ
ЪБГЦЮЊВЛПЩФмЪТМўP(A)=0ЃЛ 
6ЃЎНЋVLNOКЭNO2ЕФЛьКЯЦјЬхЭЈЙ§ЫЎЮќЪеКѓЃЌЕУЕНamLЮоЩЋЦјЬхAЁЃНЋДЫЮоЩЋЦјЬхAгыЕШЬхЛ§O2ЛьКЯЃЌдйЭЈЙ§ЫЎГфЗжЮќЪеКѓЃЌЪеМЏЕН5mLЮоЩЋЦјЬхBЁЃЪдЛиД№ЃК
(1)AЦјЬхЪЧ__________________ЃЌBЦјЬхЪЧ_________________________ЁЃ
(2)AЦјЬхЕФЬхЛ§ЪЧ______________________mL
(3)VжЕЕФШЁжЕЗЖЮЇЪЧ____________________ЁЃ
Д№АИЃК(1)AЪЧNOЃЛBЪЧO2ЁЃ(2)20mLЁЃ(3)20<V<60ЁЃ
5ЃЎЯТСаЙигкЩщ(As)дЊЫиЕФа№ЪіжаЃЌе§ШЗЕФЪЧ(ЁЁ )ЁЃ
(A)дкAsCl3ЗжзгжаЃЌЩщдзгзюЭтВуЕчзгЪ§ЮЊ8
(B)ЩщЕФЯрЖддзгжЪСПЮЊ74.92ЃЌгЩДЫПЩжЊЩщдзгКЫФкга42Иіжазг
(C)ЩщЕФЧтЛЏЮяЕФЛЏбЇЪНЮЊAsH3ЃЌЫќЪЧвЛжжЧПбѕЛЏМС
(D)ЩщЫс(H3AsO4)ЪЧЧПЫсЃЌЦфЫсадгыСђЫсЯрЫЦЁЁ
Д№АИЃКAЁЃ
4ЃЎдквЛЖЈЮТЖШКЭбЙЧПЯТЃЌНЋзАгаN2КЭNO2ЛьКЯЦјЬхЕФЪдЙмЕЙСЂгкЫЎВлжаЃЌзюКѓЪдЙмФкЦјЬхЕФЬхЛ§ЫѕаЁЮЊдЬхЛ§ЕФ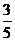 ЃЌдђЛьКЯЦјЬхжаN2гыNO2ЕФЬхЛ§БШЪЧ(ЁЁ )ЁЃ
ЃЌдђЛьКЯЦјЬхжаN2гыNO2ЕФЬхЛ§БШЪЧ(ЁЁ )ЁЃ
(A)2:3ЁЁЁЁЁЁ (B)3:2ЁЁЁЁЁЁ (C)3:5ЁЁЁЁЁЁ (D)5:3
Д№АИЃКAЁЃ
3ЃЎдкГЧЪаПеЦјжаКЌгаХЈЖШНЯДѓЕФвЛбѕЛЏЬМЁЂЕЊЕФбѕЛЏЮяЕШДѓЦјЮлШОЮяЃЌетаЉЮлШОЮяЕФжївЊРДдДЪЧ(ЁЁЁЁ )ЁЃ
(A)СђЫсЙЄвЕХХЗХЕФЗЯЦјЁЁЁЁЁЁ (B)АБбѕЛЏЗЈжЦЯѕЫсжаЮќЪеЫўХХЗХЕФЗЯЦј
(C)ЦћГЕЮВЦјЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (D)УКЬПВЛЭъШЋШМЩеВњЩњЕФЗЯЦј
Д№АИЃКCЁЃ
2ЃЎЙигкСзЕФЯТСаа№ЪіжаЃЌе§ШЗЕФЪЧ(ЁЁ )
(A)КьСзУЛгаЖОадЖјАзСзгаОчЖОЁЁЁЁЁЁ (B)АзСздкПеЦјжаМгШШЕН260ЁцПЩзЊБфЮЊКьСз
(C)АзСзПЩгУгкжЦдьАВШЋЛ№ВёЁЁЁЁЁЁЁЁ (D)ЩйСПАзСзгІБЃДцдкЫЎжа
Д№АИЃКADЁЃ
3ЃЎвЛбѕЛЏЕЊЁЂбѕЦјЭЌЪБИњЫЎЗДгІЃК4NO+3O2+H2O = 4HNO3
гіЕНетРрМЦЫуЬтЪБЃЌЪзЯШвЊХЊЧхЫљЩцМАЕФЗДгІдРэЪЧФФжжЧщПіЃЌдйНјааМЦЫуЁЃШчЃЌЖўбѕЛЏЕЊИњбѕЦјЕФЛьКЯЦјЬхШмгкЫЎЪБЃЌПЩФмгавдЯТЯђжжЧщПіЃК
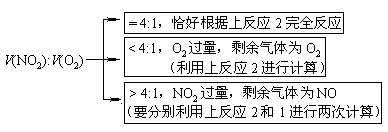
[Р§ЬтНВНт]
[Р§1]НЋЪЂгаЕЊЦјКЭЖўбѕЛЏЕЊЛьКЯЦјЬхЕФЪдЙмЕЙСЂгкЫЎжаЃЌОЙ§зуЙЛЪБМфКѓЃЌЪдЙмФкЦјЬхЬхЛ§ЫѕаЁЮЊдЬхЛ§ЕФвЛАыЃЌдђдЛьКЯЦјЬхжаЕЊЦјКЭЖўбѕЛЏЕЊЕФЬхЛ§БШЪЧЁЁЁЁЁЃ
[ЗжЮі]ЕЊЦјИњЫЎВЛЗДгІЃЌЫљвдПЩИљОнЁА3NO2+H2O=2HNO3+NOЁБгУЬхЛ§ВюЗЈНјааМЦЫуЁЃ
Д№АИЮЊЃК1:3ЁЃ
[Р§2]
НЋШнЛ§ЮЊ50mLЕФСПЭВФкГфТњNO2КЭO2ЕФЛьКЯЦјЬхЃЌЕЙжУСПЭВдкЪЂТњЫЎЕФЫЎВлРяЃЌзуЙЛЪБМфКѓЃЌСПЭВРяЪЃгрЦјЬхЬхЛ§ЮЊ5mLЁЃдђЛьКЯЦјЬхжаNO2КЭO2ЬхЛ§БШПЩФмЪЧЁЁЁЁЁЃ
[ЗжЮі]ЖўбѕЛЏЕЊЁЂбѕЦјЛьКЯЦјЬхР§жУгкЫЎжаЃЌзюКѓВаСєЦјЬхПЩФмгаЖўжжЧщПіЃЌвЛЪЧбѕЦјЃЌЖўЪЧвЛбѕЛЏЕЊЁЃЫљвдгІЯШМйЩшЃЌдйСЂЪНМЦЫуЁЃ
[НтД№](1)ШєЪЃгрЕФ5mLЦјЬхЪЧO2ЃЌдђЙВга45mLNO2ЁЂO2ЛьКЯЦјЬхИњЫЎЗДгІЃЌИљОн4NO2+O2+H2O = 4HNO3ПЩЕУГіЃК
V(NO2)=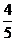 ЁС45mL=36mL
ЁС45mL=36mL
V(O2)=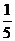 ЁС45mL+5mL=14mL
ЁС45mL+5mL=14mL
ЫљвдЃЌдЛьКЯЦјЬхжаNO2КЭO2ЬхЛ§БШЮЊ18:7ЁЃ
(2)ШєЪЃгрЕФ5mLЦјЬхЪЧNOЃЌдђNO2ЁЂO2ЛьКЯЦјЬхИњЫЎЗДгІЪБЪЧNO2Й§СПЃЌЙ§СПЕФNO2дйИњЫЎЗДгІЁЃИљОнЗДгІЁА3NO2+H2O=2HNO3+NOЁБПЩЕУГіЃЌЙВга15mLNO2Й§СПЁЃ
МДЃЌдкNO2ЁЂO2ЛьКЯЦјЬхИњЫЎЗДгІЕФЙ§ГЬжаЙВЯћКФЦјЬх35mLЁЃИљОн4NO2+O2+H2O = 4HNO3ПЩЕУГіЃК
V(O2)=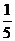 ЁС35mL=7mL
ЁС35mL=7mL
V(NO2)=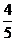 ЁС35mL+15mL= 43mL
ЁС35mL+15mL= 43mL
ЫљвдЃЌдЛьКЯЦјЬхжаNO2КЭO2ЬхЛ§БШЮЊ43:7ЁЃ
2ЃЎЖўбѕЛЏЕЊЁЂбѕЦјЭЌЪБИњЫЎЗДгІЃК4NO2+O2+H2O = 4HNO3
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com