
4、(1)打开止水夹,挤出胶头滴管中的水 氨气极易溶解于水,致使烧瓶内气体压强迅速减小
(2)打开夹子,用手(或热毛巾等)将烧瓶捂热,氨气受热膨胀,赶出玻璃导管
(3)
①先打开a、b活塞,再挤压胶头滴管(或先挤压胶头滴管,再打开a、b活塞)。
②导管口处产生白烟。
③先打开a、c活塞,再挤压胶头滴管(或先打开a活塞,挤压胶头滴管,再打开c活塞)。片刻后,关闭a,然后打开b活塞。
(4)C、D (5)A
3、(1)B C C A 两个C依次是饱和食盐水及浓硫酸
(2)
(3)水浴(附温度计)。将D置于冰水中
1、(1)分液漏斗,将两种互不相溶的液体分开(或组装反应发生装置)
(2)①用D代替长颈漏斗;②将B放入A的广口瓶中,长颈漏斗下端插入B中。
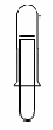
2.
 3.
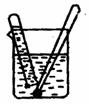
3.
 4
4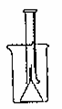
 5.DG 6.
5.DG 6.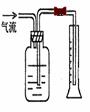


例1、① A 、 B
② Al2(SO4)3 + 6NaHCO3 = 2Al(OH)3↓+ 6CO2↑+ 3Na2SO4
抽滤瓶中放入NaHCO3溶液,试管中放入Al2(SO4)3溶液,并将试管放入抽滤瓶中,塞紧塞子,使用时将抽滤瓶倒转即可。
③ 试管 , 浓氨水和NaOH(S) ,
将圆底烧瓶倒放,向试管中依次放入NaOH(S)和浓氨水,迅速将试管伸入烧瓶瓶底,片刻,用湿润的红色石蕊试纸放于瓶口,试纸变蓝色,说明烧瓶已充满氨气。
④有毒气体不会排放到空气中。
例2、(1)BCD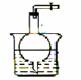
 (2)
(2) 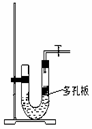


例3、①Ⅱ 3CuO+2NH3 3Cu+N2+3H2O
3Cu+N2+3H2O
②不可以 B起到安全瓶的作用,可防止C中的水倒吸至A中引起试管的破裂
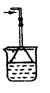

⑵ c→d→e→a→b→f排空。

例4.(1)
(2)由于大量草酸蒸气逸出,与石灰水反应生成草酸钙沉淀 。
在未洗气的情况下通入石灰水,还可能因草酸蒸气与石灰水反应生成了草酸钙沉淀,对实验有干扰,因而在气体通澄清石灰水前可增加一个装有水的洗气装置。
课堂练习
4.
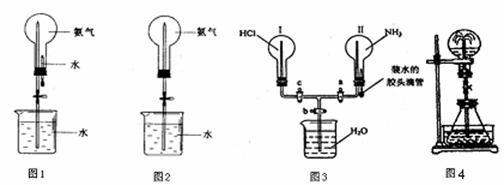
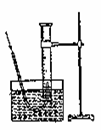
(1)用图1装置进行喷泉实验,上部烧瓶已充满干燥氨气,引发水上喷的操作是 。该实验的原理是 _________________________ 。
(2)如果只提供如图2的装置,请说明引发喷泉的方法。
(3)利用如图3所示的装置,可以验证NH3和HCl的有关性质.实验前a、b、c活塞均关闭.
①若要在烧瓶Ⅱ中产生“喷泉”现象,烧瓶I中不产生“喷泉”现象,其操作方法是____________________________
②若先打开a、c活塞,再挤压胶头滴管,在烧瓶II中可观察到的现象是
__________________________________
③通过挤压胶头滴管和控制活塞的开关,在烧瓶I中产生“喷泉”现象,烧瓶II中不产生“喷泉”现象,其操作方法是______________ _。
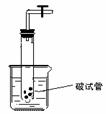
(4)在图4的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是 ,这种方法产生喷泉的原理是 。
A.Cu与稀盐酸 B.NaHCO3与NaOH溶液
C.CaCO3与稀盐酸 D.NH4HCO3与稀盐酸
(5)在图4的锥形瓶外放一水槽,锥形瓶中加入酒精,水槽中加入冷水后,再加入足量的下列物质,结果也产生了喷泉。水槽中加入的物质可以是 。
A.浓硫酸 B.食盐 C.硝酸铵 D.硫酸铜
第2讲常见玻璃仪器的使用(详解)
双基回顾1.①查漏 ②润洗 ③干燥
3.二氯化硫(SCl2)是一种用途极为广泛的化学原料。其熔点-78℃,沸点59℃。密度1.638g/cm3。遇水易分解。
(1)请用图示装置组合由Cl2与S反应(Cl2+S SCl2)合成二氯化硫的实验装置,其顺序为(装置可重复使用),
SCl2)合成二氯化硫的实验装置,其顺序为(装置可重复使用),
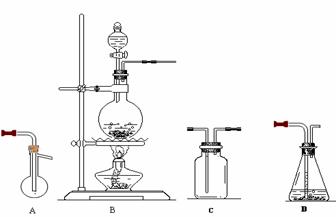
( )→( )→( )→( )→D(D为收集二氯化硫的装置),并指明除A、B、D外,其它装置中盛放的药品
(2)为了得到纯净的二氯化硫及避免环境污染,应在D后增加一个装置,请画出该装置简图并指明所盛放的药品
(3)实验时,A装置需加热至50-59oC,最好采用何种方式 加热 。如何防止D中液体挥发 。
2.实验室可用氯气与金属铁反应制备无水三氯化铁,该化合物是棕红色、易潮解,100℃左右时升华。下图是两个学生设计的实验装置,左边的反应装置相同,而右边的产品收集装置则不同,分别如(Ⅰ)和(Ⅱ)所示。试回答:
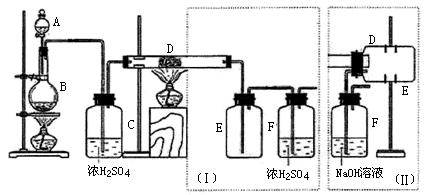
(1)认真比较装置(Ⅰ)和装置(Ⅱ),请指出它们各自的主要缺点。
装置(Ⅰ)缺点: , 。
装置(Ⅱ)缺点: 。
(2)如果选用装置(Ⅱ)来完成实验,则必须采取的改进措施是
1.如右图所示,A可用于实验室制取气体的发生装置。B、C、D为常见仪器。请回答下列问题:
(1)仪器D的名称是_______________。
列举D的一种常见的用途为____________________
(2)制取气体时,常会有生成的气体逸散到空气中,有的还会造成空气污染。例如本题中的A装置(气密性良好)。为了防止上述弊端,请在B、C、D中选择适当的仪器,对A进行重新设计和组装。(以简洁的文字予以说明):
安装方法①__________________________________________________
安装方法②________________________________________________________
2.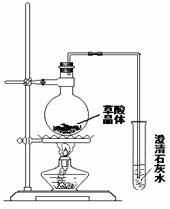 利用右图装置验证草酸分解后有CO2气体产生,结果连续加热一段时间后的现象是:试管里澄清石灰水只变浑浊,其原因是
利用右图装置验证草酸分解后有CO2气体产生,结果连续加热一段时间后的现象是:试管里澄清石灰水只变浑浊,其原因是
请指出装置中存在的问题,并提出实验的改进措施。
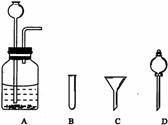
例1.化学仪器的多样性为设计化学实验提供了很多便利,如图1所示的“套管实验”装置,当A管放入Na2CO3,B管放入NaHCO3,a和b管口用导管连接并插入澄清石灰水,对A管底部加热,可用于比较Na2CO3,NaHCO3的热稳定性。
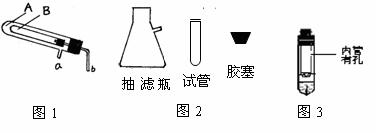
① 利用右图1的“套管装置”,若要比较红磷与白磷的着火点,则红磷应放入
管,白磷应放入 管;
② 现有Al2(SO4)3溶液,NaHCO3溶液以及如上图2所示的仪器,用“套管法”设计一个泡沫灭火器实验装置。该反应的化学方程式为
,
简述该实验设计及演示的操作过程
③ 用圆底烧瓶收集氨气做“喷泉实验”,由于常规收集方法很难使烧瓶充满氨气,若用“套管法”能较好地解决这一问题,除圆底烧瓶外,此法还需另一种玻璃仪器,其名称是 ,所选用的试剂为 (从浓氨水、NH4Cl(S)、NaOH(S)、浓硫酸中选用),简述操作过程及判断烧瓶已充满NH3的方法
。
④欲利用上图3验证铜与浓硝酸的反应产物,该装置除简洁外,还有一个明显的优点是: 。
例2.若实验室只有下列仪器用品,请从中选择合适仪器组装一套能随开随用、随关随停的氢气发生装置。你认为必须选择的仪器是(填下图中的字母序号);
。并画出实验装置图
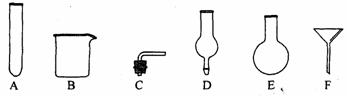
请用U形管,破试管和烧杯分别设计并绘制二套“随开随用、随关随停”的氢气发生装置(其它仪器自选)
例3.某绿色粉末的组成可表示为Cu2(OH)2CO3·xH2O,在加热条件下,该粉末在失去结晶水的同时发生分解反应,化学方程式如下:
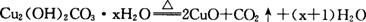
现取一定量该粉末(未精确测定质量)样品,用下图所列仪器(夹持、加热等仪器均略)先后进行两个实验:(I)测定粉末组成中结晶水的x值;
(Ⅱ)用NH3还原前一个实验的残留固体,可回收其中的金属单质,同时还生成一种无污染的气体
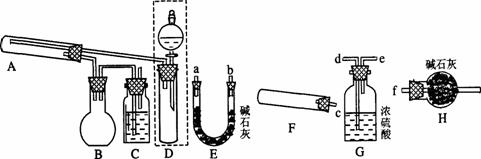
(1)见图中已装配好的一套装置,回答下列问题:
①该装置用于进行实验(选填I或Ⅱ)________,实验时需对A处进行加热,写出A中的反应方程式 _____________________________________________
 ②虚线框内的仪器可用于快速制取少量的氨气,所用药品为浓氨水、NaOH固体;广口瓶C中盛有蒸馏水,其作用是吸收末反应的NH3,避免对室内环境带来不良的影响。有的同学建议为了简化实验装置,可以去掉烧瓶B,直接将A、C相连,这样做可以吗?说一说你对这一建议的看法
②虚线框内的仪器可用于快速制取少量的氨气,所用药品为浓氨水、NaOH固体;广口瓶C中盛有蒸馏水,其作用是吸收末反应的NH3,避免对室内环境带来不良的影响。有的同学建议为了简化实验装置,可以去掉烧瓶B,直接将A、C相连,这样做可以吗?说一说你对这一建议的看法
___________________________、___________________________,
有的同学提出可用一个装置代替B、C两个装置,请你在右边虚线框内画出替代装置的装置;
(2)用图中其它仪器组装成另一套实验装置,用来完成另一个实验,则这些仪器按气流从左到右方向的连接,各接口的连接顺序(填写各接口的小写字
母)___ _→____ _→_____ _→______ →_______ →f;
例4.已知乙二酸(HOOC-COOH)俗称草酸,易溶于水,为二元弱酸,酸性强于碳酸,它所形成的盐草酸钙和草酸氢钙均为白色不溶物。无色晶体H2C2O4·2H2O称为草酸晶体,其熔点为101.5℃。草酸晶体失去结晶水得到无水草酸,它在157℃升华。已知草酸分解的化学方程式为:H2C2O4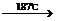 H2O+CO2↑+CO↑
H2O+CO2↑+CO↑
根据上述信息,回答下列问题:
1.如何证明草酸晶体受热时会有水生成?[用简要的实验装置图表示,要体现所使用仪器(加热和夹持仪器不必画出)和试剂]。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com