
94、有一瓶澄清溶液, 可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、SO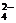 、CO
、CO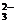 、NO
、NO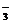 、Cl-、I-现进行如下实验:
、Cl-、I-现进行如下实验:
(1)测该溶液显强酸性;
(2)取样加少量四氯化碳和数滴新制氯水、CCl4层为紫红色;
(3)另取样滴加稀NaOH溶液, 使溶液变为碱性, 此过程无沉淀生成;
(4)取少量上述碱性溶液, 加Na2CO3溶液出现白色沉淀;
(5)将实验(3)中的碱性溶液加热, 有气体放出, 该气体能使湿红色石蕊试纸变蓝。
问:(1)原溶液中肯定存在的离子是 ;
(2)肯定不存在的离子是 ;
(3)不能确定是否存在的离子是 。
答案.(1)
(2)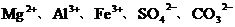
(3)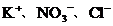
93、有一瓶溶液只含Cl-、CO32-、SO42-、Na+、NH4+、K+、Mg2+ 七种离子中的某几种。经实验:
 ① 原溶液
① 原溶液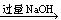 白色沉淀;
白色沉淀;
 ② 将①所得溶液
② 将①所得溶液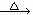 放出使湿润的红色石蕊试纸变蓝的气体;
放出使湿润的红色石蕊试纸变蓝的气体;
 ③ 原溶液中加BaCl2溶液不产生沉淀。
③ 原溶液中加BaCl2溶液不产生沉淀。
 ④ 原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
④ 原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
 回答下列问题:
回答下列问题:
 (1) 试分析原溶液中一定含有的离子是 ,一定不含有的离子是 ,
可能含有的离子是 。
(1) 试分析原溶液中一定含有的离子是 ,一定不含有的离子是 ,
可能含有的离子是 。
 (2) 有同学认为实验④可以省略,你认为呢?(填“可以”或“不可以”)
,
(2) 有同学认为实验④可以省略,你认为呢?(填“可以”或“不可以”)
,
 并说明理由
。
并说明理由
。
答案:
(1)Mg2+、NH4+、Cl-; CO32-、SO42-; Na+ 、 K+
 (2)可以、 溶液显电中性有阳离子存在必有阴离子存在
(2)可以、 溶液显电中性有阳离子存在必有阴离子存在
92、在反应:2MnO4-+5H2S+6H+=2Mn2++5S↓+8H2O中,电子转移的总数为 ,还原剂为 ,还原产物为 ,当反应中有80g S析出时,有 mol MnO4-被 ,同时有 g H2S被 。
答案:
10e-;H2S;Mn2+;1;还原;85;氧化。
91、某河道两旁有甲乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、C1-、OH- 、NO3- 六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子 、
、 ,乙厂的废水中含有另外三种离子。对于该两厂的废水,可采取下列两种方法来处理:
(1)如果在废水中加一定量 (选填:活性炭或铁粉),可以发生 反应,离子方程式是 ,并且能够回收其中的金属 (填写金属元素符号)。
(2)将甲厂和乙厂的废水按适当的比例混合,可以使废水中的某些离子转化为沉淀,写出两个离子方程式: 、
。经过滤后的废水主要含 ,可用来浇灌农田。
答案:
(1)OH-、C1-、K+;铁粉;置换;Fe+2Ag+=2Ag+Fe2+;Ag;
(2)Ag++C1-=AgC1↓、Fe3++3OH-=Fe(OH)3↓; KNO3
90、(1)向Ba(OH)2溶液中,逐滴加入NaHSO4溶液至恰好不再生成沉淀时为止,
写出反应的离子方程式: 。
(2)在以上溶液中,继续滴加NaHSO4溶液,写出反应的离子方程式:
。
答案:
(1)Ba2++OH-+ H++SO42-= BaSO4↓+H2O (2)OH-+ H+= H2O
89、写出下列反应的离子方程式:
(1)石灰石溶于稀硝酸: ;
(2)电解氯化钠的水溶液: ;
(3)氯气通入水中: ;
(4)氯气通入氢氧化钠溶液中: ;
(5)漂白粉投入水中,再通入少量CO2气体: ;
(6)氯气通入澄清石灰水: ;
(7)硫酸和氧化铜: ;
(8)烧碱溶液与小苏打溶液混合 。
答案:
(1)CaCO3+2H+=Ca2++H2O+CO2↑
(2)2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
(3)Cl2+H2O=H++Cl-+HClO
(4)Cl2+2OH-=Cl-+ClO-+H2O
(5)Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO
(6) Cl2+2OH-=Cl-+ClO-+H2O
(7)CuO+2H+=Cu2++H2O
(8)HCO3-+OH-=CO32-+H2O
88.已知A、B、C、D四种溶液分别为NaHCO3、Ca(OH)2、FeCl3、HCl,它们相互之间的反应现象如下表所示,其中“↓”表示有沉淀生成,“↑”表示有气体生成,“-”表示无现象。
|
|
A |
B |
C |
D |
|
A |
|
↑ |
- |
- |
|
B |
↑ |
|
↓ |
↑ ↓ |
|
C |
- |
↓ |
|
↓ |
|
D |
- |
↑ ↓ |
↓ |
|
(1)写出B的化学式 ,D的化学式 。
(2)写出B+C(过量)反应的离子方程式 。
答案:
(1)NaHCO3 、FeCl3
(2)HCO3- + Ca2+ + OH- = CaCO3 ↓+ H2O
87.配平下列化学方程式:
____NH4NO3 = ____HNO3 + ____N2↑ + ____H2O
____Cr2O72- + ____H2C2O4 +_______ = ____Cr3+ + ____CO2 ↑+____H2O
答案:
)5NH4NO3 = 2HNO3 + 4N2 + 9H2O
Cr2O72- + 3H2C2O4 +8H+ = 2Cr3+ + 6CO2 +7H2O
86.一个完整的氧化还原反应方程式可以拆开,写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”。如2Fe3++Cu===2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e-===Cu2+,还原反应式:2Fe3++2e-=== 2Fe2+。据此,回答下列问题:
⑴将反应Zn+2H+ === Zn2++H2↑拆写为两个“半反应式”:
氧化反应式: ,还原反应式: 。
⑵将反应3NO2+H2O == 2H++2NO3-+NO拆写为两个“半反应式”:
氧化反应式: ,还原反应式: 。
⑶已知某反应的两个“半反应式”为:CH4+10 OH--8e-===CO32-+7H2O,O2+2H2O+4e-=== 4OH-,则氧化还原反应方程式为 。
答案:
⑴Zn-2e-=== Zn2+,2 H++2e-=== H2 。
⑵2NO2+2H2O-2e-=== 4H++2 NO3-;NO2+2 H++2e-=== NO+H2O
⑶CH4+2O2+2OH-=== CO32-+3H2O
[点拨:⑵注意电子得失守恒、粒子数目守恒以及物质的选择与系数调整。在反应3NO2+H2O ===2 H++2 NO3-+NO中,只有1个NO2分子作氧化剂,有2个NO2分子作还原剂。2个NO2分子变为2个NO3-离子时,需2个H2O分子提供2个O原子,2个 H2O分子中的4个H原子则变为4个 H+离子。1个NO2分子变成1个NO分子时,另1个O原子需要与2个 H+离子结合成水。所以,有以上“半反应”。⑶前式 + 后式×2即得]
85.甲、乙、丙、丁分别是盐酸、碳酸钠、氯化钙、硝酸银4 种溶液中的一种。将它们两两混合后,观察到的现象是:①甲与乙或丙混合都产生沉淀;②丙与乙或丁混合也产生沉淀;③丁与乙混合产生无色气体。
回答下面问题:
⑴这四种溶液分别是:甲 ,乙 ,丙 ,丁 。
⑵写出下列反应的离子方程式
①丁与乙: 。
②甲与乙: 。
③丙与丁: 。
答案:
⑴甲:氯化钙、乙:碳酸钠 、丙:硝酸银、丁:盐酸 (或写化学式)。
⑵①2H++CO32-===H2O+CO2↑ ②Ca2++CO32-===CaCO3↓
③Ag++Cl-===AgCl↓
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com