
10、(1)K= ; 减小。 (2)
; 减小。 (2) mol·(L·min)-1。 (3)b; c。
mol·(L·min)-1。 (3)b; c。
(4)Cu2O+CO 2Cu+CO2。
2Cu+CO2。
1、BD 2、D 3、B 4、D 5、C 6、D 7、B 8、C、9、A
10、(2007年高考上海)一定条件下,在体积为3 L的密闭容器中,一氧化
碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g)
CH3OH(g)

根据题意完成下列各题:(1)反应达到平衡时,平衡常数表达式K= ,升高温度,K值 (填“增大”、“减小”或“不变”)。
(2)在500 ℃,从反应开始到平衡,氢气的平均反应速率v (H2)= 。
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是 a.氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大
(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:_______________________________________(用化学方程式表示)。
第31讲 化学平衡移动图像
9、下图中,C%表示某反应物在体系中的百分含量,同时符合以下两图象的反应是
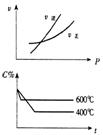
 A、4NH3(g)+5O2(g) 4NO(g)+6H2O(g),
A、4NH3(g)+5O2(g) 4NO(g)+6H2O(g),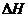 =-808.7KJ/mol
=-808.7KJ/mol
 B、N2O3(g) NO2(g)+NO(g),
B、N2O3(g) NO2(g)+NO(g),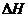 =+41.8KJ/mol
=+41.8KJ/mol
 C、3NO2(g)+H2O(l) 2HNO3(l)+NO(g),
C、3NO2(g)+H2O(l) 2HNO3(l)+NO(g),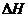 =-261.5KJ/mol
=-261.5KJ/mol
 D、CO2(g)+C(s) 2CO(g),
D、CO2(g)+C(s) 2CO(g),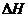 =+171.4KJ/mol
=+171.4KJ/mol
8、 反应2X(g)+Y(g) 2Z(g);△H<0。在不同温度和压强下,产物Z的
反应2X(g)+Y(g) 2Z(g);△H<0。在不同温度和压强下,产物Z的
物质的量(n2)与反应时间(t)的关系如图所示,下列判断正确的是
A、T1<T2,P1<P2 B、T1<T2,P1>P2
C、T1>T2,P1>P2 D、T1>T2,P1<P2
7、 如图(Ⅰ)表示反应:mA(g)+nB(g)
pC(g)+qD(g);△H。在不同温度下经过一定时间混合气体体系中C的百分含量与温度T的关系。图(Ⅱ)表示在一定条件下达到平衡后,t时刻改变影响平衡的另一个条件,重新建立平衡的反应过程。由此可判断该反应中
如图(Ⅰ)表示反应:mA(g)+nB(g)
pC(g)+qD(g);△H。在不同温度下经过一定时间混合气体体系中C的百分含量与温度T的关系。图(Ⅱ)表示在一定条件下达到平衡后,t时刻改变影响平衡的另一个条件,重新建立平衡的反应过程。由此可判断该反应中
 A、m+n>p+q,
A、m+n>p+q, 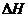 <0
<0
B、m+n>p+q, 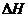 >0
>0
C、m+n<p+q, 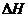 >0
>0
 D、m+n<p+q,
D、m+n<p+q,  <0
<0
6、根据下图中的两个图象,选出符合题意的反应方程式
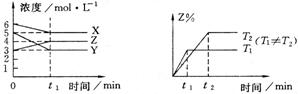
 A、X+2Y
Z;
A、X+2Y
Z; >0
>0
 B、X+2Y
Z;
B、X+2Y
Z; <0
<0
 C、5X+3Y
4Z;
C、5X+3Y
4Z;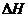 <0
<0
 D、X+2Y
3Z;
D、X+2Y
3Z;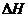 <0
<0
5、 对于反应mA(g)+nB(g) pC(g)+gD(g);△H=Q,改变反应条件时,
对于反应mA(g)+nB(g) pC(g)+gD(g);△H=Q,改变反应条件时,
A的转化率变化情况如图所示,符合题意的是
A、m+n=p+g;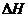 <0 B、m+n<p+g;
<0 B、m+n<p+g;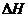 <0
<0
C、m+n<p+g;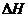 >0 D、m+n>p+g;
>0 D、m+n>p+g;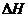 >0
>0
4、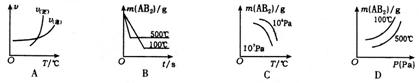 在可逆反应A2(g)+2B2(g)====2AB2(g)(正反应为放热反应)趋向平衡时,图中符合勒夏特列原理的是
在可逆反应A2(g)+2B2(g)====2AB2(g)(正反应为放热反应)趋向平衡时,图中符合勒夏特列原理的是

3、可逆反应mA(s)+nB(g)  eC(g)+fD(g),反应过程中,当其他条件不变时,C的体积分数w(C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系见下图,下列叙述正确的是
eC(g)+fD(g),反应过程中,当其他条件不变时,C的体积分数w(C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系见下图,下列叙述正确的是  A、达平衡后,若使用催化剂,C的体积分数将增大
A、达平衡后,若使用催化剂,C的体积分数将增大
B、达平衡后,若温度升高,化学平衡向逆反应方向移动
C、化学方程式中:n>e+f
D、达平衡后,增加A的质量有利于化学平衡向正反
应方向移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com