
15.答案:D
解析:A、B选项因是干燥的故HCl、Cl2都不作用;C项两者都生成白色沉淀。而D项HCl无变化,Cl2可使其变蓝。
14.答案:B
解析:随卤素原子半径的增大即按其原子核电荷增加的顺序,它们单质的熔点升高,对应阴离子的还原性增强,气态氢化物稳定性减弱;单质的氧化性减弱。
13.答案:B
解析:由题给反应,要证明有IO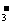 ,应用到I-、淀粉和酸。现给出了KI淀粉试纸,包括前两种试剂,所以再选用食醋(即酸)便可完成上述检验。向待测液中加入醋酸,然后将溶液滴在KI淀粉试纸上,若试纸变蓝,即证明有IO
,应用到I-、淀粉和酸。现给出了KI淀粉试纸,包括前两种试剂,所以再选用食醋(即酸)便可完成上述检验。向待测液中加入醋酸,然后将溶液滴在KI淀粉试纸上,若试纸变蓝,即证明有IO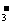 。
。
12.答案:D
解析:I2不能食用,KIO和NaIO不稳定,故选D。
11.答案:BC
解析:硫酸不能将Fe2+氧化成Fe3+;氯水能将溶液中的Fe2+氧化成为Fe3+离子;金属铁溶于盐酸得到氯化亚铁的强酸性溶液,再加入硝酸锌后,溶液就显示有硝酸的性质,可以将Fe2+氧化成为Fe3+离子。氯化铜溶液中的Cu2+离子有一定的氧化能力,可以将金属铁氧化成Fe2+离子,但却不能将Fe2+离子氧化成为Fe3+离子。
10.答案:B
解析:ICl中I带部分正电荷结合水分子中的OH-,形成HIO,则带部分负电荷的Cl结合H2O分子带部分正电荷的H+,形成HCl。
9.答案:D
解析:假设反应中生成1 mol NaClO和3 mol NaClO3,则有1 mol+3 mol×5=16 mol电子发生转移,由电子守恒知,必有16 mol氯原子被还原。
8.答案:C
解析:苯的密度比水轻,CCl4的密度比水重;酒精和汽油的气味有明显不同;碘易升华,而KMnO4虽显紫色,但无此性质;NH4Cl和NH4NO3的物理性质相似,不易区别。
7.答案:A
解析:溴化钠是一种离子晶体,可溶于水,且熔点较高;其中溴离子可与银离子结合生成浅黄色的溴化银沉淀;溴离子能被浓硫酸氧化为单质的溴,所以常用浓磷酸与溴化钠反应制取溴化氢;自然界中溴以化合态存在,用单质钠与单质溴反应制溴化钠的经济成本太高。
6.答案:A
解析:同主族元素的气态氢化物的稳定性由上至下依次减弱。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com