
1.下列物质中含有共价键的离子化合物是
A. Ba(OH)2 B.CaCl2 C. H2O D. H2
2、为什么冰会浮在水面上?雪花为什么是六角形的?
在水蒸气中水是以单个的H2O分子形式存在;在液态水中,经常以几个水分子通过氢键结合起来,形成(H2O)n;在固态水(冰)中,水分子大范围地以氢键互相联结,形成相当疏松的晶体,从而在结构中有许多空隙,造成体积膨胀,密度减小,因此冰能浮在水面上。水的这种性质对于水生动物的生存有重要意义。
[小结]这节课重点学习了化学键、化学键的分类、及离子键共价键的区别,化学反应的实质。
[自我评价]
1、分子间作用力
(1) 定义:把分子聚集在一起的作用力叫做分子间作用力(也叫范德华力)。
[问] 请大家思考一下,分子间作用力是不是一种化学键,为什么? 请举例说明。
[讲] 大家所举例子都很恰当,也即分子间作用力不是化学键,它比化学键要弱得多,它主要影响物质的熔、沸点等物理性质,而化学键主要影响物质的化学性质。分子间作用力广泛地存在于分子与分子之间,如:多数非金属单质、稀有气体、非金属氧化物、酸、氢化物、有机物等。但只有在分子与分子充分接近时,分子间才有明显的作用。分子间作用力对物质的熔点、沸点、溶解度等都有影响。
[投影]根据图总结一下分子间作用力对物质的影响
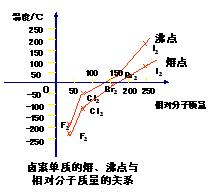
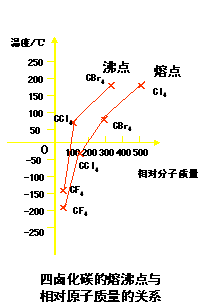
[板书] (2)一般来说,对于组成和结构相似的物质,相对分子质量越大,分子间作用力越大,物质的熔、沸点越高。
[思考与交流]对于四氟化碳、四氯化碳、四溴化碳、四碘化碳,其熔沸点如何变化?
[投影小结]化学键与分子间作用力的比较

[思考与交流]为什么HF、H2O和NH3的沸点会反常呢?
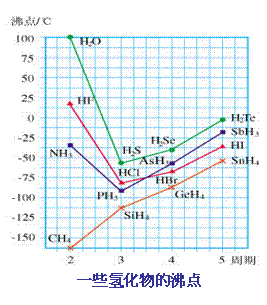
[板书] 2、氢键:
[讲]与吸电子强的元素(F、O、N等)相结合的氢原子,由于键的极性太强,使共用电子极大地偏向于高电负性原子。而H原子几乎成了不带电子、半径极小的带正电的核,它会受到相邻分子中电负性强、半径较小的原子中孤对电子的强烈吸引,而在其间表现出较强的作用力,这种作用力就是氢键。
[板书] (1) 形成条件:原子半径较小,非金属性很强的原子X,(N、O、F)与H原子形成强极性共价键,与另一个分子中的半径较小,非金属性很强的原子Y (N、O、F),在分子间H与Y产生较强的静电吸引,形成氢键
[投影]
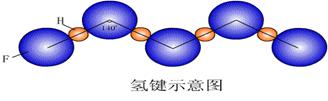
[讲述]氢键的形成对化合物的物理和化学性质具有重要影响。 化合物的熔沸点,主要取决于分子间力,其中以色散力为主。以氧族元素为例,H2Te、S2Se、H2S随相对分子质量的减小,色散力依次减弱,因而熔沸点依次降低。然而H2O由于分子间氢键的形成,分子间作用力骤然增强,从而改变了Te-S氢化物熔沸点降低的趋势而猛然升高,卤族中的HF和氮族中的NH3也有类似情况。
[板书] (2) 氢键作用:
1 使物质有较高的熔沸点(H2O、HF 、NH3)
2 使物质易溶于水(C2H5OH,CH3COOH)
[思考与交流]1、根据元素周期律,卤素氢化物的水溶液均应为强酸性,但HF表现为弱酸的性质,为什么?
2、对于共价化合物,例如酸溶于水,在水的作用下,使其分子内共价键被破坏
[过]在分子内相邻原子之间存在着强烈的相互作用,我们称之为化学键,实际上还存在一种把分子聚集在一起的作用力,我们叫做分子间作用力,又称为范德华力。
[板书] 四、分子间作用力和氢键
1.定义:离子相结合或原子间相结合的作用力分子间的作用力称为化学键
[讲]一般的化学物质则主要由离子键或共价键结合而成,除此以外还有金属键。化学键的形成与原子结构有关,离子键通过原子价电子间的转移,共价键是原子价电子的共用。由此说明化学键可分为以下几类:
[板书]2.分类:
[投影]
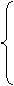 离子键
离子键
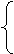 极性共价键
极性共价键
共价键 非极性共价键
配位键
金属键
[讲]在初中我们学过化学反应的实质是学生成新的物质,从化学键的角度应该如何解释呢?
其实在化学反应的过程中,包含着反应物分子内化学键的断裂和产物分子中新的化学键的形成。以Cl2和H2 反应为例,Cl-Cl和H-H 键断裂成H原子、Cl原子(旧键的断裂)后H原子Cl原子组合学生成HCl分子,也就形成了H-Cl键(新键的形成)。
[板书]3、化学反应的实质:旧化学键的断裂和新化学键的形成。
[讲]大家要注意的是,若只有键的断裂没有键的形成这不能称为化学反应。
例:(1)HCl溶于水,电离成H+、Cl-破坏了两者间的共价键,但没有形成新的化学键所以不为化学反应。(2)NaCl固体受热变为熔融状态,破坏了Na+、Cl-之间的作用力,但未结合成新的化学键,也不为化学反应。
[投影小结]1、对于离子化合物,溶于水和熔化后,离子键被破坏,成为自由移动的阴阳离子
6、用电子式下列物质的形成过程。
Mg3N2 、Na2S、MgBr2、Na2O
教 案
长春市第二实验中学 李佳惠
|
课题:第三节 化学键(二) 共价键 |
授课班级 |
|
||||
|
课 时 |
|
|||||
|
教 学 目 的 |
知识 与 技能 |
1、理解共价键的概念,初步掌握共价键的形成 2、通过学生对离子键和共价键的认识与理解,培养学生的抽象思维能力; 3、通过电子式的书写,培养学生的归纳比较能力 |
||||
|
过程 与 方法 |
培养学生从宏观到微观,从现象到本质的认识事物的科学方法 |
|||||
|
情感 态度 价值观 |
通过共价键形成过程的分析,培养学生怀疑、求实、创新的精神 |
|||||
|
重 点 |
共价键的形成及特征 |
|||||
|
难 点 |
用电子式表示共价分子的形成过程 |
|||||
|
知 识 结 构 与 板 书 设 计 |
二.共价键 1、定义:原子间通过共用电子对所形成的相互作用。 (1) 成键粒子:原子 (2) 成键性质:共用电子对间的相互作用 2.形成条件: 同种或不同种非金属元素原子结合; 部分金属元素元素原子与非金属元素原子,如AlCl3 ,FeCl3; 3.存在: (1 ) 非金属单质 (2) 原子团 (3) 气态氢化物,酸分子,非金属氧化物,大多数有机物 4、电子式表示: 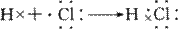  5.共价键的种类: (1) 配位键:共用电子对由成键单方面提供的共价键。例如NH4+ 、H3O+ (2) 非极性键:电子对处在成键原子中间; 极性键:电子对偏向于成键原子其中一方。 |
|||||
|
教学过程 |
||||||
|
教学步骤、内容 |
教学方法、手段、师生活动 |
|||||
|
[复习]复习离子键,原子、离子、分子的电子式以及离子化合物的形成过程的书写。 [引言]我们知道钠在氯气中燃烧学生成氯化钠分子,它是由钠离子和氯离子间的静电作用形成的。那我们在初中学习过的共价化合物HCl的形成和NaCl一样吗?H2和Cl2在点燃或光照的情况下,H2和Cl2分子被破坏成原子,当氢原子和氯原子相遇时是通过什么样的方式结合在一起的呢,是通过阴阳离子间静电作用结合在一起呢? [讲]氢原子最外层有一个电子要达到稳定结构就需要得到一个电子,氯原子最外有7个电子要达到8电子稳定结构需要得到一个电子,两原子各提供一个电子形成共用电子对,两原子都可以达到稳定结构 象氯化氢分子这样,原子间通过共用电子对所形成的相互作用就叫做共价键。 [板书]二.共价键 1、定义:原子间通过共用电子对所形成的相互作用。 [讲]让我们进一步深入的对概念进行一下剖析 [板书](1) 成键粒子:原子 (2) 成键性质:共用电子对间的相互作用 [问]那么什么样的元素原子之间能够形成共用电子对呢?(对照离子键形成的条件) [讲]得失电子能力较强的形成离子键,得失电子能力较差的一般形成共用电子对,这也就说明了形成共价键的条件。 [板书]2.形成条件: 同种或不同种非金属元素原子结合; 部分金属元素元素原子与非金属元素原子,如AlCl3 ,FeCl3; [讲]象HCl这样以共用电子对形成分子的化合物叫做共价化合物。 [问]还有哪些是共价化合物呢?举例说明。 [讲]刚才我们所举例的化合物都符合我们所说的共价化合物的形成条件,那是不是所有的由非金属元素原子组成的化合物都是共价化合物呢? [讲]象NH4Cl,(NH4)2SO4由非金属组成,但是是离子化合物。NH4+我们把它当作金属离子。 [问]那么共价间存在在哪里呢? [板书]3.存在: 1 非金属单质 ② 原子团 ③ 气态氢化物,酸分子,非金属氧化物,大多数有机物 [讲]共价键是在分子、原子、原子团中,相邻两个或多个原子通过共用电子对(电子云重叠)所形成的相互作用,参与成键的原子各自提供未成对的价电子形成共用电子对,这一对电子同时围绕成键的两原子核运动,并在原子核间出现的几率最大,通过这样的共用电子对与原子核间的相互作用,形成了稳定的共价键。 [讲]在HCl分子中,由于Cl对电子对的吸引力比H稍强,所以,电子对偏向氯一方,即氯略显负电性,H略显正电性,但作为整体仍显电中性,以上过程用电子式表示如下: [板书]4、电子式表示: 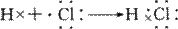  [讲]在HCl分子中,共用电子对仅发生偏移,没有发生电子转移,并未形成阴阳离子。因而,书写共价化合物的电子式时不能标电荷,在用电子式表示共价化合物时,首先需要分析所涉及的原子最外层有几个电子,需共用几对电子,才能形成稳定的结构,再根据分析结果进行书写。 [点击试题]1、用电子式表示下列物质:O2、N2、OH―、H2O 2、用电子式表示下列共价化合物的形成过程 CO2、CH4、NH3 [讲]在HF分子中,F原子吸引电子的能力强于H原子,电子对偏向于F原子方向,即F原子带部分负电荷,H原子带部分正电荷,整个分子显中性,在HF的形成过程中并没有电子的得失,也未形成阴阳离子,所以书写共价化合物的电子式不能标电荷。 [投影小结]在书写电子式时要注意: 1.电子对共用不归属于成键其中任何一个原子,不能像离子化合物一样用[ ] 2.不能用“→”表示电子的转移。 [思考与交流]根据H2、 Cl2 、 O2 的电子式思考为什么H2 、Cl2 、O2 是双原子分子,而稀有气体为单原子分子?(从电子式的角度考虑) 因为H、Cl、O、N两两结合才能形成稳定结构,而构成稀有气体的原子本身就具有稳定结构 [过]在化学上,我们常用一根短线来表示一对共用电子,这样得到的式子又叫结构式。 [点击试题]用结构式表示:N2、CH4、NH3、CO2、HCl、HClO [讲]以上共价键由共用电子对都是由成键双方提供的,那么共用电子对能不能由成键原子单方面提供呢?下面我们通过NH4+ 的形成及结构进行说明。我们知道氨分子和氢离子可结合成铵离子,那么它们是通过什么方式结合的呢? [讲]从氨分子的电子式可看出氨分子在氮原子周围有一对未共用电子(又称孤对电子)而氢离子的周围是空的,当氨分子和氢离子相遇时,氢离子共用了NH3 分子中未共用的电子对,从而是两者都达到稳定结构,这时氮原子和氢原子之间又多了一种化学键,氨分子也因氢离子的介入而带了正电荷,变成NH4+。 像这样共用电子对由成键单方面提供的共价键叫做配位键,配位键属于共价键的一种。 [板书]5.共价键的种类: (1) 配位键:共用电子对由成键单方面提供的共价键。例如NH4+ 、H3O+ [讲]在我们以上所接触的分子中,有些共用电子对处在中间位置,也有些偏向成键原子的其中一方。因此,我们又可以把共价键分为:电子对处在中间的称为非极性键(也就是两者吸引电子的能力一样,指相同元素原子),电子对偏向于成键原子其中一方的称为极性键(两者吸引电子的能力不同,就是不同非金属元素原子)。 [板书](2) 非极性键:电子对处在成键原子中间; 极性键:电子对偏向于成键原子其中一方。 [点击试题]判断Cl2 、N2 、HCl、NH3 、NaOH、H2O2分子中共价键的极性。 [小结]这节课我们主要介绍了共价键饿相关知识,共价化合物的电子式、形成过程,共价键的分类,我们要能够判断出极性键、非极性键。 [自我评价] 1.下列含有共价键的化合物是( ) A.HI B.NaOH C.Br2 D.NaCl 2.下列叙述正确的是( ) A.O2分子间存在着非极性共价键 B.CO2分子内存在着极性共价键 C.SO2与H2O反应的产物是离子化合物 D.盐酸中含有H+和Cl-,故HCl为离子化合物 3.含有下列键型的物质,可能为单质的是( ) A.只有离子键的物质 B.既有离子键,又有非极性键的物质 C.既有极性键,又有离子键的物质 D.只有非极性键的物质 4.下列性质中,可以证明某化合物内一定存在离子键的是( ) A.可溶与水 B.具有较高的熔点 C.水溶液能导电 D.熔融状态能导电 5. 膦(PH3)又称为磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含之。它的分子是三角锥形。以下关于PH3的叙述正确的是( ) A.PH3是非极性分子 B.PH3分子中有未成键的电子对 C.PH3是一个强氧化剂 D.PH3分子中的P-H键是非极性键 6. 有人建议将氢元素排在元素周期表的VIIA族。下列事实能支持这一观点的是( ) ①H原子得到一个电子实现最外电子层稳定结构;②氢分子的结构式为H-H;③与碱金属元素形成离子化合物M+[:H]-;④分子中原子间的化学键都属于非极性键 A.只有①②③ B.只有①③④C.只有②③④ D.有①②③④ |
|
|||||
|
教学回顾: |
||||||
教 案
|
课题:第三节 化学键(三) 化学键与分子间作用力 |
授课班级 |
|
|||||||||||||
|
课 时 |
|
||||||||||||||
|
教 学 目 的 |
知识 与 技能 |
1、理解化学键的概念,培养学生对微观粒子运动的想象力 2、了解极性键和非极性键以及分子构型问题 |
|||||||||||||
|
过程 与 方法 |
1、通过学生对化学键的认识与理解,培养学生的抽象思维能力 2、通过电子式的书写,培养学生的归纳比较能力, 3、通过分子构型的教学培养学生的空间想象力 |
||||||||||||||
|
情感 态度 价值观 |
1、通过对化学键形成过程的分析,培养学生怀疑、求实、创新的精神 2、在学习过程中,激发学生的学习兴趣和求知欲 3、培养学生从宏观到微观,从现象到本质的认识事物的科学方法 |
||||||||||||||
|
重 点 |
化学键的概念, |
||||||||||||||
|
难 点 |
化学键的实质 |
||||||||||||||
|
知 识 结 构 与 板 书 设 计 |
知识拓展------共价键性质的参数 1、键长:成键的两个原子或离子的核间距离。 3、键角:分子中相邻的两个键之间的夹角。 2、键能:拆开1 mol某键所需的能量叫键能。单位:kJ/mol。 三、化学键 1.定义:离子相结合或原子间相结合的作用力分子间的作用力称为化学键 2.分类: 3、化学反应的实质:旧化学键的断裂和新化学键的形成。 四、分子间作用力和氢键 1、分子间作用力 (1) 定义:把分子聚集在一起的作用力叫做分子间作用力(也叫范德华力)。 (2)一般来说,对于组成和结构相似的物质,相对分子质量越大,分子间作用力越大,物质的熔、沸点越高。 (2) 氢键作用: 1 使物质有较高的熔沸点(H2O、HF 、NH3) 2 使物质易溶于水(C2H5OH,CH3COOH) |
||||||||||||||
|
教学过程 |
|||||||||||||||
|
教学步骤、内容 |
教学方法、手段、师生活动 |
||||||||||||||
|
[知识回顾]回忆一下共价键,极性键,非极性键和配位键的定义 请写出NH4+ 的电子式 [过]为了进一步描述共价键的强弱,表述结构相似的物质的性质,我们在这里为大家拓展了有关共价键参数的问题 [板书]知识拓展------共价键性质的参数 1、键长:成键的两个原子或离子的核间距离。 [讲]键长决定分子的稳定性,一般说来,键长越短,键越强,也越稳定。键长的大小与成键微粒的半径大小有关。如键和H-Cl<H-Br<H-I,则稳定性:H-Cl>H-Br>H-I。 [板书]2、键能:拆开1 mol某键所需的能量叫键能。单位:kJ/mol。 [讲]键能决定分子的稳定性,键能越大,键越牢,分子越稳定。 [板书]3、键角:分子中相邻的两个键之间的夹角。 [讲]键角决定分子的空间构型,凡键角为180°的为直线型,如: 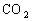 ;凡键角为109°28′的为正四面体,如: ;凡键角为109°28′的为正四面体,如: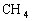 。 。[投影] 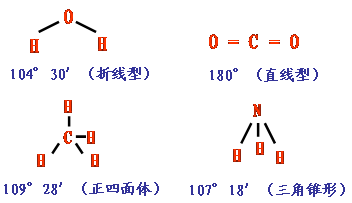 [过]前面两节课我们介绍了离子键、共价键,请大家回忆一下相关内容,然后回答它们之间有什么区别。 [投影小结]离子键、共价键的比较
[讲]通过学习有关离子键和共价键的认识,我们知道,原子结合成分子时,原子之间存在着相互作用,这种作用不仅存在于直接相邻的原子之间,而且也存在于分子内非直接相邻的原子之间,前一种相互作用比较强烈,破坏它要消耗较大的能量,是使原子互相联结成分子的主要因素。 离子键使离子结合形成离子化合物;共价键是原子结合形成共价化合物分子,那么人们通常称离子相结合或原子间相结合的作用力为化学键。 [板书]三、化学键 5、下列各数值表示有关元素的原子序数,其所表示的各原子组中能以离子键相互结合成稳定化合物的是:( C ) A.10与12 B.8与17 C.11与17 D.6与14 4、下列说法正确的是:( D ) A.离子键就是使阴、阳离子结合成化合物的静电引力 B.所有金属与所有非金属原子之间都能形成离子键 C.在化合物CaCl2中,两个氯离子之间也存在离子键 D.钠原子与氯原子结合成氯化钠后体系能量降低 3.下列化合物电子式书写正确的是( )
2.下列微粒电子式错误的是( B )
同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |