
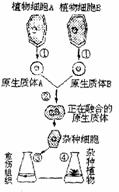
31.I.(每空1分,共l0分)右图是植物体细胞杂交过程示意图。
据图分析回答:
(1)图中的④过程是____,目前最常用的方法是____。
(2)②过程的发生,常用的化学方法是用____诱导,该过
程依赖细胞膜的结构特点是:________。
(3)融合成功的标志是____,该结构的产生与细胞内____
(细胞器)有关。
(4)③和④过程是一个 和 的过程,在该过
程中,细胞分裂的主要方式是________。
(5)植物体细胞杂交技术的意义在于: ,
大大扩展了可用于杂交的亲本组合范围。
II.(每空2分,共12分)现有一种植物的种子,不知道它
的萌发过程是否与光照有关。下面是探究此问题的实验。
(1)体提出的假设是: 。
实验材料和用品:数量充足的铺有滤纸的培养皿、无菌水、表面消毒过的种子等。
实验方案:
①向两组培养皿中倒入适量的水,每组培养皿中放入100粒种子。
②将一组置于____环境中,另一组置于____环境中。培养过程满足种子萌发所需的其它条件相同且适宜。
③数日后,分别统计两组处理中萌发种子的数照,并计算出各皂的发芽率。
(2)你预期(期望得到)的实验结果是;
(3)若两组的发芽率无明显差异,你的实验结论是: 。
(4)若两组的发芽率差异很显著(或一组绝大部分萌发,另一组未萌发),你的实验结论是: 。
30.I.(每空1分,共8分)下图为人体血糖平衡调节示意图,请据图回答有关问题
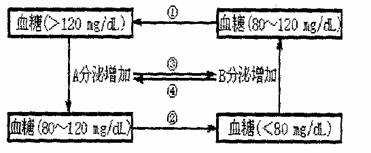
(1)当由于①使血糖含量上升时,A____的分泌会增加,通过促进合成___ _,以及转化成非糖物质等途径,使血糖含量恢复至正常水平。当由于②使血糖含量降低时,B 的分泌增加,主要通过促进____,使血糖恢复至正常水平。
(2)A的增加会③ B的分泌,B的分泌增加会④____ A的分泌,从而共同维持血糖含量的相对稳定。
(3)在血糖平衡调节中,与B激素具有协同作用的激素是____。
(4)糖尿病痛人会出现高血糖和糖尿,其根本原因在于患者 。
II.(每空2分,共12分)植物的新陈代谢受外部环境因子(如光、温度)和内部因子(如激素)的影响,研究内、外园子对植物生命活动的影响具有重要意义。下图表示野外松树(阳生植物)光合作用强度与光照强度的关系。英中的纵坐标表示松树整体表现出的吸收CO2和释放CO2量的状况。请分析回答:
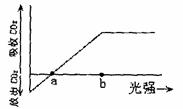
(1)光照强度为b时,该植物光合作用强度____,光照强度再增强, 。
(2)光照强度为a对,光合作用吸收CO2的量等于呼吸作用放出CO2的量。如果白天光照强度较长时期为a,植物能不能正常生长____?为什么____
 (3)妇果将曲线改绘为人参(阴生植物)光合作用强度与光照强度关系的盐线,b点的位置应如何移动____,为什么____
(3)妇果将曲线改绘为人参(阴生植物)光合作用强度与光照强度关系的盐线,b点的位置应如何移动____,为什么____
29.(15分)测定慕硫酸锄黑体(Na2SO4·XH2O)中结晶水含量韵实验包括如下两步:
①将硫酸钠晶体制成粉末,准确称取该样品26.8 g
②将样品加热至恒重,冷却后称得样品质量变为14.2 g
试回答下列问题:
(1)将晶体制成粉末,所用的主要化学仪器是____(填仪器名称,下同);准确称量后将样品放在 中加热至恒重。
(2)判断试样已加热至恒重的标准是________。
(3)根据实验数据计算出x=____。
(4)下面的情况有可能造成测定结果偏低的是 (填序号)。
A.试样中含有加热易挥发的杂质 B.加热后不是在于燥器中冷却试样
C.实验前坩埚来完全干燥 D.加热时有晶体溅出
E.试样中含有加热不挥发的杂质
28.(14分)
I.常温下浓度均为0.l mol/L的下列溶液:①Na2CO3溶液②NaHCO3溶液③盐酸④氨水
回答下列问题。
(1)上述溶液中有水解反应发生的是 (填编号,下同),溶液中溶质存在电离平衡的是 。
(2)四种溶液中对水的电离抑制作用最大的是 ;比较①、②溶液,pH较大的是 。
(3)在溶液④中加入NH4Cl固体,NH+4浓度与OH-浓度的比值将____(填“变大”、“变小”、“不变”)
 II.有一瓶无色澄清溶渡,其中可能含有:NH+4、K+、Mg2+、Al3+、Fe2+、NO-3、Cl-、SO2-4、CO2-3取该溶液进行下列实验:
II.有一瓶无色澄清溶渡,其中可能含有:NH+4、K+、Mg2+、Al3+、Fe2+、NO-3、Cl-、SO2-4、CO2-3取该溶液进行下列实验:
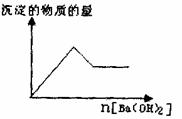
(1)取部分溶液,向其中逐滴滇入Ba(OH)2溶液至过
量,有白色沉淀生成,沉淀量与加入Ba(OH)2溶
液量的关系如右图所示。
(2)取(I)反应后过滤所得沉淀和滤液,在沉淀中加入
稀盐酸后,沉淀不减少。将滤液分为两等份,一份加
热,未产生刺激性气味的气体;另一份如HNO3酸化
时有白色沉淀产生,继续加HNO3,沉淀又消失,再加AgNO3没有变化。
根据以上事实确定:
该溶液中肯定存在的离子有 ;
肯定不存在的离子有____ 。
27.(17分)
I.(1)亚硫酸钠和碘酸钾在酸性溶液中发生以下反应:
Na2SO3+ KIO3+ H2SO4-- Na2SO4+ K2SO4+ I2+ H2O
①配平上面的氧化还原反应方程式,将计量数填在方框内。
②其中氧化剂是 ,若反应中有5 mol电子转移,则生成的碘是 mol。
(2)0.3 mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5 kJ热量,乙硼烷燃烧热的热化学方程式为 。
II.含氰化物(有CN-)的废水危害大,CN-的含量为0.01mol/L~0.04mol/L就能毒杀鱼类。其处理方法是用氧化法使其转化为低毒的氰酸钾(KCNO),氧化剂常用次氯酸盐;而生成的CNO-可进一步降解为能直接排放到空气中的无毒气体。近期研究将把某些导体的小粒悬浮在溶液中,在光的作用下,在小粒和溶液界面发生氧化还原反应。但小粒的质量和性质不发生变化,如二氧化钛(TiO2)小粒表面就可以破坏氰化物等有毒废物。
(1)二氧化钛在上述反应中的作用是 。
(2)CNO-经进一步处理后产生的两种无毒气体应该是 和 。
(3)若用NaClO溶液处理NaCN的废液,产生另外两种盐,其化学方程式为 。
26.(14分)短周期元素A、B、C、D、E原子序数依次增大,其中D是日常生活中常见的金属元素,E是所在周期原子半径最小的主族元素,A、B、C分别位于不同周期,且A和C同主族。回答下列问题:
(1)B和A组成的简单化合物与B元素最高价的含氧酸反应生成一种盐,则B和A组成的简单化合物的化学式为 ,其空间构型为 型,属于 (填“极性”或“非极性”)分子。
(2)D原子结构示意图为 ,C的晟高价氧化物对应水化物与D的最高价氧化物对应水化物反应的离子方程式为 。
(3)在B和A组成的简单化台物与BE3这两种物质中B元素的化合价相同,其中BE3可与水发生水解反应,其中会生成一种强氧化性物质,则反应方程式为 ,该强氧化性物质的结构式为 。
25.(20分)静止在匀强磁场中的锂原子核(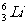 ),俘获一个速度为7.7×104m/s的中子而发生核反应放出
),俘获一个速度为7.7×104m/s的中子而发生核反应放出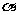 粒子后变成一个新原子核,已知中子速度方向与磁场方向垂直,测得
粒子后变成一个新原子核,已知中子速度方向与磁场方向垂直,测得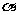 粒子速度为2×10m/s,方向与中子速度方向相同,求:
粒子速度为2×10m/s,方向与中子速度方向相同,求:
(1)写出核反应方程式;
(2)生成的新核的速度大小和方向(在运用动量守恒时,不考虑质量亏损):
(3)若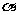 粒子与新核间相互作用不计,则二者在磁场中运动轨道半径之比为多少?
粒子与新核间相互作用不计,则二者在磁场中运动轨道半径之比为多少?
(4)经过测量发现在核反应前后原子核总质量减少了0.035u,则这个反应放出了多少焦耳的能量?
24.(18分)一辆汽车以54km/h的速度匀速行驶,现在前方出现红灯,汽车以1 5m/s2的加速度做匀减速直线运动恰好在斑马线前停下,然后在斑马线前又等了0.5min后绿灯亮,汽车立即以lm/s2的加速度作匀加速直线运动,直到恢复到原来的速度正常行驶。求:
(1)汽车刹车后产t=12s时的位移大小;
(2)这辆汽车通过这个红绿灯所延误的时间是多少?
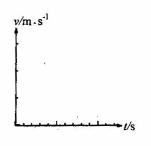
(3)结合上面计算数据,在坐标系中取适当标度画出整个过程的v-t图。
23.(14分)如图所示,质量为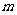 的物体A放在倾角θ=37°的斜面上时,轻轻一推恰好能沿斜面匀速下滑。
的物体A放在倾角θ=37°的斜面上时,轻轻一推恰好能沿斜面匀速下滑。
(1)请简要分析判断斜面与地面间有无摩擦力?
(2)现用细线系住物体A,并平行于斜面向上绕过光滑的定滑轮,另一端系住物体B,欲使物体A和B都处于静止状态,则物体B的质量应满足什么条件?(设最大静摩擦力等于滑动摩擦力,sin37°=0.6,cos37°=0.8)
22.本题共两小题(20分)
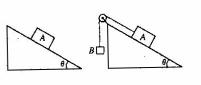
(1)(4分)如图所示,游标卡尺的读数为 cm。
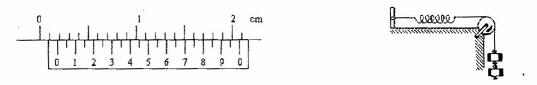
 (2)某同学在做“探究弹力和弹簧伸长的关系”的实验时,
(2)某同学在做“探究弹力和弹簧伸长的关系”的实验时,
所用实验装置如图所示,所得的测量数据如下表所示
(一个钩码的质量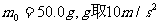 )。
)。
|
钩码个数 |
0 |
1 |
2 |
3 |
4 |
5 |
|
弹簧长度/cm |
40.00 |
42.02 |
43.96 |
46.02 |
47.21 |
50.00 |
①(4分)请在坐标纸中建立坐标系,画出弹力F与弹簧伸长量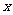 的关系图象(要求明确写出坐标轴代表的物理量和单位)。由图可知该弹簧的劲度系数
的关系图象(要求明确写出坐标轴代表的物理量和单位)。由图可知该弹簧的劲度系数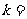 N/m
N/m
 ②(2分)如果弹簧受到的拉力F=5.0N时,仍在弹簧的弹性限度内,则弹簧的长度为
cm.
②(2分)如果弹簧受到的拉力F=5.0N时,仍在弹簧的弹性限度内,则弹簧的长度为
cm.
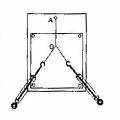
(3)①(6分)在《验证力的平行四边形定则》的实验中,如图所示在水平放置的木反上垫上一张白纸,把橡皮条的一端固定在板上的A点,橡皮条的另一端拴上两个细绳套。先用两个弹簧秤钩住细绳套,互成角度拉橡皮条使之伸长,将结点拉到某一位置O,此时需记下 、 、 ;再用一个弹簧秤钩住细绳套把橡皮条拉长,将结点位置拉到 ,记下 、 。
②(4分)下列关于本实验的说法中,正确的是
A.拉橡皮条的细绳套长一些较好
B.F1和F2之间的夹角越大越好
C.若实验中作出F和F′的图示不完全重合,则证明力的平行四边形定则是不完全正确的
D.若F1和F2的方向不变而大小都增大1N,则合力方向不变,大小也增大1N
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com