
1.氨气(NH3):
(1)分子结构:由极性键形成的三角锥形的极性分子,N原子有一对孤对电子;
(2)物理性质:无色、刺激性气味的气体,密度比空气小,极易溶于水,常温常压下
1体积水能溶解700体积的氨气,易液化(可作致冷剂)
(3)化学性质:
①与H2O反应:NH3
+ H2O  NH3·H2O
NH3·H2O NH4+ + OH-,
NH4+ + OH-,
溶液呈弱碱性,氨水的成份为:NH3 、 H2O、NH3·H2O、NH4+ 、 OH-、H+,氨水易挥发;
②与酸反应:NH3 + HCl = NH4Cl NH3 + HNO3 = NH4NO3 与挥发性酸反应有白烟生成
③还原性(催化氧化):
|
4NH3 + 5O2 = 4NO + 6H2O(N为-3价,最低价态,具有还原性)
(4)实验室制法 Ca(OH)2 + 2NH4Cl CaCl2 +
2NH3↑ + 2H2O,
CaCl2 +
2NH3↑ + 2H2O,
工业㓡法:N2与H2在高温高压催化剂条件下合成氨气
3、比较H2O和H2O2
|
|
H2O |
H2O2 |
|
电子式 |
H: O: H |
H:O:O:H |
|
化学键 |
极性键 |
极性键和非极性键 |
|
分子极性 |
有 |
有 |
|
稳定性 |
 稳定 稳定2H2O 2H2↑+O2↑ |
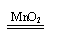 不稳定 不稳定2H2O2 2H2O+O2↑ |
|
氧化性 |
较弱(遇强还原剂反应) 2Na+2H2O==2NaOH+H2↑ |
较强(遇还原剂反应) SO2+H2O2===H2SO4 |
|
还原性 |
较弱 (遇极强氧化剂反应) 2F2+2H2O===4HF+O2 |
较强 (遇较强氧化剂反应) 2MnO4-+5H2O2+6H+==2Mn2++5O2↑+8H2O |
|
作用 |
饮用、溶剂等 |
氧化剂、漂白剂、消毒剂、脱氯剂等 |

H2S+H2SO4(浓) S↓+SO2↑+H2O
S↓+SO2↑+H2O
SO3+2NaHSO3==Na2SO4+2SO2+H2O
3CuSO4  3CuO+2SO2↑+SO3↑+O2↑
3CuO+2SO2↑+SO3↑+O2↑
6FeSO4+3Br2══2Fe2(SO4)3+2FeBr3
2、O2和O3比较
|
|
O2 |
O3 |
|
颜色 |
无色 |
气态-淡蓝色 |
|
气味 |
无 |
刺激性特殊臭味 |
|
水溶性 |
臭氧密度比氧气的大 |
|
|
密度 |
臭氧比氧气易溶于水 |
|
|
氧化性 |
强 (不易氧化Ag、Hg等) |
极强(O3+2KI+H2O==2KOH+I2+O2) (易氧化Ag、Hg等不活泼金属) |
|
漂白性 |
无 |
有(极强氧化性-作消毒剂和脱色剂) |
|
稳定性 |
 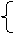 3O2
2O3 2O3===3O2 常温:缓慢 3O2
2O3 2O3===3O2 常温:缓慢加热:迅速 |
|
|
相互关系 |
臭氧和氧气是氧的同素异形体 |
1、氧族元素比较: 原子半径 O<S<Se<Te 单质氧化性 O2>S>Se>Te
单质颜色 无色 淡黄色 灰色 银白色 单质状态 气体 固体 固体 固体
氢化物稳定性 H2O>H2S>H2Se>H2Te 沸点 H2O>H2Te>H2Se>H2S(水反常)
最高价含氧酸酸性 H2SO4>H2SeSO4>H2TeO4
2、尾气处理: 氨水 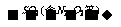 (NH4)2SO3
(NH4)2SO3 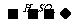 (NH4)2SO4+
SO2↑
(NH4)2SO4+
SO2↑
NH4HSO3
氧族元素
1、生产过程:
|
三阶段 |
SO2制取和净化 |
SO2转化为SO3 |
SO3吸收和H2SO4的生成 |
||||
|
三方程 |
2Fe2O3+8SO2 |
2SO2+O2 △ |
SO3+H2O=H2SO4 |
||||
|
三设备 |
沸腾炉 |
接触室 |
吸收塔 |
||||
|
有 关 原 理 |
矿石粉碎,以增大矿石与空气的接触面,加快反应速率 |
逆流原理(热交换器)目的: 冷热气体流向相反,冷的SO2、O2、N2被预热,而热的SO3、SO2、O2、N2被冷却. |
逆流原理(98.3%的浓硫酸从塔顶淋下,气体由下往上,流向相反,充分接触,吸收更完全) |
||||
|
设备中排出的气 体 |
炉气:SO2.N2.O2.矿尘(除尘).砷硒化合物(洗涤). H2O气(干燥)…… 净化气:SO2.N2.O2 |
SO2、O2、N2、SO3 |
尾气:SO2及N2、O2 不能直接排入大气中 |
||||
|
说 明 |
矿尘.杂质:易使催化剂“中毒” H2O气:腐蚀设备、影响生产 |
反应条件-- 理论需要:低温、高压、催化剂;实际应用:400℃-500℃、常压、催化剂 |
实际用98.3%的浓硫酸吸收SO3,以免形成酸雾不利于气体三氧化硫被进一步吸收 |
5、硫酸的工业制法──接触法
4、硫酸
①稀H2SO4具有酸的一般通性,而浓H2SO4具有酸的通性外还具有三大特性:
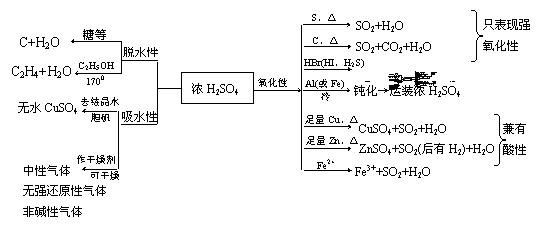
②SO42-的鉴定(干扰离子可能有:CO32-、SO32-、SiO32-、Ag+、PO43-等):
待测液 澄清液
澄清液 白色沉淀(说明待测液中含有SO42-离子)
白色沉淀(说明待测液中含有SO42-离子)
③硫酸的用途:制过磷酸钙、硫酸铵、硫酸铜、硫酸亚铁、医药、炸药,用于铅蓄电池,作干燥剂、制挥发性酸、作脱水剂和催化剂等。
3、硫的氧化物
(1)二氧化硫:
①SO2是无色而有刺激性气味的有毒气体,密度比空气大,容易液化,易溶于水。
②SO2是酸性氧化物,能跟水反应生成亚硫酸,亚硫酸是中强酸。
③SO2有强还原性 常见氧化剂(见上)均可与SO2发生氧化一还原反应
如:SO2 + Cl 2 +2H2O == H2SO4 + 2HCl
④SO2也有一定的氧化性 2H2S + SO2 == 3S↓ +2H2O
⑤SO2具有漂白性,能跟有色有机化合物生成无色物质(可逆、非氧化还原反应)
⑥实验室制法:Na2SO3 + H2SO4(浓) == Na2SO3 + H2O +SO2↑
或Cu + 2H2SO4(浓)  CuSO4 + 2H2O + SO2↑
CuSO4 + 2H2O + SO2↑
(2)三氧化硫:是一种没有颜色易挥发的晶体;具有酸性氧化物的通性,遇水剧烈反应生成硫酸并放出大量的热。
(3)比较SO2与CO2、SO3
|
|
SO2 |
CO2 |
SO3 |
||
|
主要物性 |
无色、有刺激性气体、易液化易溶于水(1:40) |
无色、无气味气体能溶于水(1:1) |
无色固体.熔点(16.8℃) |
||
|
与水反应 |
 SO2+H2O H2SO3 中强酸 SO2+H2O H2SO3 中强酸 |
 CO2+H2O H2CO2
弱酸 CO2+H2O H2CO2
弱酸 |
SO3+H2O==H2SO4(强酸) |
||
|
与碱反应 |
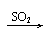 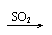 Ca(OH)2 CaSO3↓ Ca(HSO3)2 清液 白 清液 |
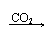  Ca(OH)2 CaCO3↓ Ca(HCO3)2 清液 白↓ 清液 |
SO3+Ca(OH)2==CaSO4(微溶) |
||
|
紫色石蕊 |
变红 |
变红 |
变红 |
||
|
品红 |
褪色 |
不褪色 |
不褪色 |
||
|
鉴定存在 |
能使品红褪色 又能使清石灰变浑浊 |
不能使品红褪色 但能使清石灰水变浑浊 |
|
||
|
氧化性 |
SO2+2H2S=2S↓+2H2O |
 CO2+2Mg
点燃 2MgO+C CO2+2Mg
点燃 2MgO+C
|
|
||
|
还原性 |
有 |
无 |
|
||
|
与Na2O2作用 |
Na2O2+SO2==Na2SO4 |
2Na2O2+2CO2==2Na2CO3+O2 |
2Na2O2+2SO3==2NaSO4+O2↑ |
(4)酸雨的形成和防治
酸雨的形成是一个十分复杂的大气化学和大气物理过程。酸雨中含有硫酸和硝酸等酸性物质,其中又以硫酸为主。从污染源排放出来的SO2、NOx(NO、NO2)是酸雨形成的主要起始物,因为大气中的SO2在光照、烟尘中的金属氧化物等的作用下,经氧化、溶于水等方式形成H2SO4,而NO被空气中氧气氧化为NO2,NO2直接溶于水形成HNO3,造成了雨水pH值降低,便形成了酸雨。
硫酸型酸雨的形成过程为:气相反应:2SO2+O2=2SO3、SO3+H2O=H2SO4;液相反应:SO2+H2O=H2SO3、2H2SO3+O2=2H2SO4。总反应: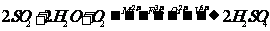
硝酸型酸雨的形成过程为:2NO+O2=2NO2、3NO2+H2O=2HNO3+NO。
引起硫酸型酸雨的SO2人为排放主要是化石燃料的燃烧、工业尾气的排放、土法炼硫等。引起硝酸型酸雨的NOx人为排放主要是机动车尾气排放。
酸雨危害:①直接引起人的呼吸系统疾病;②使土壤酸化,损坏森林;③腐蚀建筑结构、工业装备,电信电缆等。
酸雨防治与各种脱硫技术:要防治酸雨的污染,最根本的途径是减少人为的污染物排放。因此研究煤炭中硫资源的综合开发与利用、采取排烟脱硫技术回收二氧化硫、寻找替代能源、城市煤气化、提高燃煤效率等都是防止和治理酸雨的有效途径。目前比较成熟的方法是各种脱硫技术的应用。
在含硫矿物燃料中加生石灰,及时吸收燃烧过程中产生的SO2,这种方法称为“钙基固硫”,其反应方程式为:SO2+CaO=CaSO3,2CaSO3+O2=2CaSO4;也可采用烟气脱硫技术,用石灰浆液或石灰石在烟气吸收塔内循环,吸收烟气中的SO2,其反应方程式为:SO2+Ca(OH)2=CaSO3+H2O,SO2+CaCO3=CaSO3+CO2,2CaSO3+O2=2CaSO4。在冶金工业的烟道废气中,常混有大量的SO2和CO,它们都是大气的污染物,在773K和催化剂(铝矾土)的作用下,使二者反应可收回大量的硫黄,其反应原理为:SO2+2CO==S+CO2
2、硫的氢化物
①硫化氢的制取:
Fe+H2SO4(稀)=FeSO4+H2S↑(不能用浓H2SO4或硝酸,因为H2S具有强还原性)
--H2S是无色、有臭鸡蛋气味的有毒气体;能溶于水,密度比空气略大。
②硫化氢的化学性质
 A.可燃性: 2H2S+O2
点燃 2S+2H2O(H2S过量)
A.可燃性: 2H2S+O2
点燃 2S+2H2O(H2S过量)
 2H2S+3O2
点燃 2SO2+2H2O(O2过量)
2H2S+3O2
点燃 2SO2+2H2O(O2过量)
B.强还原性:常见氧化剂Cl2、Br2、O2、Fe3+、HNO3、KMnO4等,甚至SO2均可将H2S氧化成S。
C.不稳定性:300℃以上易受热分解
③H2S的水溶液叫氢硫酸,是二元弱酸。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com