
21.(2010·唐山模拟)某探究性学习小组拟用小颗粒状铝硅合金与足量稀硫酸的反应测定通常状况(约20℃,1atm)下气体摩尔体积的方法。拟选用下列实验装置完成实验:
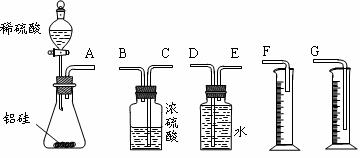
(1)该组同学必须选用的装置的连接顺序是(填接口字母,可不填满。):
A接( )( )接( )( )接( )
(2)实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶。请你帮助分析原因。_________________________。
(3)实验结束时,该组同学应怎样测量实验中生成氢气的体积?_______________。
(4)实验中准确测得4个数据:实验前铝硅合金的质量m1 g,实验后残留固体的质量m2 g,实验后量筒中液面读数为VmL。则通常状况下气体摩尔体积Vm=_________ L·moL-1。
[解析]测定气体的摩尔体积,可以测定一定量的金属和酸反应放出的氢气的体积,然后根据化学方程式得到气体的摩尔体积的计算表达式。(1)测定气体的体积可以用排水法测定液体的体积,为了能够保证将液体顺利排出,E为进气口,F为出水口,导气管深入量筒内部,可以防止液体溅出而使测得的气体体积偏小,所以正确的装置的连接顺序是A→E→D→G。(2)金属和酸反应为放热反应,而且随着反应快速进行,锥形瓶内气体越来越多,压强越来越大,所以分液漏斗内的液体不容易流下。(3)测量气体体积时,一定要使气体的温度和压强与外界温度和大气压相同,所以应将实验装置冷却到室温,然后调节量筒中液面与广口瓶中液面相平,以保证气体压强等于外界大气压,读数时注意要平视量筒刻度。(4)反应的铝的质量为m(Al)=(m1-m2)g,气体的体积为V×10-3L,由化学方程式:
2Al+3H2SO4=Al2(SO4)3+3H2↑
54g 3Vm L
(m1-m2)g V×10-3L
得Vm=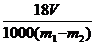 L·moL-1。
L·moL-1。
[答案](1)EDG (2)铝与稀硫酸反应放热且生成气体,使锥形瓶中气体压强变大 (3)待实验装置冷却后,上下移动量筒,使其中液面与广口瓶中液面相平,再平视读取量筒中水的体积,即氢气在通常状况时的体积。
(4)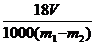
20.(2010·淄博模拟)在t℃时,将ag NH3完全溶解于水,得到VmL溶液。假设该溶液的密度为ρg·cm-3,质量分数为ω,其中含NH4+的物质的量为bmol。下列叙述正确的
是( )。
A.溶质的质量分数ω=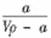 ×100%
×100%
B.溶质的物质的量浓度c=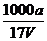 mol/L
mol/L
C.溶液中c(H+)=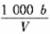 mol/L
mol/L
D.上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω
[解析]选B。
19.(2010·沈阳模拟)有一浓度为14%的KOH溶液,加热蒸发掉100g水后,得到浓度为28%的KOH溶液80mL,则浓缩后溶液的物质的量浓度为( )。
A.6mol/L B.6.25mol/L C.5mol/L D.7.25mol/L
[解析]选B。蒸发前后KOH的质量和物质的量都不变,假设原溶液的质量为x,则:x·14%=(x-100g)×28%,解得:x=200g,m(KOH)=200g×14%=28g,n(KOH)= =0.5mol,c(KOH)=
=0.5mol,c(KOH)=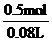 =6.25mol/L。
=6.25mol/L。
18.(2010·广元模拟)在某温度下,NaOH的溶解度为20克,该温度下将80克NaOH放入220克水中,充分搅拌后,测得溶液的密度为1.2g/mL,则溶液中溶质的物质的量浓度为( )。
A.0.02mol/L B.2.0mol/L C.5.0mol/L D.7.5mol/L
[解析]选B。假设220克水中最多溶解x g NaOH形成饱和溶液,则: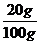 =
=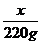 ,解得:x=44g<80g,所以NaOH没有完全溶解,溶液达到饱和。NaOH的质量分数为w(NaOH)=
,解得:x=44g<80g,所以NaOH没有完全溶解,溶液达到饱和。NaOH的质量分数为w(NaOH)=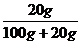 ×100%=16.7%,c(NaOH)=
×100%=16.7%,c(NaOH)=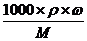 =
=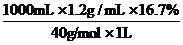 =5.0mol·L-1。
=5.0mol·L-1。
17.(2010·铜川模拟)20℃时,KCl的溶解度为34g,若忽略固体溶解引起的溶液体积变化,则在该温度下,所配KCl溶液的物质的量浓度不可能是( )。
A.5mol/L B.4mol/L C.3mol/L D.2mol/L
[解析]选A。饱和KCl溶液中KCl的物质的量浓度最大。假设将34gKCl固体溶于100g水中,则n(KCl)=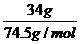 =0.46mol,溶液的体积近似等于水的体积,
=0.46mol,溶液的体积近似等于水的体积,
c(KCl)=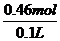 =4.6mol/L。因为不知道溶液是否饱和,所以其物质的量浓度≤4.6mol/L。
=4.6mol/L。因为不知道溶液是否饱和,所以其物质的量浓度≤4.6mol/L。
16.(2010·九江模拟)标准状况下,将VL A气体(摩尔质量为M g·mol-1)溶于0.1L水中,所得溶液密度为ρg·mL-1。则此溶液物质的量浓度为( )。
A.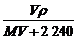 mol·L-1
B.
mol·L-1
B.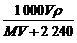 mol·L-1
mol·L-1
C.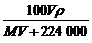 mol·L-1
D.
mol·L-1
D.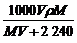 mol·L-1
mol·L-1
[解析]选B。c=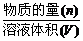 ,n=
,n= mol,溶液质量=(
mol,溶液质量=( ·M+100)g,所以溶液体积=
·M+100)g,所以溶液体积= ×10-3L,所以c=
×10-3L,所以c= mol÷(
mol÷( ×10-3)L=
×10-3)L=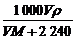 mol·L-1。
mol·L-1。
15.(2010·河池模拟)有五瓶溶液分别是:①10mL0.60mol/LNaOH水溶液 ②20mL0.50mol/LH2SO4水溶液 ③30mL0.40mol/LHCl水溶液 ④40mL0.30mol/LHAc水溶液 ⑤50mL0.20mol/L蔗糖水溶液。以上各瓶溶液所含离子、分子总数的大小顺序是( )。
A.①>②>③>④>⑤ B.②>①>③>④>⑤
C.②>③>④>①>⑤ D.⑤>④>③>②>①
[解析]选D。溶液中的离子.分子总数应包含水分子,因此溶液的体积就决定了离子分子总数的顺序。本题容易错选C,原因都是只考虑了溶质的离子和分子而忽略了溶剂中的水分子,不但丢分,而且计算量不小,浪费了许多宝贵的时间。因此,仔细审题,通盘考虑是关键。
14.(2010·荆州模拟)质量分数不同的两种硫酸溶液等质量混合时,其质量分数为a%,而等体积混合时为b%;质量分数不同的两种乙醇溶液等质量混合时,其质量分数也为a%,而等体积混合时则为c%,则a、b、c之间的大小关系为( )。
A.a>b>c B.b>a>c C.c>a>b D.不能比较
[解析]选B。两种质量分数不同的溶液等质量混合时,混合物中溶质质量分数等于混合前两溶液溶质质量分数之和的一半;等体积相混时,若溶液的密度比水的小,则混合物中溶质质量分数小于混合前两溶液溶质质量分数之和的一半,若溶液的密度比水的大,则混合物中溶质质量分数大于混合前两溶液溶质质量分数之和的一半,硫酸的密度比水的大,乙醇的密度比水的小,所以b>a>c。
13.(2010·安阳模拟)下图为用某浓度的NaOH溶液(Y),滴定10mL某浓度的HCl溶液(X)的图像,据此推断NaOH溶液和HCl溶液的物质的量浓度是( )。
|
|
A |
B |
C |
D |
|
X溶液/mol·L-1 |
0.150 |
0.090 |
0.080 |
0.040 |
|
Y溶液/mol·L-1 |
0.050 |
0.030 |
0.160 |
0.120 |
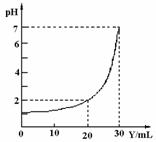
[解析]选B。假设NaOH溶液和HCl溶液的物质的量浓度分别为x和y,由图可知,当加入20mLNaOH溶液时,溶液的pH=2,此时c(H+)=10-2mol/L,则有:0.01L·y-0.02L·x=(0.01L+0.02L)×10-2mol/L;当加入30mLNaOH溶液时,溶液的pH=7,此时恰好完全中和,则有:0.01L·y=0.03L·x,解得:x=0.03mol/L,y=0.09mol/L。
12.(2010·南阳模拟)若以w1和w2分别表示浓度为c1 mol/L和c2 mol/L硫酸的质量分数,已知2w1=w2,则下列推断正确的是(硫酸的密度比纯水的大)( )。
A.2c1=c2 B.2c2=c1 C.c2>2c1 D.c1<c2<2c1
[解析]选C。因为硫酸的密度比纯水的大,其浓度越大,密度也越大,w2>w1,所以ρ2>ρ1,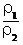 <1,根据c=
<1,根据c=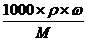 可得:
可得: =
=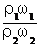 =
= <
<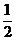 ,即c2>2c1。
,即c2>2c1。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com