
例1 已知角 的终边经过点P(2,-3)(如图),求
的终边经过点P(2,-3)(如图),求 的六个三角函数值.
的六个三角函数值.
解:∵x=2,y=-3
∴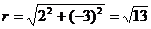
于是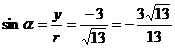
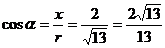
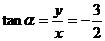
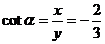
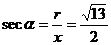
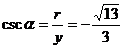
例2求下列各角的六个三角函数值.
(1)0
(2)π (3)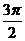 (4)
(4) 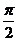
解:(1)因为当 =0时,x=r,y=0,所以
=0时,x=r,y=0,所以
sin0=0 cos0=1 tan0=0 cot0不存在
sec0=1 csc0不存在
(2)因为当 =π时,x=-r,y=0,所以
=π时,x=-r,y=0,所以
sinπ=0 cosπ=-1 tanπ=0 cotπ不存在
secπ=-1 cscπ不存在
(3)因为当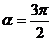 时,x=0,y=-r,所以
时,x=0,y=-r,所以

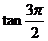 不存在
不存在 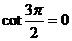
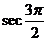 不存在
不存在 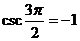
(4)当a=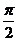 时
时  ,所以
,所以
sin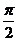 =1 cos
=1 cos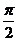 =0 tan
=0 tan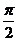 不存在 cot
不存在 cot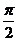 =0
=0
sec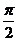 不存在 csc
不存在 csc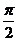 =1
=1
例3填表:
|
a |
0° |
30° |
45° |
60° |
90° |
120° |
135° |
150° |
180° |
270° |
360° |
|
弧度 |
|
|
|
|
|
|
|
|
|
|
|
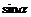 |
|
|
|
|
|
|
|
|
|
|
|
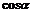 |
|
|
|
|
|
|
|
|
|
|
|
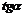 |
|
|
|
|
|
|
|
|
|
|
|
 |
|
|
|
|
|
|
|
|
|
|
|
 |
|
|
|
|
|
|
|
|
|
|
|
 |
|
|
|
|
|
|
|
|
|
|
|
例4 ⑴ 已知角a的终边经过P(4,-3),求2sina+cosa的值
⑵已知角a的终边经过P(4a,-3a),(a¹0)求2sina+cosa的值
解:⑴由定义 :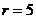 sina=-
sina=-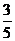 cosa=
cosa=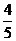 ∴2sina+cosa=-
∴2sina+cosa=-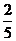
⑵若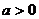
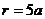 则sina=-
则sina=-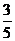 cosa=
cosa=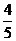 ∴2sina+cosa=-
∴2sina+cosa=-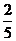
若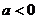
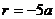 则sina=
则sina=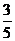 cosa=-
cosa=-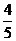 ∴2sina+cosa=
∴2sina+cosa=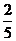
例5 求函数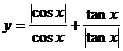 的值域
的值域
解: 定义域:cosx¹0 ∴x的终边不在x轴上
又∵tanx¹0 ∴x的终边不在y轴上
当x是第Ⅰ象限角时, cosx=|cosx|
tanx=|tanx| ∴y=2
cosx=|cosx|
tanx=|tanx| ∴y=2
当x是第Ⅱ象限角时,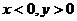 |cosx|=-cosx |tanx|=-tanx ∴y=-2
|cosx|=-cosx |tanx|=-tanx ∴y=-2
当x是第Ⅲ象限角时, 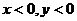 |cosx|=-cosx |tanx|=tanx ∴y=0
|cosx|=-cosx |tanx|=tanx ∴y=0
当x是第Ⅳ象限角时, 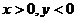 |cosx|=cosx |tanx|=-tanx ∴y=0
|cosx|=cosx |tanx|=-tanx ∴y=0
4.注意:
(1)以后我们在平面直角坐标系内研究角的问题,其顶点都在原点,始边都与x轴的非负半轴重合.
(2)OP是角 的终边,至于是转了几圈,按什么方向旋转的不清楚,也只有这样,才能说明角
的终边,至于是转了几圈,按什么方向旋转的不清楚,也只有这样,才能说明角 是任意的.
是任意的.
(3)sin 是个整体符号,不能认为是“sin”与“
是个整体符号,不能认为是“sin”与“ ”的积.其余五个符号也是这样.
”的积.其余五个符号也是这样.
(4)定义中只说怎样的比值叫做 的什么函数,并没有说
的什么函数,并没有说 的终边在什么位置(终边在坐标轴上的除外),即函数的定义与
的终边在什么位置(终边在坐标轴上的除外),即函数的定义与 的终边位置无关.
的终边位置无关.
(5)比值只与角的大小有关.
(6)任意角的三角函数的定义与锐角三角函数的定义的联系与区别:
任意角的三角函数就包含锐角三角函数,实质上锐角三角函数的定义与任意角的三角函数的定义是一致的,锐角三角函数是任意角三角函数的一种特例. 所不同的是,锐角三角函数是以边的比来定义的,任意角的三角函数是以坐标与距离、坐标与坐标、距离与坐标的比来定义的. 即正弦函数值是纵坐标比距离,余弦函数值是横坐标比距离, 正切函数值是纵坐标比横坐标,余切函数值是横坐标比纵坐标,正割函数值是距离比横坐标,余割函数值是距离比纵坐标.
(7)为了便于记忆,我们可以利用两种三角函数定义的一致性,将直角三角形置于平面直角坐标系的第一象限,使一锐角顶点与原点重合,一直角边与x轴的非负半轴重合,利用我们熟悉的锐角三角函数类比记忆.
3.突出探究的几个问题:
①角是“任意角”,当b=2kp+a(kÎZ)时,b与a的同名三角函数值应该是相等的,即凡是终边相同的角的三角函数值相等
②实际上,如果终边在坐标轴上,上述定义同样适用
③三角函数是以“比值”为函数值的函数
④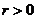 而x,y的正负是随象限的变化而不同,故三角函数的符号应由象限确定.
而x,y的正负是随象限的变化而不同,故三角函数的符号应由象限确定.
⑤定义域:对于正弦函数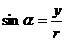 ,因为r>0,所以
,因为r>0,所以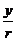 恒有意义,即
恒有意义,即 取任意实数,
取任意实数,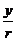 恒有意义,也就是说sin
恒有意义,也就是说sin 恒有意义,所以正弦函数的定义域是R;类似地可写出余弦函数的定义域;对于正切函数
恒有意义,所以正弦函数的定义域是R;类似地可写出余弦函数的定义域;对于正切函数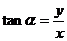 ,因为x=0时,
,因为x=0时,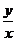 无意义,即tan
无意义,即tan 无意义,又当且仅当角
无意义,又当且仅当角 的终边落在纵轴上时,才有x=0,所以当
的终边落在纵轴上时,才有x=0,所以当 的终边不在纵轴上时,
的终边不在纵轴上时,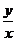 恒有意义,即tan
恒有意义,即tan 恒有意义,所以正切函数的定义域是
恒有意义,所以正切函数的定义域是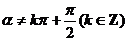 .从而有
.从而有
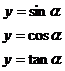
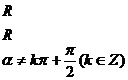
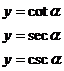
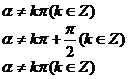
2.比值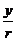 叫做
叫做 的正弦 记作:
的正弦 记作: 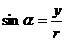
 比值
比值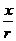 叫做
叫做 的余弦 记作:
的余弦 记作: 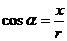
比值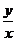 叫做
叫做 的正切 记作:
的正切 记作: 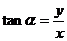
比值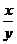 叫做
叫做 的余切 记作:
的余切 记作: 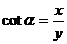
比值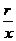 叫做
叫做 的正割 记作:
的正割 记作: 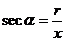
比值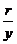 叫做
叫做 的余割 记作:
的余割 记作: 
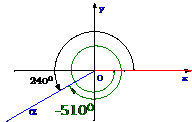 根据相似三角形的知识,对于终边不在坐标轴上确定的角
根据相似三角形的知识,对于终边不在坐标轴上确定的角 ,上述六个比值都不会随P点在
,上述六个比值都不会随P点在 的终边上的位置的改变而改变.当角
的终边上的位置的改变而改变.当角 的终边在纵轴上时,即
的终边在纵轴上时,即 时,终边上任意一点P的横坐标x都为0,所以tan
时,终边上任意一点P的横坐标x都为0,所以tan 、sec
、sec 无意义;当角
无意义;当角 的终边在横轴上时,即
的终边在横轴上时,即 =kπ(k∈Z)时,终边上任意一点P的纵坐标y都为0,所以cot
=kπ(k∈Z)时,终边上任意一点P的纵坐标y都为0,所以cot 、csc
、csc 无意义,除此之外,对于确定的角
无意义,除此之外,对于确定的角 ,上面的六个比值都是惟一确定的实数,这就是说,正弦、余弦、正切、余切、正割、余割都是以角为自变量,以比值为函数值的函数.
,上面的六个比值都是惟一确定的实数,这就是说,正弦、余弦、正切、余切、正割、余割都是以角为自变量,以比值为函数值的函数.
以上六种函数,统称为三角函数.
对于锐角三角函数,我们是在直角三角形中定义的,今天,对于任意角的三角函数,我们利用平面直角坐标系来进行研究.
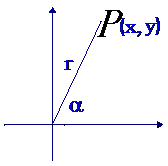
1.设 是一个任意角,在
是一个任意角,在 的终边上任取(异于原点的)一点P(x,y)
的终边上任取(异于原点的)一点P(x,y)
则P与原点的距离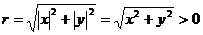

2.前面我们对角的概念进行了扩充,并学习了弧度制,知道角的集合与实数集是一一对应的,在这个基础上,今天我们来研究任意角的三角函数.
1.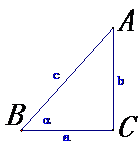 在初中我们学习了锐角三角函数,它是以锐角为自变量,边的比值为函数值的三角函数:
在初中我们学习了锐角三角函数,它是以锐角为自变量,边的比值为函数值的三角函数:
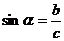
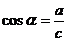
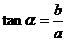
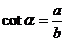
24.(2010·南平模拟)人体血液里Ca2+离子的浓度一般采用g/cm3来表示。抽取一定体积
的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将
此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定
血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓
度:
[配制KMnO4标准溶液]下图是配制50mLKMnO4标准溶液的过程示意图。
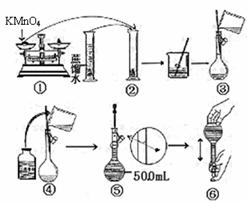
(1)请你观察图示判断其中不正确的操作有(填序号)____________;
(2)其中确定50mL溶液体积的容器是(填名称)__________________;
(3)如果按照图示的操作所配制的溶液进行实验,在其他操作均正确的情况下,所测得的实验结果将____________(填偏大或偏小)
[测定血液样品中Ca2+的浓度]抽取血样20.00mL,经过上述处理后得到草酸,再用0.020mol/LKMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液。
(4)已知草酸跟KMnO4反应的离子方程式为:
2MnO4―+5H2C2O4+6H+=2Mnx++10CO2↑+8H2O
则式中的 ________________。
________________。
(5)滴定时,根据现象_____________________________,即可确定反应达到终点。
(6)经过计算,血液样品中Ca2+离子的浓度为________mg/cm3。
[解析](1)量筒不能用于配制溶液,视线应该与凹液面的最低点相平读数,所以②⑤操作错误;(2)配制50mL一定物质的量浓度KMnO4标准溶液需要50mL的容量瓶;(3)仰视读数时,定容时,所加的水超过刻度线,体积偏大,所以浓度偏小。(4)~(6)血样处理过程中发生反应的离子方程式依次是:①Ca2++C2O42-=CaC2O4↓;②CaC2O4+2H+=Ca2++H2C2O4;③2MnO4―+5H2C2O4+6H+=2Mnx++10CO2↑+8H2O,由此可得如下关系式:5Ca2+-5CaC2O4-5H2C2O4-2MnO4―,所以n(Ca2+)=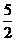 n(MnO4-)=
n(MnO4-)=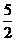 ×0.0120L
×0.0120L
×0.020mol·L-1=6.0×10-4mol,血液样品中Ca2+的浓度=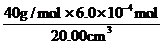 =1.2×10-3g/cm3=1.2mg/cm3。对于反应③根据电荷守恒,2×(-1)+6×(+1)=2×(+x),所以x=2。草酸溶液无色,当反应正好完全进行的时候,多加一滴KMnO4溶液,溶液恰好由无色变为紫红色。
=1.2×10-3g/cm3=1.2mg/cm3。对于反应③根据电荷守恒,2×(-1)+6×(+1)=2×(+x),所以x=2。草酸溶液无色,当反应正好完全进行的时候,多加一滴KMnO4溶液,溶液恰好由无色变为紫红色。
[答案](1)②⑤ (2)容量瓶 (3)偏小
(4)2 (5)溶液由无色变为紫红色 (6)1.2
|
|
23.(2010·石家庄模拟)用质量分数为36.5%的浓盐酸(密度为1.16g/cm3)配制成1mol/L的稀盐酸。现实验室仅需要这种盐酸220mL。试回答下列问题:
(1)配制稀盐酸时,应选用容量为______mL的容量瓶;
(2)经计算需要______mL浓盐酸,在量取时宜选用下列量筒中的______。
A.5mL B.10mL C.25mL D.50mL
(3)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸其温度与室温一致后,沿玻璃棒注入250mL容量瓶中。
②往容量瓶中小心加蒸馏水至液面接近环形标线2-3 cm处,改用胶头滴管加蒸馏水,使溶液的凹面底部与瓶颈的环形标线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶
上述操作中,正确的顺序是(填序号)____________。
(4)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度是______(填“偏高”、“偏低”、“无影响”)。若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则配制的稀盐酸浓度是____________(填“偏高”、“偏低”、“无影响”)。
[解析](1)由于实验室里没有220mL容量瓶,所以必须选用250mL容量瓶,先配制250mL溶液,再从其中取出220mL即可。(2)c(HCl)=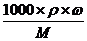 =
=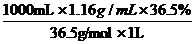 =11.6mol/L。加水稀释前后HCl的物质的量不变,所以11.6mol/L·V(HCl)=250mL×1mol/L,解得V(HCl)=21.6mL,应该选择25mL的量筒量取。(3)配制一定物质的量浓度的溶液基本步骤为:计算→称量或量取→溶解→冷却后转移洗涤→振荡后定容→倒转摇匀,所以正确的顺序是③①④②。(4)用刚刚洗涤洁净的量筒来量取浓盐酸,量取的盐酸被稀释了,其物质的量比实际偏小,所配制溶液的浓度偏低;若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则一部分溶质损失,所配制溶液的浓度偏低。
=11.6mol/L。加水稀释前后HCl的物质的量不变,所以11.6mol/L·V(HCl)=250mL×1mol/L,解得V(HCl)=21.6mL,应该选择25mL的量筒量取。(3)配制一定物质的量浓度的溶液基本步骤为:计算→称量或量取→溶解→冷却后转移洗涤→振荡后定容→倒转摇匀,所以正确的顺序是③①④②。(4)用刚刚洗涤洁净的量筒来量取浓盐酸,量取的盐酸被稀释了,其物质的量比实际偏小,所配制溶液的浓度偏低;若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则一部分溶质损失,所配制溶液的浓度偏低。
[答案](1)250 (2)21.6 C (3)③①④② (4)偏低;偏低
22.(2010·兴义模拟)Ba2+是一种重金属离子,有一环境监测小组欲利用Na2S2O3、KI、K2Cr2O7等试剂测定某工厂废水中Ba2+的浓度。
(1)现需配制250mL 0.100mol·L-1标准Na2S2O3溶液,所需要的玻璃仪器除量筒、250mL容量瓶、玻璃棒外,还需要_________________________。
(2)需准确称取Na2S2O3固体的质量为_______________g。
(3)另取废水50.00mL,控制适当的酸度加人足量的K2Cr2O7溶液,得BaCrO4沉淀;沉淀经洗涤.过滤后,用适量的稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加过量KI溶液反应,反应液中再滴加上述Na2S2O3溶液,反应完全时,消耗Na2S2O2溶液36.00mL。已知有关的离子方程式为:
①Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O;
②I2+2S2O32-=2I-+S4O62-。
试计算该工厂废水中Ba2+的物质的量浓度。
[解析](1)配制0.100mol·L-1的Na2S2O3溶液时,将Na2S2O3固体在烧杯中溶解,将溶液沿玻璃棒转移到250mL容量瓶中,用胶头滴管定容,所以必须使用到这三种玻璃仪器。
(2)m(Na2S2O3)=0.250L×0.100mol·L-1×158g·mol-1=3.95g。
(3)设Ba2+的物质的量为x,则有:
Ba2+~BaCrO2~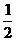 Cr2O72-~
Cr2O72-~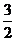 I2~3S2O32-
I2~3S2O32-
1mol 3mol
xmol 36.00×0.100×10-3mol
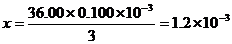 mol
mol
所以c(Ba2+)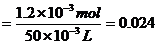 mol·L-1
mol·L-1
[答案](1)胶头滴管 (2)3.95 (3)0.024mol·L-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com