
2. 判断下列数列是否有极限,若有,写出极限
(1)1,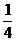 ,
,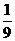 ,…,
,…,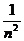 ,… ; (2)7,7,7,…,7,…;
,… ; (2)7,7,7,…,7,…;
(3)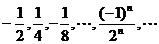 ; (4)2,4,6,8,…,2n,…;
; (4)2,4,6,8,…,2n,…;
(5)0.1,0.01,0.001,…, ,…; (6)0,
,…; (6)0,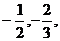 …,
…,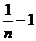 ,…;
,…;
(7)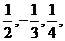 …,
…,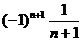 ,…; (8)
,…; (8)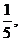
 …,
…,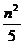 ,…;
,…;
(9)-2, 0,-2,…,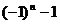 ,…,
,…,
答案:⑴0 ⑵7 ⑶0 ⑷不存在 ⑸0 ⑹-1 ⑺0 ⑻不存在 ⑼不存在.
1.下列命题正确的是( )
①数列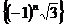 没有极限 ②数列
没有极限 ②数列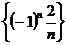 的极限为0 ③数列
的极限为0 ③数列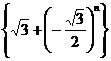 的极限为
的极限为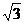 ④ 数列
④ 数列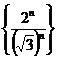 没有极限
没有极限
A ①② B ②③④ C ①②③ D ①②③④ 
答案:D
例1判断下列数列是否有极限,若有,写出极限;若没有,说明理由
(1)1,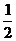 ,
,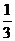 ,…,
,…,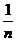 ,… ;
,… ;
(2)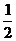 ,
,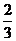 ,
, ,…,
,…,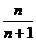 ,…;
,…;
(3)-2,-2,-2,…,-2,…;
(4)-0.1,0.01,-0.001,…,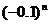 ,…;
,…;
(5)-1,1,-1,…,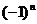 ,…;
,…;
解:(1)1,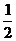 ,
,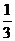 ,…,
,…,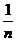 ,… 的项随n的增大而减小,且当n无限增大时,
,… 的项随n的增大而减小,且当n无限增大时,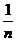 无限地趋近于0.因此,数列{
无限地趋近于0.因此,数列{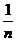 }的极限是0,即
}的极限是0,即
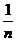 =0.
=0.
(2)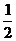 ,
,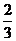 ,
, ,…,
,…,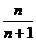 ,…的项随n的增大而增大,且当n无限增大时,
,…的项随n的增大而增大,且当n无限增大时,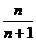 无限地趋近于1.因此,数列{
无限地趋近于1.因此,数列{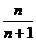 }的极限是1,即
}的极限是1,即
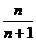 =1.
=1.
(3)-2,-2,-2,…,-2,…的项随n的增大都不变,且当n无限增大时,无限地趋近于-2.因此,数列{-2}的极限是-2,即 (-2)=-2.
(-2)=-2.
(4)-0.1,0.01,-0.001,…,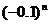 ,…的项随n的增大而绝对值在减小,且当n无限增大时,
,…的项随n的增大而绝对值在减小,且当n无限增大时,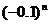 无限地趋近于0.因此,数列{
无限地趋近于0.因此,数列{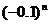 }的极限是0,即
}的极限是0,即
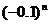 =0.
=0.
(5)-1,1,-1,…,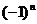 ,…的项随n的增大而在两个值-1与1上变化,且当n无限增大时,
,…的项随n的增大而在两个值-1与1上变化,且当n无限增大时,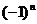 不能无限地趋近于同一个定值.因此,数列{
不能无限地趋近于同一个定值.因此,数列{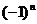 }无极限
}无极限 
2.几个重要极限:
(1)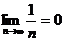 (2)
(2)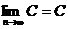 (C是常数)
(C是常数)
(3)无穷等比数列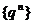 (
(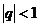 )的极限是0,即
)的极限是0,即 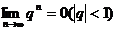

1.数列极限的定义:
一般地,如果当项数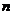 无限增大时,无穷数列
无限增大时,无穷数列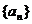 的项
的项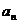 无限趋近于某个常数
无限趋近于某个常数 (即
(即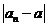 无限趋近于0),那么就说数列
无限趋近于0),那么就说数列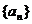 以
以 为极限,或者说
为极限,或者说 是数列
是数列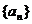 的极限.记作
的极限.记作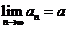 ,读作“当
,读作“当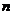 趋向于无穷大时,
趋向于无穷大时,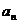 的极限等于
的极限等于 ”
”
“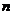
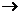 ∞”表示“
∞”表示“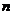 趋向于无穷大”,即
趋向于无穷大”,即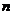 无限增大的意思
无限增大的意思
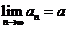 有时也记作:当
有时也记作:当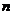
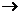 ∞时,
∞时,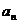
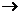
 .
.
理解:数列的极限的直观描述方式的定义,只是对数列变化趋势的定性说明,而不是定量化的定义.“随着项数n的无限增大,数列的项an无限地趋近于某个常数a”的意义有两个方面:一方面,数列的项an趋近于a是在无限过程中进行的,即随着n的增大an越来越接近于a;另一方面,an不是一般地趋近于a,而是“无限”地趋近于a,即|an-a|随n的增大而无限地趋近于0.
2. 观察下列数列,随n变化时,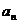 是否趋向于某一个常数:
是否趋向于某一个常数:
(1)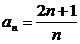 ; (2)
; (2)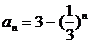 ; (3)an=4·(-1)n-1; (4)an=2n;
; (3)an=4·(-1)n-1; (4)an=2n;
(5)an=3; (6)an=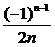 ; (7)an=(
; (7)an=(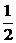 )n; (8)an=6+
)n; (8)an=6+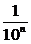
1.战国时代哲学家庄周所著的《庄子·天下篇》引用过一句话:“一尺之棰,日取其半,万世不竭 ”也就是说一根长为一尺的木棒,每天截去一半,这样的过程可以无限制地进行下去
”也就是说一根长为一尺的木棒,每天截去一半,这样的过程可以无限制地进行下去 (1)可以求出第
(1)可以求出第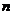 天剩余的木棒长度
天剩余的木棒长度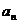 =
=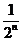 (尺);(2)前
(尺);(2)前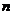 天截下的木棒的总长度
天截下的木棒的总长度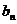 =1-
=1-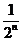 (尺)
(尺) 分析变化趋势.
分析变化趋势.
13、(2010·河北石家庄模拟) 下列五个化学方程式(X、Y、Z均为正值):
①C2H2(g)+H2(g)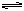 C2H4(g)
C2H4(g)
②CH4(g)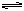 H2(g)+
H2(g)+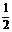 C2H4(g)
C2H4(g)
③C(s)+2H2(g)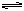 CH4(g); △H= -X kJ·mol-1
CH4(g); △H= -X kJ·mol-1
④C(s)+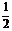 H2(g)
H2(g)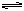
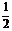 C2H2(g); △H= -Y kJ·mol-1
C2H2(g); △H= -Y kJ·mol-1
⑤C(s)+H2(g)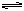
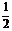 C2H4(g); △H= -ZkJ·mol-1
C2H4(g); △H= -ZkJ·mol-1
当温度下降时①式平衡向右移动,②式平衡向左移动。据此判定③-⑤式中关于X、Y、Z的大小顺序排列正确的是:( )
A.X>Y>Z B.X>Z>Y C.Y>X>Z D.Y>Z>X
[答案]B
()
12、(2010·台州模拟)已知:①2H2(g) + O2(g) = 2H2O(l) △H =-571.6 kJ·mol-1
②H+(aq) + OH-(aq) = H2O(l) △H = -57.3kJ·mol-1。
下列说法中错误的是( )
A.①式表示25℃,101 kPa时,2 mol H2和1 mol O2完全燃烧生成2 mol H2O(l)放热571.6 kJ
B.2H2(g) + O2(g) = 2H2O(g)中△H大于-571.6 kJ·mol-1
C.将含1 mol NaOH的水溶液与50 g 98%的硫酸溶液混合后放出的热量为57.3 kJ
D.将含1 mol NaOH的稀溶液与含1 mol CH3COOH的稀溶液混合后放出的热量小于57.3 kJ
[答案]C。
11、(2010·苏州模拟)1840年,俄国化学家盖斯(G.H.Hess)从大量的实验事实中总结出了一条规律:化学反应不管是一步完成还是分几步完成,其反应热是相同的,即盖斯定律。盖斯定律在生产和科学研究中有很重要的意义,有些反应的反应热虽然无法直接测得,但可以利用盖斯定律间接计算求得。已知3.6 g碳在6.4 g的氧气中燃烧,至反应物耗尽,并放出X kJ热量。已知单质碳的燃烧热为Y kJ・mol-1,则1 mol C与O2反应生成CO的反应热ΔH为 ( )
A.-Y kJ・mol-1 B.-(10X-Y)kJ・mol-1
C.-(5X-0.5Y) kJ・mol-1 D.+(10X-Y) kJ・mol-1
[解析]选C。由3.6 g C与6.4 g O2完全反应,可知生成CO2与CO之比为1∶2。设3.6 g C按此方式反应,则生成1 mol CO2和2 mol CO,C单质燃烧热为Y kJ・mol-1,1 mol C与O2生成CO的反应热为:
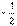 (10X-Y)kJ・mol-1,即-(5X-0.5Y)kJ・mol-1,C正确。
(10X-Y)kJ・mol-1,即-(5X-0.5Y)kJ・mol-1,C正确。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com