
7. 某校学生课外活动小组为测定Na元素的相对原
某校学生课外活动小组为测定Na元素的相对原
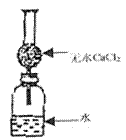
子质量,设计的装置如右图,该装置(包括水和干燥剂)
的总质量为ag,从实验室取出bg(不足量)的钠放入
水中,塞紧瓶塞,完全反应后再称量此装置的总质量为
cg,试回答:
(1)实验室取用一小块钠,需要的用品有_________________________
(2)此干燥管的作用是:____________,若不用此干燥管,则测出相对原子质量会比
实际相对原子质量________(填“偏大”、“偏小”或“不变”,下同),若此
块中极少量被氧化,则会_____________
(3)有甲同学建议在图中干燥管上再连一同样干燥管(设此干燥管质量为mg),其目
的是:__________________若所增加干燥管待完全反应后质量变为m1g,则依甲
学建议,计算钠的相对原子质量的表达式为_______________。
(4)有乙同学为避免由于行动不够迅速产生偏差,又建议在集气瓶中再加入一定量煤
油,其目的是:____________
(5)若生成的NaOH溶液恰好使100mL C molL-1硫酸铝溶液中Al3+沉淀完全,则
C=_______________(以a、b、c的表达式表示)。
6.海水占地球总储水量的97.2%,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源。
(1)海水中存在大量的氯化钠,氯化钠中的金属元素位于元素周期表第______族。
(2)目前,国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经冷却而得高纯度淡水。由此可判断蒸馏法是________(填:物理变化或化学变化)。
(3)工业上利用电解饱和食盐水可制得重要化工产品。反应式为:食盐十H2O→NaOH+H2↑+Cl2↑(未配平),该反应中食盐的化学式是____________________;利用电解所得气体制36.5%的浓盐酸1000 t,最少需消耗食盐_________t。(可能需要的相对原子质量:Na 23 Cl 35.5 H 1 O 16)
(4)近年来,有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法。该方法流程如下:
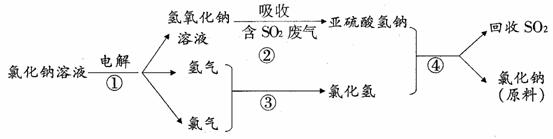
请写出②④的化学反应方程式:_____________________、________________________。
(5)上述亚硫酸氢钠与甲醛经过一定反应可以合成俗称“吊白块(雕白粉)”的物质,因该物质对人体有害,不能用于食品漂白。“吊白块”结构简式为:HOCH2SO3Na,根据其结构特点,“吊白块”能发生的反应有________________。(填字母)
A.皂化反应 B.聚合反应 C.与金属钠反应 D.氧化反应
5.将a摩钠和a摩铝一同放入m克水(足量)中,所得溶液的密度为d克/毫升,该溶液的质量分数为
A.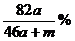 B.
B.
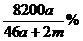 C.
C.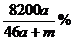 D.
D.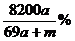
4、 “绿色化学实验”进课堂,某化学教师为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验。实验操作:钠与氯气反应的装置可作如下图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火
燃烧,生成大量白烟。以下叙述错误的是 ( )
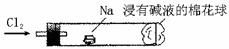 A.反应生成的大量白烟是氯化钠晶体
A.反应生成的大量白烟是氯化钠晶体
B.玻璃管尾部塞一团浸有NaOH溶液的棉球是用 于吸收过量的氯气,以免其污染空气
C.钠着火燃烧产生苍白色火焰
D.若在棉球外沿滴一滴淀粉碘化钾溶液,可据其颜色变化判断氯气是否被碱液完全吸收
2.目前人们正在研究开发一种高能电池--钠硫原电池,它是以熔融的钠硫为电极,以Na+导电的β″-Al2O3陶瓷作固体电解质,反应式为:
A.放电时,钠作正极,硫作阴极 B.放电时,钠极发生还原反应 C.充电时,钠极与外接电源正极相连 D.充电时,阳极发生的反应为 Sx2--2e-=xS 3、下列离子方程式正确的是 ( )
A、Na与水的反应:Na+2H2O==Na++2OH-+H2↑
B、碳酸氢钠溶液中加入过量氢氧化钠:Ca2++2HCO3-+2OH-==CaCO3+2H2O+CO32-
C、过量CO2通入氢氧化钠溶液中:CO2+2OH-==CO32-+H2O
D、将Na2O2溶于H218O中:2Na2O2 + H218O==4Na++4OH-+18O2
1.所含的质子总数和电子总数分别与Na+的质子总数和电子总数相同的是 ( )
A Mg2+ B LiF C NH4+ D H2O
4、保存:金属钠必须 保存,通常保存在 里。 (能或不能)保存在CCl4里
例6、下列有关钠的叙述中错误的是( )
A、钠的还原性很强,可以用来冶炼金属钛、锆、铌等。
B、钠的化学性质非常活泼,钠元素只能以化合态存在于自然界
C、钠是一种灰黑色的固体 D、钠的质地软,可用小刀切割
[针对性训练]
3、用途:
2、存在:自然界里的元素有二种存在形态:一种是单质的形态,叫 态;一种以化合物的形态存在,叫 态。钠只以 态存在,如自然界中的 、 、 、 等。
1、制备:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com