
37.(10分)恒温下,将amolN2与bmolH2的混合气体通入一个固定容积的密闭容器中,发生
如下反应:N2(g) + 3H2(g)  2NH3(g);反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的含量为25%(体积分数)。则:
2NH3(g);反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的含量为25%(体积分数)。则:
(1)若反应进行到某时刻t时,n(N2)=13mol,n(NH3)=6mol,则a的值为 ;
(2)原混合气体中,a∶b= ;
(3)原混合气体与平衡混合气体的总物质的量之比,n(始):n(平)= ;
(4)若把容器体积减小一半,则正反应速率变 ,逆反应速率变 。
(填“大”、“小”或“不变”)
36.(4分)将铜片和锌片用导线连接后同时插入200mL硫酸铜溶液中,相当长时间后将铜片
和锌片取出、烘干、称量,质量比反应前少0.1g。则
(1)此过程中有 个电子通过了导线;
(2)原硫酸铜溶液的物质的量浓度为 mol/L。
35.(9分)已知A、B、C、D、E均为短周期元素,原子序数按A、E、B、C、D的顺序依次递增。A元素原子形成的离子就是一个质子;C原子的最外层电子数是次外层的3倍;C和D可形成两种固体化合物,其中一种为淡黄色固体;B和C可形成多种气态化合物;由A、B、C三种元素可形成离子化合物X,X中A、B、C元素原子的物质的量之比为A∶B∶C=4∶2∶3;E原子最外层电子数是内层电子数的2倍。回答下列问题:
(1)请写出元素符号: B 、C 、D 、E ;
(2)写出C和D形成的淡黄色固体化合物的电子式 ;
(3)化合物X的名称为: ;
(4)由B、C元素组成元素原子质量比为B∶C=7∶12的化合物的化学式 ;
(5)由A、B、C、E四种元素按原子个数比为5∶1∶3∶1组成的化合物的水溶液与足量的NaOH溶液在加热时发生反应的离子方程式为 。
34.(4分)(1)请写出氢氧燃料电池以KOH溶液为电解质溶液时正极的电极反应式:
;
(2)请写出甲烷燃料电池以KOH溶液为电解质溶液时负极的电极反应式:
。
33.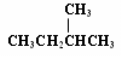 (4分)有下列各组微粒或物质:
(4分)有下列各组微粒或物质:

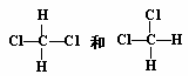 A.
A. 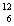 C和
C和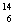 C
B.CH3CH2CH2CH3和
C
B.CH3CH2CH2CH3和
C. D.
(1)__________组两种微粒互为同位素;
(2)__________组两种物质属于同系物;
(3)__________组两种物质互为同分异构体;
(4)__________组两种物质是同一物质。
32.(2分)10g重水中含有 个中子。同物质的量的H2O、D2O、T2O三种水的质量比为 。
31.(3分)实验室制乙烯的化学方程式为: ,
浓硫酸的作用为: 。
30.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:

下列描述正确的是
A.反应开始到10s,用Z表示的反应速率为0.158 mol·L-1·s-1
B.反应开始到10s,X的物质的量浓度减少了0.79 mol·L-1
C.反应开始到10s,Y的转化率为79.0%
D.反应的化学方程式为:X(g) + Y(g) Z(g)
Z(g)
Ⅱ卷(共40分)
29.把2.5 mol A和2.5 mol B混合通入容积为1L的密闭容器里发生如下反应:
3A(g) + B(g) x C(g)
+ 2D(g),容器里的压强逐渐降低,经5s后保持不变。在此5s内
x C(g)
+ 2D(g),容器里的压强逐渐降低,经5s后保持不变。在此5s内
C的平均反应速率为0.1 mol·L-1·s-1。则下列的说法中正确的是
A.达平衡时,A的物质的量浓度2.0 mol/L
B.达平衡时,B的转化率20%
C.此5s内D的平均反应速率为0.2 mol·L-1·min-1
D.x ≥ 3
28.设NA为阿伏加德罗常数,下列叙述中正确的是
A.常温下11.2 L的甲烷气体含有甲烷分子数为0.5 NA个
B.14g乙烯和丙烯的混合物中总原子数为3 NA个
C.0.1 mol/L的氢氧化钠溶液中含钠离子数为0.1 NA个
D.5.6 g铁与足量的稀硫酸反应失去电子数为0.3 NA个
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com