
4、辨析:改革开放是决定当代中国命运的关键抉择,所以要坚持以改革开放为中心。
答:(1)改革开放是决定当代中国命运的关键抉择,是发展中国特色社会主义、实现中华民族伟大复兴的必由之路;只有社会主义才能救中国,只有改革开放才能发展中国、发展社会主义发展马克思主义。(2)必须坚持以经济建设为中心,只有坚持以经济建设为中心,大力发展生产力,才能从根本上巩固和发展社会主义制度,才能不断满足人民日益满足增长的物质文化需要,才能推动社会的全面进步。(3)改革是动力是发展经济的必由之路。坚持以经济为中心必须大力推行改革开放。
3.材料:弹指挥间、沧桑巨变,60年前,中华人民共和国宣告成立,开启了中国历史的新纪元。在中国共产党的领导下,亿万人民艰苦创业,努力探索中国特色社会主义的发展道路,在改革开放和现代化建设的历程中,创造了一个又一个奇迹,实现着强国富民、民族复兴的百年梦想。当今之中国,到处充满勃勃生机,各项事业蒸蒸日上,中国特色社会主义事业显示出强大的生命力。改革开放,从根本上,使中国一步步走向繁荣昌盛,华夏儿女们安居乐业。
(1)国特色社会主义的发展道路,是从什么开始的?
(2)祖国发展、繁荣、富强的60年伟大历程告诉我们什么?
(3)为什么改革开放,能使中国一步步走向繁荣昌盛?
答:(1)从中共十一届三中全会开始的。
(2)发展是解决中国一切问题的关键所在;改革开放是强国之路;把马克思主义基本原理同中国具体实际相结合,继续解放思想;坚持党的领导,是我们取得辉煌成就的最根本保证
(3)改革开放能够解放和发展社会生产力。
2.60年我国发生巨变的原因
60年来,我们之所以能够经受一次次严峻考验,取得一个又一个辉煌成就,归结起来就是开辟了中国特色社会主义道路,形成了中国特色社会主义理论体系。坚持了中国共产党的领导,保持了中国共产党的先进性。坚持党的基本路线,以经济建设为中心,坚持四项基本原则,坚持改革开放,坚持科教兴国和人才强国战略,推动科学发展,促进社会和谐;实行以公有制经济为主体多种所有制经济共同发展的基本经济制度,实行以按劳分配为主体的分配制度,实现全体人民的共同富裕;全国人民的艰苦奋斗等。
1、建国60年来,中国共产党领导全国各族人们实施改革开放和实行社会主义市场经济。给国家、社会带来那些巨大的变化?
答:改革开放以来,我国综合国力大幅度跃升,人民得到的实惠越来越多,我国社会长期保持安定团结,政通人和,成为世界上发展追快,变化最大的国家之一。我国社会主义制度显示了强大的生命力,中国国际地位日益提高,民族凝聚力极大增强,在国际舞台上发挥着越来越重要的作用,一个和平、合作、负责任的中国形象已经为国际社会所公认。
现代化建设取得了成就举例:教育事业不断发展,人民的科学文化水平有了一定的提高。科技事业取得了巨大的发展,我国建立了独立的完整的工业体系,人民生活总体上达到了小康水平。具体实例:神舟系列飞船及嫦娥一号卫星的发射成功。举办2008年奥运会。
身边的变化列举:房屋建筑方面有毛草房、平房到楼房。并由狭窄发展到宽敞、明亮。电信事业方面由写信到邮局打电话,到手机互联网、电子邮件交流。
16.在标准状况下进行甲、乙、丙三组实验,三组各取30 mL同浓度的盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据列表如下:
|
实验序号 |
甲 |
乙 |
丙 |
|
合金质量(mg) |
255 |
385 |
459 |
|
生成气体体积(mL) |
280 |
336 |
336 |
(1)甲组实验中,盐酸 (填“过量”“适量”或“不足量”),理由是 。乙组实验中,盐酸 (填“过量”“适量”或“不足量”),理由是 。要算出盐酸的物质的量浓度,题中可作计算依据的数据是 ,求得的盐酸的物质的量浓度为 。
(2)求合金中Mg、Al的物质的量之比,题中可作计算依据的数据是 ,求得的Mg、Al的物质的量之比为 。
(3)在丙组实验之后,向容器中加入1 mol·L-1的氢氧化钠溶液,能使合金中的铝恰好溶解,不形成含铝的沉淀,并使Mg2+刚好沉淀完全,再过滤出不溶固体,求滤液中各溶质的物质的量和所加入氢氧化钠溶液的体积(写计算过程)。
10.准确称取6 g铝土矿样品(含A12O3、Fe2O3、SiO2)放人盛有100 mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10 mol/L的NaOH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示:
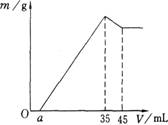 请填空回答:(1)H2SO4溶液的物质的量浓度为____;
请填空回答:(1)H2SO4溶液的物质的量浓度为____;
(2)若a=2.3,用于沉淀Fe3+消耗NaOH的体积是_____mL,
铝土矿中各组成成分的质量:
A12O3为____ Fe2O3为 SiO2为 .
9. 某无色溶液可能由Ba(NO3)2、MgCl2、KHS、KOH、Al2(SO4)3中的一种或几种混合而成,在此无色溶液中滴加稀HNO3,先产生白色沉淀 ,而后白色沉淀又会溶解,变为无色溶液。试填写下列空白:
(1)组成该无色溶液的确切成分是____________,形成该无色溶液的离子方程式是________________。
(2)滴加稀HNO3产生白色沉淀的离子方程式是____________,继续滴加HNO3使白色沉淀溶解的离子方程式是________________。
8.( )有10.2g Mg、Al混合物,溶于0.5L 4mol/L盐酸中。若加入2mol/L NaOH溶液,使得沉淀量最大,应加NaOH溶液的体积是A.0.1L B.0.5L C.1L D.1.5L
7.( )等体积、等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5:6,则甲、乙两烧杯中的反应情况可能分别是
A.甲、乙中都是铝过量 B.甲中铝过量、乙中碱过量
C.甲中酸过量、乙中铝过量 D.甲中酸过量、乙中碱过量
6.( )把铝粉和Fe3O4粉末配成铝热剂并分成两份,第一份在高温下恰好完全反应,然后将生成物与足量盐酸充分反应;第二份直接加入足量的氢氧化钠溶液使之充分反应,前后两种情况下生成的气体在相同状况下的体积比是 A.3:4 B. 4:3 C.3:8 D.8;3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com