
30.(太原成成中学九年级第五次月考)
如要将100g溶质质量分数为20%的硝酸钾溶液稀释成溶质质量分数为10%的硝酸钾溶液,需加入水的质量为
A.50g B.90g C.100g D.200g
29.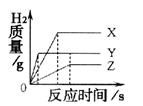 (太原成成中学九年级第五次月考)把相同体积、相同质量分数的稀盐酸,分别滴到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如右图所示。这三种金属的活动性顺序为
;假如X、Y、Z都是+2价金属,则相对原子质量由大到小的顺序为
。
(太原成成中学九年级第五次月考)把相同体积、相同质量分数的稀盐酸,分别滴到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如右图所示。这三种金属的活动性顺序为
;假如X、Y、Z都是+2价金属,则相对原子质量由大到小的顺序为
。
28.
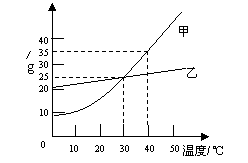 (太原成成中学九年级第五次月考)右图是甲、乙两固体物质的溶解度曲线图,看图后回答下列问题:
(太原成成中学九年级第五次月考)右图是甲、乙两固体物质的溶解度曲线图,看图后回答下列问题:
(1)40℃时,甲物质溶解度为_____________。
(2)30℃时,向100g水中加入30g乙物质,充分溶解后,所得溶液是 溶液(填“饱和”或“不饱和”),所得溶液中溶质的质量分数为 。
(3)20℃时,甲、乙两种物质的溶解度由大到小的顺序是_________________。
(4)两条曲线相交的含义是 _______________________________________________。
27. (太原成成中学九年级第五次月考)医生给病人输液时,常用葡萄糖注射液。右图为葡萄糖注射液的部分标签图,根据右图回答下列问题:
(太原成成中学九年级第五次月考)医生给病人输液时,常用葡萄糖注射液。右图为葡萄糖注射液的部分标签图,根据右图回答下列问题:
(1)从该溶液中取出10mL,则取出溶液中溶质的质量分数______________;
(2)某病人一天共输入该葡萄糖注射液1500mL,此病人这一天共补充葡萄糖__________g。
(3)如果从瓶中取出100g,将它变成15%的葡萄糖注射液,
需要加入_________g(结果精确到0.1g)的葡萄糖。
26. (泰兴市 济川实验初中 初三化学阶段试题)t℃时,向一支盛有0.1g熟石灰的试管内加入10mL水,充分振荡后,静置,试管底部仍有未溶解的白色固体。对于试管内上层澄清液体的叙述正确的是
A.溶液是t℃时的饱和溶液 B.升高温度溶液变为不饱和溶液
C.溶液中溶质的质量等于0.1g D.溶液中溶质的质量分数等于1%
25.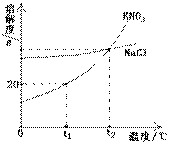 (天津市2009年中考化学冲刺模拟题六).右图是KNO3和NaCl的溶解度曲线。下列说法中正确的是 ( )
(天津市2009年中考化学冲刺模拟题六).右图是KNO3和NaCl的溶解度曲线。下列说法中正确的是 ( )
A.NaCl的溶解度不受温度的影响
B.t1℃时,KNO3饱和溶液中溶质的质量分数是20%
C.t2℃时,NaCl饱和溶液与KNO3饱和溶液中,
溶质的质量分数不一定相等
D.在温度高于t2℃范围内,KNO3的溶解度始终大于NaCl的溶解度
24.(湖北省大冶市2009年中考调研考试化学试卷)(2分)根据KNO3和NaCl的溶解度曲线,回答下列问题:
(1)10℃时KNO3的溶解度 NaCl溶解度(填“>”、“<”或“=”)。
(2)t℃时,将mg KNO3、ng NaCl 分别溶解在20mL水中恰好饱和,
则m n(填“>”、“<”或“=”)。
23.(桂林市灌阳县2009届初中毕业班第一次中考模拟考化学试卷)
(7分)甲.乙.丙三种物质的溶解度曲线如右图所示,
据图回答:
(1)50 ℃时,乙物质的溶解度是 g;
(2)30 ℃时,三种物质的溶解度由大到小的顺序为 ;
(3)要使饱和的丙溶液变为不饱和,可采取的措施是 ;
(4)40 ℃时, (填“能”或“不能”)配制溶质质量分数相同的甲和乙的饱和溶液;
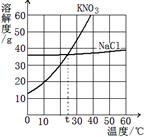 (5)50 ℃时,将等质量的甲.乙.丙三种物质的饱和溶液同时降温至10 ℃时,析出晶体最多的是 ,所得溶液中溶质质量分数最小的是 。
(5)50 ℃时,将等质量的甲.乙.丙三种物质的饱和溶液同时降温至10 ℃时,析出晶体最多的是 ,所得溶液中溶质质量分数最小的是 。
22.(2009年枣庄东方国际学校九年级化学二模试题)(8分)在我国某地区有一种“冬天捞碱,夏天晒盐”的说法。这里的“碱”是指Na2CO3,“盐”是指NaCl。这样捞得的“碱”中含有少量的NaCl。
某化学课外活动小组为了解释捞碱.晒盐的原理和测定“碱”样品中Na2CO3的含量进行了以下探究
[查阅资料]Na2CO3和NaCl的溶解度曲线如图所示。
(1)根据右图回答:
①t1 ℃时Na2CO3的溶解度为 g;
t2 ℃时Na2CO3的溶解度 ;
(填“<”、“>”或“=”)NaCl的溶解度。
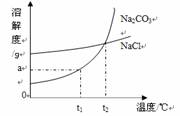 ②“冬天捞碱”的原因是由于Na2CO3的溶解度随温度降低而 (填“增大”“减小”或“不变”)。
②“冬天捞碱”的原因是由于Na2CO3的溶解度随温度降低而 (填“增大”“减小”或“不变”)。
③“夏天晒盐”是利用 (填序号)的方法,使NaCl晶体析出。
A.风吹日晒,使溶剂蒸发 B.升高温度,使NaCl溶解度增大
[实验步骤]
第一步:称取34.6 g“碱”样品
第二步:将样品放入130 g稀盐酸中,固体全部溶解,恰好完全反应。其化学方程式为:Na2CO3+2HCl==2NaCl+H2O+CO2↑
第三步:完全反应后,称得溶液的总质量为151.4 g。
[数据分析]
⑵若产生二氧化碳气体的全部逸出,试计算:(结果保留一位小数)
①产生二氧化碳气体的质量
②34.6g“碱”样品中碳酸钠的质量。
③“碱”样品中碳酸钠的质量分数。
 [继续研究]
[继续研究]
⑶计算反应后所得溶液中氯化钠的质量分数。
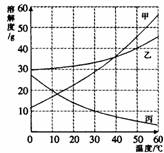
21. (2009年山东省枣庄市五校联考试题)(7分)甲、乙、丙三种物质的溶解度曲线如右图所示,据图回答:
(2009年山东省枣庄市五校联考试题)(7分)甲、乙、丙三种物质的溶解度曲线如右图所示,据图回答:
(1)50 ℃时,乙物质的溶解度是 g;
(2)30 ℃时,三种物质的溶解度由大到小的顺序为 ;
(3)要使饱和的丙溶液变为汪饱和,可采取的措施是
,
(4)40 ℃时, (填“能”或“不能”)配制溶质质量分数相同的甲和乙的饱和溶液;
(5)50 ℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10 ℃时,析出晶体最多的是 ,所得溶液中溶质质量分数最小的是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com