
1.木块A、B分别重50 N和60 N,它们与水平地面之间的动摩擦因数均为0.25。夹在A、B之间的轻弹簧被压缩了2 cm,弹簧的劲度系数为400 N/m。系统置于水平地面上静止不动。现用F=1 N的水平拉力作用在木块B上,如图所示。力F作用后
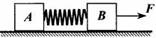 A.木块A所受摩擦力大小是12.5 N
A.木块A所受摩擦力大小是12.5 N
B.木块A所受摩擦力大小是11.5 N
 C.木块B所受摩擦力大小是9 N
C.木块B所受摩擦力大小是9 N
D.木块B所受摩擦力大小是7 N
4.硫酸工业在国民经济中占有极其重要的地位。
(1)硫酸的最大消费渠道是化肥工业,用硫酸制造的常见化肥有 (任写一种)。
(2)硫酸生产中,根据化学平衡原理来确定的条件或措施有 (填写序号)。
A.矿石加入沸腾炉之前先粉碎 B.使用V2O5作催化剂
C.转化器中使用适宜的温度 D.净化后的炉气中要有过量的空气
E.催化氧化在常压下进行 F.吸收塔中用98.3%的浓硫酸吸收SO3
(3)在硫酸工业中,通过下列反应使二氧化硫转化为三氧化硫:

2SO2(g)+O2(g) 2SO3(g) △H=-98.3kJ·mol-1
在实际工业生产中,常采用“二转二吸法”,即将第一次转化生成的SO2分离后,将未转化的SO2进行二次转化,假若两次SO2的转化率均为95%,则最终SO2的转化率为 。
 (4)硫酸的工业制法过程涉及三个主要的化学反应及相应的设备(沸腾炉、转化器、吸收塔)。
(4)硫酸的工业制法过程涉及三个主要的化学反应及相应的设备(沸腾炉、转化器、吸收塔)。
①三个设备分别使反应物之间或冷热气体间进行了“对流”。请简单描述吸收塔中反应物之间是怎样对流的。
 。
。
②工业生产中常用氨-酸法进行尾气脱硫,以达到消除污染、废物利用的目的。用化学方程式表示其反应原理。(只写出2个方程式即可)
。
3. 纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺,请按要求回答问题:
(1)“氨碱法”产生大量CaC12废弃物,请写出该工艺中产生CaC12的化学方程式:
;
(2)写出“联合制碱法”有关反应的化验学方程式:
; 。
(3)CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?
;
(4)绿色化学的重要原则之一是提高反应的原子利用率。根据“联合制碱法”总反应,列出计算原子利用率的表达式:
原子利用率(%)= 。
2. 聚合氯化铝晶体的化学式为[Al2(OH)nCl6-n·XH2O]m,它是一种高效无机水处理剂,它的制备原理是调节增大AlCl3溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣--铝灰,它主要含Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产的工艺流程如下:

(1)搅拌加热操作过程中发生反应的离子方程式为:
; 。
(2)生产过程中B和D的操作名称分别是 和 (B和D均为简单操作)。
(3)反应中副产品a是 。
(4)生产过程中可循环使用的物质是 (用化学式表示)。
 (5)调节pH至4.0~4.5的目的是
。
(5)调节pH至4.0~4.5的目的是
。
 (6)实验室要测定水处理剂产品中n和x的值。为使测定结果更准确,需得到的晶体较纯净。生产过程C物质可选用
。
(6)实验室要测定水处理剂产品中n和x的值。为使测定结果更准确,需得到的晶体较纯净。生产过程C物质可选用
。
A.NaOH B.Al C.氨水 D.Al2O3 E.NaAlO2
1. 现代社会中铜在电气、交通、机械和冶金、能源及石化工业、高科技等领域有广泛的应用。某铜矿石含氧化铜、氧化亚铜、三氧化二铁和脉石(SiO2),现采用酸浸法从矿石中提取铜,其工艺流程图如下。其中铜的萃取(铜从水层进入有机层的过程)和反萃取(铜从有机层进入水层的过程)是现代湿法炼铜的重要工艺手段。

已知:①Cu+在酸性溶液中不稳定,可发生自身氧化还原反应;②当矿石中三氧化二铁含量太低时,可用硫酸和硫酸铁的混合液浸出铜;③反萃取后的水层2是硫酸铜溶液。
回答下列问题:
(1)矿石用稀硫酸处理过程中Cu2O发生反应的离子方程式为: ;
(2)“循环I”经多次循环后的水层1不能继续循环使用,但可分离出一种重要的硫酸盐晶体,该晶体的化学式是 。若水层1暴露在空气中一段时间后,可以得到另一种重要的硫酸盐,写出水层1暴露在空气中发生反应的离子方程式 。
(3)写出电解过程中阳极(惰性电极)发生反应的电极反应式: 。
(4)“循环III”中反萃取剂的主要成分是 。
16、
15、(温州市十校2008学年高三第一学期期初联考 数学试题(文))
已知 ,若
,若 是
是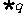 充分而不必要条件,求实数
充分而不必要条件,求实数 的取值范围.
的取值范围.
解:由题意
p: 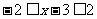
∴  (3分)
(3分)
∴ :
: (5分)
(5分)
q: (8分)
(8分)
∴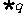 :
: (10分)
(10分)
又∵ 是
是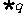 充分而不必要条件
充分而不必要条件
∴ ∴
∴ (14分)
(14分)
14、(绍兴市2008学年第一学期统考数学试题)已知集合 ,集合B=
,集合B=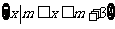 ;(1)当
;(1)当 时,求
时,求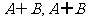 ;(2)若
;(2)若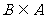 ,求
,求 的取值范围.
的取值范围.
解析:(1)当 时,
时, ;
;
(2)若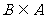 ,则
,则 的取值范围为
的取值范围为 .
.
13、(重庆市万州区2009级高三第一次诊断性试题)已知集合A=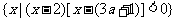 ,
, .
.
(Ⅰ) 当a=2时,求A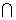 B;
B;
(Ⅱ) 求使B A的实数a的取值范围.
A的实数a的取值范围.
解:(Ⅰ)当a=2时,A= ,
…………………………2分
,
…………………………2分
B= …………………………4分
…………………………4分
∴ A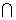 B=
B= …………………………6分
…………………………6分
(Ⅱ)∵(a2+1)-a=(a- )2+
)2+ >0,即a2+1>a
>0,即a2+1>a
∴B={x|a<x<a2+1} ……………………7分
①当3a+1=2,即a=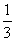 时A=Φ,不存在a使B
时A=Φ,不存在a使B A ……………………8分
A ……………………8分
②当3a+1>2,即a>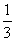 时A={x|2<x<3a+1}
时A={x|2<x<3a+1}
由B A得:
A得: 2≤a≤3
…………………10分
2≤a≤3
…………………10分
③当3a+1<2,即a<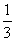 时A={x|3a+1<x<2}
时A={x|3a+1<x<2}
由B A得
A得 -1≤a≤-
-1≤a≤- …………………12分
…………………12分
综上,a的范围为:[-1,- ]∪[2,3] …………………13分
]∪[2,3] …………………13分
12、(苍山诚信中学·理科)22.(本小题满分14分)
已知函数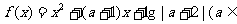 R,且
R,且 .
.
(I)若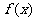 能表示成一个奇函数
能表示成一个奇函数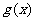 和一个偶函数
和一个偶函数 的和,求
的和,求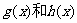 的解析式;
的解析式;
(II)命题P:函数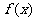 在区间
在区间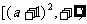 上是增函数;
上是增函数;
命题Q:函数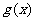 是减函数.
是减函数.
如果命题P、Q有且仅有一个是真命题,求a的取值范围;
(III)在(II)的条件下,比较 的大小.
的大小.
(解)(1)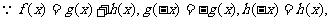
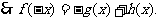
 ………2分
………2分
解得 ………………4分
………………4分
(2) 在区间
在区间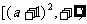 上是增函数,
上是增函数,
 解得
解得 …………6分
…………6分
又由函数 是减函数,得
是减函数,得 …………8分
…………8分
∴命题P为真的条件是:
命题Q为真的条件是: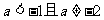 .
.
又∵命题P、Q有且仅有一个是真命题,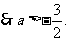 ……………………10分
……………………10分
(2)由(1)得
设函数 .
.
∴函数 在区间
在区间 上为增函数.………………12分
上为增函数.………………12分
又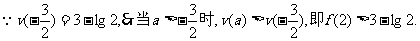 ………14分
………14分
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com