
3、化解知识难点 化学平衡中的难点不少,应讲究方法,分类突破。比如
①演绎法:用v-t图象来完整地演绎平衡建立与移动的过程,理解反应速率和化学平衡的内在联系,即平衡移动的根本原因是v(正)≠v(逆),平衡建立的必要条件是v(正)=v(逆),等则平,不等则变;如浓度变化的v-t图象:

②“定一议二”和“先拐先平”法:分析平衡图象时确定一个因素而讨论另外二个因素之间的关系和先出现拐点即先达到平衡的曲线温度高或压强大或使用了催化剂,如06江苏第16题;
③巧妙转化法:只有一种反应物或生成物的平衡,又加入该物质时,分析平衡移动方向依据浓度变化,比较转化率时将浓度的变化转化为压强的变化能使思路清晰,如下表。aA(g) bB(g)型反应浓度变化时平衡移动与转化率变化分析表
bB(g)型反应浓度变化时平衡移动与转化率变化分析表
|
|
特点 |
示例 |
改变 |
变化 |
移动方向 |
平衡比较 |
|
(1) |
△n>0 |
PCl5(g) PCl3(g)+Cl2(g) PCl3(g)+Cl2(g) |
又充入PCl5 |
c(PCl5)增大,平衡右移,p增大,平衡左移 |
右移 |
α(PCl5)减小,φ(PCl5)增大 |
|
(2) |
△n=0 |
2HI(g)  H2(g)+I2(g) H2(g)+I2(g) |
又充入HI |
c(HI)增大,平衡右移,p增大,平衡不移动 |
右移 |
α(HI)不变,φ(HI)不变 |
|
(3) |
△n<0 |
2NO2(g)
 N2O4(g) N2O4(g) |
又充入NO2 |
c(NO2)增大,平衡右移,p增大,平衡右移 |
右移 |
α(NO2)增大,φ(NO2)减小 |
④平衡计算的行之有效的“列三行”(起始、变化、平衡或始、变、末)法;
⑤等效平衡中的“一边倒”、 “极限法”、“投料量相同”、“投料比相同”等等。
讲到位、讲透彻是突破难点的方法,难点的突破能增强学生的学习信心。
2、理出知识清单
(1) 比如“化学反应速率”的知识清单有:化学反应速率的概念、定性比较与定量描述,反应速率之比与化学计量数之比和化学方程式之间的关系,浓度、压强、温度、催化剂、接触面积、光照、原电池等条件对反应速率的影响及速率随时间变化的曲线;“化学平衡”的知识清单有:化学平衡的建立、特征、标志,浓度、温度、压强、催化剂及加入稀有气体对正、逆反应速率的影响和平衡移动方向,旧平衡的建立、移动和新平衡的建立过程中条件的变化、速率的变化、移动的方向以及新平衡与旧平衡中各物质的物质的量、含量、浓度、转化率、气体的密度、压强、相对分子质量、反应热等各种量的比较、各种量的计算及相关的变化图象,定温定压和定温定容条件下等效平衡的建立和比较、计算;合成氨的知识清单有:合成氨反应的特点,适宜条件的选择,工业生产流程,与接触法制硫酸、侯氏制碱法的的联系等。知识清单能让学生对主干知识心中有数,又是学生自评掌握情况的依据。复习时要注意“概念求准”--如v正、v逆、活化分子、平衡特征、平衡标志等概念理解准确;理论求透--如勒夏特列原理,通过实验回顾、速率分析、模型建立来理解,最后巧用比喻“对着干”来小结
1、认真分析高考,确定复习标高
化学平衡内容理论性强,难度伸缩性大,在平时的考试中一般都考的较难,但近年高考各地差距较大,理综题都并不难,江苏、广东的试题较难。建议分层次,以教材习题和理综高考题为低目标,以单学科高考题为高目标。以单科卷的要求来面对综合卷,足矣。
(四)创新题
20、对于一定条件下的可逆反应,无论从正反应开始,还是从逆反应开始,都可以达到相同的平衡状态。一定温度下,碳与水蒸气在容积不变的密闭容器中发生反应并建立平衡:
C(s)+H2O(g)  CO(g)+H2(g); △H >0,试问:
CO(g)+H2(g); △H >0,试问:
(1)平衡混合气的平均相对分子质量M1的取值范围为 <M1< 。
(2)将平衡混合气体升高温度,混合气体平均相对分子质量 (填增大、减小或不变,下同),密度将 。
(3)若使用等物质的量的CO和H2从逆反应方向在相同条件下建立平衡,则混合气体的平均相对分子质量M2的取值范围为 <M2< ;若使用不等物质的量的CO和H2从逆反应方向在相同条件下建立平衡,则混合气体的平均相对分子质量M3的取值范围为
<M3< 。
(4)若起始投料C(s)1mol,H2O(g)1mol,在相同条件下反应达到平衡,混合气体平均相对分子质量为M,下列四组投料在在相同条件下反应达到平衡后合气体的平均相对分子质量 不可能为M的是(填写代号) .
A.C(s)2mol,H2O(g)1mol B.CO(g)1mol,H2(g)1mol
C.C(s)0.5mol,H2O(g)0.4mol,CO(g)0.6mol,H2(g)0.6mol
D.C(s)0.9mol,H2O(g)0.9mol,CO(g)0.1mol
21、合成氨工业中,原料气(N2,H2及少量的CO,NH3的混合气)在进入合成塔前常用乙酸二氨合铜(Ⅰ)溶液来吸收原料气中CO,其反应为:[Cu(NH3)2Ac]+CO+NH3
 [Cu(NH3)3]Ac·CO;△H<0
[Cu(NH3)3]Ac·CO;△H<0
(1)必须除去原料气中CO的原因是什么?
(2)吸收CO的生产适宜条件是什么?
(3)吸收CO后的乙酸铜氨液经过适当处理后又可再生,恢复其吸收CO的能力以供循环使用,再生的适宜条件是什么?
解析答案
1、D 2、B 3、C 4、BD 5、解析:本题考查了等效平衡问题。在等温等压条件下,把加入的物质按照反应方程式的计量数转化为反应物或生成物,物质的量之比保持一致即为等效平衡。选项A、B中三者比例为2∶1∶2 ,与题中比例一致,为等效平衡,平衡不移动。C可设想为两步加入,第一次加入1 mol A、0.5 mol B、1 mol C,此时平衡不移动,第二次再加0.5 mol B(此法与一次性各加入1 mol等效),提高反应物浓度,平衡向右移动。D中均减少1 mol,也可以设想为两步进行:先将A减少1 mol,B减少0.5 mol,C减少1 mol,此时平衡不移动,再将B减少0.5 mol,降低反应物浓度,平衡向右移动。
答案:C
6、解析:本题考查的是学生对影响速率各因素的理解和掌握情况。使用催化剂能同等程度地改变正逆反应速率;此反应为一气体反应,压强增大,反应速率也增大,压强减小,反应速率也减小;升高温度,给反应体系中施加了能量,分子碰撞机会增多,正、逆反应速率都增大。答案:C
7、解析:该题的关键是HBr由第一个反应生成后,又有一部分在第二个反应中分解,只有求出HBr的总浓度,才能与NH3联系起来。
c(HBr)总=4 mol·L-1+2×0.5 mol·L-1=5 mol·L-1
又c(NH3)=c(HBr)总则有:
v(NH3)= =
= =2.5 mol·L-1·min-1。答案:B
=2.5 mol·L-1·min-1。答案:B
8、解析:本题考查的是影响平衡的因素对化学平衡的影响。
A选项,因SO2与H2S作用,使H2S浓度下降,平衡正向移动;B选项,因NH4HS是固体,对平衡不影响,平衡不移动;C选项,因定容条件下,充入N2时,对体系各物质的浓度并没有产生影响,故平衡不移动;D选项,因恒压条件,充入N2时容器的体积必扩大,反应体系各物质的浓度都减小,相当于减压,平衡正向移动。答案:BC
9、解析:本题所给的平衡体,系是一反应前后体积不变的可逆反应,不受压强影响。其思维过程如下图: 
我们设开始时有一容器A′,容积是A和B的2倍,并向A′中充入2 mol的HI气体,B中充入1 mol的HI气体。控制A′与B的温度都为427 K,这样A′与B中将建立同一化学平衡状态,此时A′与B两个容器中各自的平衡浓度、各组分的百分含量为定值,且平衡时相等。我们再对A′加压使之变成A的容积,因压强增大,反应速率变大,可见如果一开始把2 mol HI充入A时,速率要比B中大,对B而言A相当于加大了压强,平衡时间A中较B中短,但加压平衡并不发生移动,因而各反应物的转化率均不变,各组分的体积分数都不变,但因物质的量有加和性。故c(I2)A=2c(I2)B。答案:D
10、解析:根据题意,我们可以设开始充入的3
L X气体中含X的物质的量为3a mol,则2 L Y气体中含Y的物质的量为2a
mol,因为反应在6 L的恒容容器中进行,所以当X的浓度减小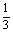 时,其物质的量必减小
时,其物质的量必减小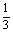 ,则X减小a mol,故有:
,则X减小a mol,故有:
4X(g)+
3Y(g)  2Q(g)+ nR(g) ?Δn
2Q(g)+ nR(g) ?Δn
4 mol 3 mol 2 mol n mol (n-5)mol
a mol 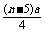 mol
mol
由压强增加百分比等于物质的量增加百分比可得: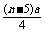 /5a=5%解得:n=6。
/5a=5%解得:n=6。
巧解:依题意压强较反应前增大,这就意味着反应向生成气体物质的量增大的方向进行了。则有:n+2>4+3 n>5。 答案:D
11、解析:由图(Ⅰ)可知:当温度相同时,p2时达平衡较p1时到平衡所需时间短,则p2>p1,又知p2时C%较p1时的C%大,从而可知x只能为1,再从T2p2、T1p2两图线可知:当压强相同时,T1条件下反应达平衡时间较T2短,则推知T1>T2,且T1时C%较T2时小,推知正反应为放热反应,则Q>0,由以上分析可知:升高温度或降低压强都可以使平衡向逆向移动。
A选项,升高温度时,A的转化率减小,当温度不变时,压强增大,A的转化率也增大,故A选项正确。
B选项,升高温度时,B的百分含量增大,所以B选项不正确。
C选项,因反应在恒容条件下进行,又因为气体的总质量不变,故气体的密度也不变,故C选项不正确。
D选项,升高温度平衡逆向移动,气体的物质的量增加,平均摩尔质量减小,同温下,压强越大气体的物质的量越小,平均摩尔质量变大,所以D选项正确。
规律:化学反应平衡图象问题
①弄清横、纵坐标轴及曲线三者之间的关系及涵义 ②弄清曲线中特殊点、拐点、交点、起点和终点的化学意义。如反应:N2(g)+3H2(g)  2NH3(g)+Q中N2
2NH3(g)+Q中N2

的转化率与温度T,压强p,时间t的关系图中“先拐先平”,“先拐”即先出现拐点,按速率理论,说明温度高或压强大。“先平”即先达到平衡。再根据勒沙特列原理,采取“定议二”的办法,即定温度,讨论纵轴与压强的关系,或定压强,讨论温度与纵轴的关系。(例如:图中如果定温度为T2时,可以看出压强p2的图线较压强p1的曲线先达到平衡,时间t1<t3,也不难看出,p2对应的平衡线较p1对应的平衡线的水平部分高,也即压强大时N2的转化率高。同理,我们也可以定压强p1,讨论T1与T2的高低,因为平衡时间t2<t3,推知T1>T2,升高温度平衡逆向移动,也不难看出温度高时,N2对应的转化率平衡线水平部分是低的)答案:AD
12、解析:(方法一)设新平衡时生成HI气体的物质的量为x mol,则有:
H2(g) + I2(g)  2HI(g)
2HI(g)
1 mol 1 mol 2 mol
转化量  mol
mol  mol x
mol
mol x
mol
平衡时 (2.5- )mol (2.5-
)mol (2.5- )mol x mol
)mol x mol
因为反应器的容积为1 L,则依题意有:

整理得:x=4 mol。
(方法二)因为反应是一不受压强影响的反应,我们可以设想有一个4 L的容器,向其中充入2 mol H2和2 mol I2蒸气,平均每升中各占0.5 mol H2和I2,可见当它建立平衡状态时,每升中平均有0.8 mol的HI气体,然后我们再用某种方法把这4 L气体压入原容器中,因平衡不受压强影响,故得出HI的总物质的量为
 ×0.8 mol=4 mol。答案:B
×0.8 mol=4 mol。答案:B
13、BC 14、BD 15、B
16、解析:(1)VA=0.8mol·L-1-0.67mol·L-1/10min =0.013 mol·(L·min)-1。
(2)对比实验1与实验2可知,从10min到20min,实验1的A的浓度相同,说明是同一平衡状态,即c2= 1.0 mol·L-1,又因实际反应的速率快,达到平衡所需时间短,说明反应中使用了催化剂。
(3)对比实验3与实验1可知,从10min到20min,实验1的A的浓度变化值为0.13 mol·L-1,而实验3的A浓度变化值为0.17 mol·L-1,这就说明了υ3>υ1。又知从0min到10minA的浓度变化值应大于0.17 mol·L-1,即c3>(0.92+0.17)mol·L-1 =1.09 mol·L-1。
(4)对比实验4与实验1可知,两实验的起始浓度相同,反应温度不同,达平衡时实验4的A的浓度小,说明了实验4A进行的程度大,即温度越高,A的转化率越大,说明正反应为吸热反应。 [答案] (1)0.013(2)1.0;催化剂(3)>;>(4)吸热;温度升高时,平衡向右移动
17、(1)(1-a);(2)3a;(3)2、(3-3a)、丁。若3a大于1,B的物质的量小于2mol、若3a=1,B的物质的量等于2mol、若3a小于1,B的物质的量大于2mol;(4)a/(2-a);(5)乙。因为(5)小题中容器容积不变,而(1)小题中容器的容积缩小,所以(5)小题的容器中的压强小于(1)小题容器中的压强,有利于逆向反应,帮反应达到平衡后a大于b。
18、 (1) 0.03 (2) ①平衡 大于 ② d a
19、(1)a=16 (2)8mol (3)5:4 (4)2:3 (5)1:2 (6)3:3:2
20、(1)15,18 (2)减小,增大 (3)15,18;2,28 (4)D
21、[解析] 合成氨工业中要使用催化剂,某些物质会使催化剂的活性降低甚至消失,从而发生催化剂中毒。故必须除去原料气中CO。根据吸收原料气中CO的反应方程式:[Cu(NH3)2Ac]+CO+NH3
 [Cu(NH3)3]Ac·CO;△H<0可知,加压和采取较低的温度可使平衡向正反应方向移动,有利于CO的吸收。要使吸收CO后的乙酸铜氨液经过适当处理后又可再生,恢复其吸收CO的能力以供循环使用,只要使平衡向逆反应方向移动即可。
[Cu(NH3)3]Ac·CO;△H<0可知,加压和采取较低的温度可使平衡向正反应方向移动,有利于CO的吸收。要使吸收CO后的乙酸铜氨液经过适当处理后又可再生,恢复其吸收CO的能力以供循环使用,只要使平衡向逆反应方向移动即可。
[答案](1)防止催化剂中毒;(2)低温、高压;(3)高温、低压。
(三)解答题
19、 恒温下,将amolN2与bmolH2的混合气体通入一个固定容积的密闭容器中,发生如N2(g)+3H2(g) 2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,计算a的值。
(2)反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的量。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始)∶n(平)= 。
(4)原混合气体中,a∶b= 。
(5)达到平衡时,N2和H2的转化率之比,α(N2)∶α(H2)= 。
(6)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)=
(二)、填充题
16、某化学反应2A 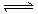 B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:

根据上述数据,完成下列填空:
⑴在实验1,反应在10至20min时间内平均速率为 mol·(L·min)-1。
⑵在实验2,A的初始浓度c2= mol·L-1,反应经20min就达到平衡,可推测实验2中还隐含的条件是 。
⑶设实验3的反应速率为υ3,实验1的反应速率为υ1,则υ3 υ1(填“>”“=”“<”),且c3 1.0mol·L-1(填“>”“=”“<”)。
⑷比较实验4和实验1,可推测该反应是 反应(选填“吸热”“放热”)。理由是 。
17、Ⅰ.恒温恒压下,在一个可变容积的容器中发生如下反应:
A(气)+B(气) C(气)
C(气)
(1)若开始时放入1molA和1molB,达到平衡后,生成amolC,这时A的物质的量为_________mol。
(2)若开始时放入3molA和3molB,达到平衡后,生成C的物质的量为_________mol。
(3)若开始时放入xmolA和2molB和1molC,达到平衡后,A和C的物质的量分别是ymol和3amol,则x= mol,y= mol。
平衡时,B的物质的量 (选填一个编号)。
(甲)大于2mol (乙)等于2mol
(丙)小于2mol (丁)可能大于、等于或小于2mol。
(4)若在(3)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数为 。
Ⅱ.若维持温度不变,在一个与(1)反应前起始体积相同、且容积固定的容器中发生上述反应
(5)开始时放入1molA和1molB到达平衡后生成bmolC。将b与(1)小题中的a进行比较 (选填一个编号)。
(甲)a<b (乙)a>b (丙)a=b (丁)不能比较a和b的大小
作出此判断的理由是 。
18、 (1)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
CO(g)十H2O(g)
 CO2(g)十H2 (g)十Q(Q>0)
CO2(g)十H2 (g)十Q(Q>0)
CO和H2O浓度变化如下图,则 0-4min的平均反应速率v(CO)=______ mol/(L·min)

(2)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min-4min之间反应处于_________状态; C1数值_________0.08 mol/L (填大于、小于或等于)。
②反应在4min-5min问,平衡向逆方向移动,可能的原因是________(单选),表中5min-6min之间数值发生变化,可能的原因是__________(单选)。
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度
(一) 选择题
1、反应E+F=G在温度T1下进行,反应M+N=K在温度T2下进行,已知T1>T2,且E和F的浓度均大于M和N的浓度(其它条件均相同),则两者的反应速率 ( )
A.前者大 B.后者大 C.一样大 D.无法判断
2、 将下列四种X溶液,分别加入四个盛有10mL3 mol/L的稀硫酸的烧
杯中,加水稀释到100mL,此时,X和盐酸缓慢反应,其中反应最快的是 ( )
A.10℃ 20mL 3mol/L的X溶液 B.20℃ 30mL 2mol/L的X溶液
C.20℃ 10mL 4mol/L的X溶液 D.10℃ 10mL 2mol/L的X溶液
3、可逆反应:A+3B 2C+2D在四种不同的情况下,反应速率分别为①VA=0.15mol/(L·S)②VB=0.6mol/(L·S)③VC=0.4mol/(L·S)④VD=0.45mol/(L·S)则以上四种情况下反应速率由小到大排列正确的是
( )
2C+2D在四种不同的情况下,反应速率分别为①VA=0.15mol/(L·S)②VB=0.6mol/(L·S)③VC=0.4mol/(L·S)④VD=0.45mol/(L·S)则以上四种情况下反应速率由小到大排列正确的是
( )
A.②>④>③>① B.②>③=④>①
C.④>②=③>① D.④>③>②>①
4、 对于可逆反应N2 (g) + 3 H2(g) 2NH3(g)达到平衡状态,下列关系式正确的是
对于可逆反应N2 (g) + 3 H2(g) 2NH3(g)达到平衡状态,下列关系式正确的是
( )
A.v(H2)正=3v(N2)正 B.v(H2)正=3v(N2)逆
C.2v(NH3)逆=v(N2)正 D.2v(H2)正=3v(NH3)逆
5、某温度下,在一容积可变的容器中,反应2A(g)+B(g)  2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、2 mol和4 mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是
( )
2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、2 mol和4 mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是
( )
A.均减半 B.均加倍 C.均增加1 mol D.均减少1 mol
6、NO和CO都是汽车尾气中的有害物质,它们缓慢起反应生成氮气和二氧化碳,即:
2NO+2CO 2CO2+N2,对此反应下列叙述正确的是
( )
2CO2+N2,对此反应下列叙述正确的是
( )
A.使用催化剂不改变反应速率 B.降低压强,逆反应速率增大
C.升高温度能加快反应速率 D.压强对该反应无影响
|
 NH3(g)+HBr(g),2HBr(g)
NH3(g)+HBr(g),2HBr(g) Br2(g)+H2(g),两分钟后,反应达平衡,测得c(H2)=0.5
mol·L-1,c(HBr)=4 mol·L-1,若用v(NH3)表示反应速率,下列表示正确的是
( )
Br2(g)+H2(g),两分钟后,反应达平衡,测得c(H2)=0.5
mol·L-1,c(HBr)=4 mol·L-1,若用v(NH3)表示反应速率,下列表示正确的是
( )
A.0.5 mol·L-1·min-1 B.2.5 mol·L-1·min-1
C.2 mol·L-1·min-1 D.5 mol·L-1·min-1
8、反应NH4HS(s) NH3(g)+H2S(g)在某温度下达到平衡,下列各种情况中,平衡不能发生移动的是
( )
NH3(g)+H2S(g)在某温度下达到平衡,下列各种情况中,平衡不能发生移动的是
( )
A.其他条件不变时,通入SO2气体 B.移走一部分NH4HS固体
C.恒容条件下,充入一定量的氮气D.压强不变时,充入一定量的氮气
9、在体积相等的密闭容器A、B中,保持温度为427 K,同时向A、B中分别加入a mol和b mol的HI气体(a>b),待反应2HI(g)  H2(g)+I2(g)达到平衡后,下列说法中正确的是
( )
H2(g)+I2(g)达到平衡后,下列说法中正确的是
( )
A.从反应开始至平衡所需时间tA>tB B.平衡时I2的浓度c(I2)A=c(I2)B
C.平衡时I2蒸气的体积分数A%>B% D.HI的平衡分解率αA=αB
10、在一个6 L的密闭容器中放入3 L
X气体和2 L Y气体,在一定条件下发生下列反应:4X(g)+3Y(g)  2Q(g)+nR(g)当反应达平衡后,容器内温度不变,混合气体的压强比原来增大5%,X的浓度减小
2Q(g)+nR(g)当反应达平衡后,容器内温度不变,混合气体的压强比原来增大5%,X的浓度减小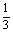 ,则该反应式中n的值为
(
)
,则该反应式中n的值为
(
)
A.3 B.4 C.5 D.6
11、在某容积一定的密闭容器中,可逆反应A(g)+B(g) xC(g)+Q符合图(Ⅰ)所示的关系,则由此推断图象(Ⅱ)的正确说法是
( )
xC(g)+Q符合图(Ⅰ)所示的关系,则由此推断图象(Ⅱ)的正确说法是
( )

A.p3>p4 y轴表示A的转化率 B.p3<p4 y轴表示B的百分含量
C.p3>p4 y轴表示混合气体的密度 D.p3>p4 y轴表示混合气体的平均摩尔质量
12、已知可逆反应:H2(g)+I2(g) 2HI(g)在一定温度下达到平衡,平衡时各平衡浓度间存在
2HI(g)在一定温度下达到平衡,平衡时各平衡浓度间存在 为一常数,若某温度时,1 L密闭容器中充入H2和I2的物质的量各0.5 mol,平衡时生成的HI为0.8
mol,如果其他条件不变,再充入2 mol H2和2 mol I2蒸气,则达到新平衡时生成HI的物质的量为
( )
为一常数,若某温度时,1 L密闭容器中充入H2和I2的物质的量各0.5 mol,平衡时生成的HI为0.8
mol,如果其他条件不变,再充入2 mol H2和2 mol I2蒸气,则达到新平衡时生成HI的物质的量为
( )
A.0.8 mol B.4 mol C.3.2 mol D.2.4 mol
13、(06江苏)某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):

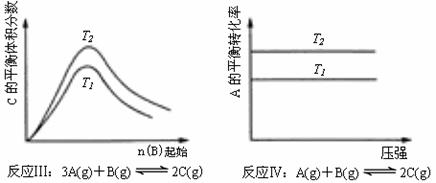
根据以上规律判断,下列结论正确的是
A.反应Ⅰ:△H>0,P2>P1
B.反应Ⅱ:△H<0,T1>T2
C.反应Ⅲ:△H>0,T2>T1;或△H<0,T2<T1
D.反应Ⅳ:△H<0,T2>T1
14、(07江苏)一定温度下可逆反应:A(s)+2B(g) 2C(g)+D(g);△H<0。现将1mol A和2molB加入甲容器中,
2C(g)+D(g);△H<0。现将1mol A和2molB加入甲容器中,
将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达
到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
A.保持温度和活塞位置不变,在甲中再加入1molA和2molB,达到新的平衡后,甲中C的浓度
是乙中C的浓度的2倍
B.保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增人
C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数
是甲中C的体积分数的2倍
D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速
率变化情况分别如图2和图3所示(t1前的反应速率变化已省略)

15、 (07福建理综)下图是在恒温密闭容器中进行的某化学反应的反应速率随时间变化的示意图。下列叙述与示意图不相不符的是
(07福建理综)下图是在恒温密闭容器中进行的某化学反应的反应速率随时间变化的示意图。下列叙述与示意图不相不符的是
A、反应达平衡时,正反应速率和逆反应速率相等
B、该反应达到平衡态I后,增大反应物的浓度,平衡发生移动,达到平衡态II
C、该反应达到平衡态I以后,减小反应物浓度,平衡发生移动,达到平衡态II
D、同一种反应物在平衡态I和平衡态II时浓度不相等。
(二)2008年高考预测
化学反应速率理论上是解决快出产品的问题,化学平衡理论主要是解决多出产品的。这两个问题无论对理论研究还是化工生产都具有重大意义。预测在2007年高考选择题中多以考查化学平衡的基本概念和影响平衡移动的条件为主,对化学平衡的计算的考查主要是基础计算,而在第Ⅱ卷中,常出现高思维强度的题目,以考查学生的思维判断能力,例如等效平衡的比较判断,应用数学方法对化学平衡原理进行定量分析等。
1、稳定 高考命题的指导思想一直是稳中有变,2008年高考对化学平衡的考查也会在题型、题量、赋分、取材、命题风格上保持相对稳定。鉴于05、06、07年的综合题中化学平衡几乎都占1/16, 08年试卷中出一道选择题的可能性仍是最大的。同时,近年综合卷中难觅大题踪影,因此,以大型填空题或填空、实验、计算相融合的综合题来考查化学平衡的可能性也是存在的。
2、 创新 创新是试题的灵魂和魅力所在。化学平衡中包含很广阔的创新空间,如化学
反应速率和化学平衡的实验分析和设计、灵活多变的化学平衡图象、小巧新颖的速率和平衡计算等,特别是在情景、取材上创新,在图象上创新,化学平衡的思想和勒夏特列原理在其它平衡体系中的应用等值得关注。
3、综合 学科内综合性体现好的试题是“亮点”,显得新颖而体现选拔功能。这方面江苏的考题走在前面, 往往4个选项的角度不同或4个图象的类型不同,这种综合方式还可能出现在今后的高考中并会不断创新。
4、 迁移 这里所说的迁移主要是指各种不同类型的高考试卷之间的借鉴迁移。如全国卷与京津卷、综合卷与单科卷、旧课程卷与新课程卷等。现行新教材中补充了化学反应速率的定量测定和曲线绘制(旧教材中侧重于定性比较)、活化能、平衡常数、沉淀溶解平衡、溶度积等大量知识,是否会以信息的形式引入即将进入新课程的省区的高考试题中是一个值得考虑的问题。
(一)方法总结
1、外界条件的变化对v(正)、v(逆)的影响
升温,v(正)、v(逆)一般均加快,吸热反应增加的倍数大于放热反应增加的倍数;降温,v(正)、v(逆)一般均减小,吸热反应减小的倍数大于放热反应减小的倍数。加压对有气体参加的反应,v(正)、v(逆)均增大,气体体积之和大的一侧增加倍数大于气体体积之和小的一侧增加的倍数;降压,v(正)、v(逆)均减小,气体体积之和大的一侧减小的倍数大于气体体积之和小的一侧减小的倍数。增加反应物的浓度,v(正)急剧增大,v(逆)逐渐增大。加催化剂可同倍地改变v(正)、v(逆)。
稀有气体或其他非反应气体,充入反应容器中,分以下两种情况讨论:①若容器恒温、恒容,则充入的稀有气体或其他不反应气体虽改变了容器内气体压强,但却没有改变反应气体产生的分压,即并没有改变反应物的浓度,不影响化学反应速率。②若容器恒温、恒压,则充入的稀有气体或其他不反应气体,就会使容器容积扩大,虽未减少容器内气体压强,但却减小了反应气体产生的分压,即降低了反应的浓度,故能使反应速率降低。
2、分析化学平衡移动的一般思路

应用上述规律分析问题时应注意:
(1)不要把v(正)增大与平衡向正反应方向移动等同起来,只有v(正)>v(逆)时,才使平衡向正反应方向移动。
(2)不要把平衡向正反应方向移动与原料转化率的提高等同起来,当反应物总量不变时,平衡向正反应方向移动,反应物转化率提高,当增大一种反应物的浓度,使平衡向正反应方向移动时,只会使另一种反应物的转化率提高。
3、判断可逆反应达到平衡状态的方法和依据(标志)


4、等效平衡原理及规律
(1)等效平衡原理
相同条件下,同一可逆反应体系,不管从正反应开始,还是从逆反应开始,只要按反应方程式中的化学计量数之比投入反应物或生成物,建立起的平衡状态都是相同的,这就是所谓等效平衡原理。
由于化学平衡状态与条件有关,而与建立平衡的途径无关。因而,同一可逆反应,从不同的状态开始,只要达到平衡时条件(温度、浓度、压强等)完全相同,则可形成等效平衡。
如:常温常压下,可逆反应:
2SO2 + O2  2SO3
2SO3
①2 mol 1 mol 0 mol
②0 mol 0 mol 2 mol
③0.5 mol 0.25 mol 1.5 mol
①从正反应开始,②从逆反应开始,③正逆反应同时开始,由于①②③三种情况如果按方程式的计量关系折算成同一方向的反应物,对应各组分的物质的量均相等(如将②③折算为①)。
(2)等效平衡规律
①在定温、定容条件下,对于反应前后气体分子数不变的可逆反应只改变起始时加入物质的物质的量,如通过可逆反应的化学计量数比换算成同一半边的物质的物质的量与原平衡相同,则两平衡等效。
②在定温、定容情况下,对于反应前后气体分子数不变的可逆反应,只要反应物(或生成物)的物质的量的比值与原平衡相同,两平衡等效。
③在定温、定压下,改变起始时加入物质的物质的量,只要按化学计量数换算成同一半边的物质的物质的量之比与原平衡相同,则达平衡后与原平衡等效。
5.化学反应速率大小的变化与化学平衡移动的关系
根据化学平衡状态的实质是v(正)=v(逆)可知,某可逆反应是否处于化学平衡状态与v(正)、v(逆)的数值大小无关,只与v(正)、v(逆)的相对大小有关,即当外界条件改变引起v(正)、v(逆)的大小发生变化时,平衡状态是否发生移动,取决于变化后的v(正)、v(逆)的相对大小。总结如下:不管v(正)、v(逆)的数值变大还是变小,只要变化后①v′(正)>
v′(逆),则平衡正向移动;②v′(正)<v′(逆),则平衡逆向移动;③v′(正)=v′(逆),则平衡不发生移动。
6.勒夏特列原理的适用范围
勒夏特列原理适用于中学化学中一切关于平衡的问题,即它除适用于化学平衡外,还适用于溶解平衡、电离平衡、水解平衡、络合平衡等有关平衡的问题。
7.稀有气体与化学平衡
(1)在恒温、恒容下:平衡不发生移动。因为恒容,各气体组分的浓度不变。可认为各气体的“分压”没变,对平衡无影响。
(2)在恒温、恒压下:平衡一般发生移动。因为恒压,充入稀有气体,体积一定增大,各气体组分的浓度减小,平衡向着使气体体积增大的方向移动。但对于反应前后气态物质的总体积不变的反应,平衡不移动。
8.解有关图象题注意的问题
一般说来解图象题的大致方法如下:
(1)一看面,即认准横坐标、纵坐标各表示什么量。
(2)二看线,即看清曲线的起点位置及曲线的变化趋势,确定函数曲线的增减性。弄清曲线斜率大小即曲线“平”与“陡”的意义。
(3)三看点,即准确把握各特殊点包含原点、曲线的拐点、最高点的含义。
(4)四看要不要作辅助线(如等温线、等压线),并看清定量图象中有关量的多少。
(5)认准某些关键数据在解题中的特定作用。
(6)全面、准确地从图中找出直接或隐含的化学相关知识。
例1、100 mL 6 mol·L-1的硫酸与过量的锌粉反应,在一定温度下,为了减缓反应速率,但又不影响生成气体的总量,可向反应物中加入适量的 ( )
A.硫酸钠(固体) B.水 C.硫酸钾溶液 D.硫酸铵(固体)
答案:BC
[解析]A选项中Na2CO3固体虽然能减小c(H+),但使H+的物质的量减少,进而影响了氢气的总量。D选项,硫酸铵固体不但不会减小c(H+),反而能使H+的量增大,影响氢气的量。B、C两个选项,实质都是用水把盐酸稀释了,但没有影响氢气的总量,因而正确选项为B、C。
[答案]B、C
[点评]本题主要考查浓度对化学反应速率的影响,主要分两个层次:一是减缓反应速率,二是又不影响产生气体的总量,从反应的离子方程式:Zn+2H+=Zn2++H2↑的实质上看,可采取的措施只能是减少c(H+)。
例2、反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在两升密闭容器中进行1分钟后,NH3减少了0.12 mol,则平均每秒钟浓度变化正确的是 ( )
A.NO:0.001 mol·L-1 B.H2O:0.002 mol·L-1
C.NH3:0.002 mol·L-1 D.O2:0.00125 mol·L-1
[解析]v(NH3)=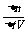 =
= 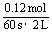 =0.001 mol·L-1·s-1
=0.001 mol·L-1·s-1
又因:υ(NH3)∶υ(O2)∶υ(NO)∶υ(H2O)=4∶5∶4∶6不难得出:
v(O2)= v(NH3)=0.00125 mol·L-1·s-1
v(NH3)=0.00125 mol·L-1·s-1
v(NO)=v(NH3)=0.001 mol·L-1·s-1
v(H2O)= v(NH3)=0.0015 mol·L-1·s-1
v(NH3)=0.0015 mol·L-1·s-1
[答案]AD
[点评]本题是考查学生对化学反应速率概念的理解情况。本题让求每秒钟浓度变化,其实质就是求反应速率。
例3、 某温度时,在2L容器中X、Y、Z三种物质的物质的量随时间的变化关系曲线如图所示。

(1)由图中的数据分析,该反应的化学方程式为 ___________
(2)反应开始至2min、5minZ的平均反应速率为 、 ;
(3)5min后Z的生成速率比5min末Z的生成速率 (大、小、相等)。
[解析] 回答第一个问题,首先要根据X、Y的物质的量的减少,Z的物质的量增加,分析出X、Y是反应物,Z是生成物,再根据2分钟内或5分钟内物质的量的变化之比等于化学计量数之比,确定X、Y、Z的化学计量数。
第二个问题则先分别求出2min内和5min内Z的浓度变化,然后根据公式求出反应速率。
第三个问题要注意到从5min开始,反应达到平衡,反应速率不变。
(1)由X、Y的物质的量的减少,Z的物质的量增加,说明X、Y是反应物,Z是生成物, 5分钟内X、Y、Z物质的量的变化之比=化学计量数之比=0.6mol:0.2mol:0.4mol=3:1:2,所以,该反应的化学方程式为:
3X+Y 2Z
2Z
(2)反应开始至2min,△n(Z)=0.2mol,
△c(Z)=0.2mol/2L=0.1 mol·L-1,
v(Z)=0.1 mol·L-1/2min=0.05 mol/(L·min)
5min 时,△n(Z)=0.4mol,
△c(Z)=0.4mol/2L=0.2 mol/L
v(Z)=0.2 mol·L-1/5min=0.04 mol/(L·min)
(3)5min时,反应达到了平衡,各物质的反应速率不再改变,故5min后Z的生成速率与5min末Z的生成速率相等。
[答案](1)3X+Y 2Z (2)0.05 mol/(L·min),0.04 mol/(L·min) (3)相等
2Z (2)0.05 mol/(L·min),0.04 mol/(L·min) (3)相等
[点评]解图象题时要注意挖掘隐藏在图象中的条件。
例4、二氧化氮在加热条件下能够分解成一氧化氮和氧气。该反应进行到45 s时,达到平衡(此时NO2的浓度约为0.0125 mol·L-1)。下图中的曲线表示二氧化氮分解反应在前25 s内的反应进程。

(1)请计算前20 s内氧气的平均生成速率;
(2)若反应延续到70 s,请在图中用实线画出25 s至70 s的反应进程曲线。
(3)若反应开始时加入催化剂(其他条件不变),请在图上用虚线画出加入催化剂后的反应进程曲线。
[解析](1)v(O2)= v(NO2)=
v(NO2)=  ×
× =5.5×10-4mol·L-1·s-1
=5.5×10-4mol·L-1·s-1
(2)因为45 s时达平衡,此时NO2的浓度为0.0125 mol·L-1,在图中45 s处画出纵坐标0.0125 mol·L-1,因平衡后各自的浓度将不再变化,在70 s处,再画出纵坐标为0.0125 mol·L-1的点,把纵坐标为0.016 mol·L-1(20 s时)、0.0125 mol·L-1(45 s时)及0.0125 mol·L-1(70 s时)三个点相连即得如上图所示的曲线。
(3)催化剂能同等程度地改变正逆反应速率缩短了化学反应达平衡的时间,但不会改变化学平衡状态,平衡时间前移,但NO2的平衡浓度仍保持0.0125 mol·L-1,从而得出如上图虚线部分的曲线示意图。
[答案](1)5.5×10-4mol·L-1·s-1
( 2)如下图
(3)如下图虚线部分
二氧化碳的浓度与时间的关系
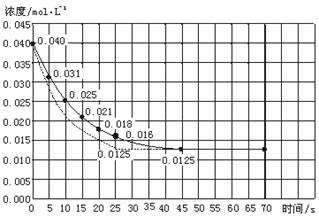
[点评]本题考查了学生对化学反应速率的掌握以及平衡时速率特点和催化剂对反应速率的影响,同时也考查了学生识图、绘图的能力。
 例5、一定温度下,下列叙述不能作为可逆反应A(g)+3B(g) 2C (g) 达到平衡状态标志的是
( )
例5、一定温度下,下列叙述不能作为可逆反应A(g)+3B(g) 2C (g) 达到平衡状态标志的是
( )
(1)C生成速率与C分解速率相等
(2)单位时间内生成amolA,同时生成3amolB
(3)A、B、C的浓度不再变化
(4)A、B、C的压强不再变化
(5)混合气体的总压不再变化
(6)混合气体的物质的量不再变化
(7)单位时间内消耗amoA,同时生成3amolB
(8)A、B、C的分子数之比为1:3:2。
A. (2) (8) B. (1) (6) C.(2) (4) D. (3) (8)
[解析]一个可逆反应达到化学平衡状态的标志是:①v(正)=v(逆),但必须是同一物质;②反应混合物中各组分的百分含量保持不变,另外,还可以再演变出其它一些判断依据,由于该反应前后气体的物质的量发生了变化,所以,只有平衡状态时,气体的总物质的量、总体积、总压强、密度等不发生变化,这些方面也可以作为平衡状态的标志。因此,(1)、(3)、(4)、(5)、(6)、(7)达到平衡,(2)、(8)不能确定,答案为A
[答案]A
[点评] 一个可逆反应达到化学平衡状态时,v(正)=v(逆)是对同一物质或者是化学计量数相同的物质而言的,对化学计量数不同的物质就要换算成同一物质进行比较,看是否相等;对于反应前后气体体积不等的反应,还可以根据气体的总物质的量、总体积、总压强、密度不变来判断,但对于反应前后气体体积相等的反应则不行。
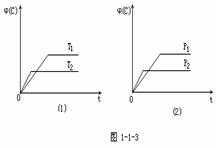
例6、 可逆反应mA(固)+nB(气)  eC(气)+fD(气)反应过程中,当其他条件不变时,C的体积分数j(C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是
( )
eC(气)+fD(气)反应过程中,当其他条件不变时,C的体积分数j(C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是
( )
 A.达到平衡后,若使用催化剂,C的体积分数将增大
A.达到平衡后,若使用催化剂,C的体积分数将增大
B.当平衡后,若温度升高,化学平衡向逆反应方向移动
C.化学方程式中,n>e+f
D.达到平衡后,增加A的质量有利于化学平衡向正反 应方向移动
[解析] 从(1)图中应先判断出T1与T2温度的大小关系。在其他条件不变时,温度升高,反应速率变大,达到平衡时间越短。由此可知,T2>T1。从图(1)分析可知温度较高时j(C)变小,说明升高温度时,平衡向逆反应方向移动,所以该正反应是放热反应。B选项是正确的。从(2)图中,应先判断出P1与P2大小关系。在其他条件不变情况下,压强越大,达到平衡的时间就越短,由此可知P2>P1。从图中可知,压强增大时j(C)变小,说明增大压强平衡向逆反应方向移动,逆反应方向是气体体积减小方向,即n<e+f,C项错误。由于使用催化剂,并不影响化学平衡的移动,A项错误。在化学平衡中,增大或减小固体物质的质量不影响化学平衡的移动。因此D项错误。
[答案] B
[点评]本题是一道图象题,考查了温度、压强、催化剂对平衡的影响。
例7、某温度时,在一个定容器中放入3L的A和1L的B,充分反应后,建立如下平衡:3A(g)+B(g)  xC(g)+yD(g) 平衡时测得混合气体中D的质量分数为n%。如果现在把0.6L的A、0.2L的B、0.8L的C和wL(w≤1.6)的D气体,在相同温度下放入相同的容器中,当反应达平衡时,测得混合气体中D的质量分数也是n%。
xC(g)+yD(g) 平衡时测得混合气体中D的质量分数为n%。如果现在把0.6L的A、0.2L的B、0.8L的C和wL(w≤1.6)的D气体,在相同温度下放入相同的容器中,当反应达平衡时,测得混合气体中D的质量分数也是n%。
(1)请将x、y、w可能的组合数值填入下表(有几组就填几组)
|
组号 |
x |
y |
w |
|
① |
|
|
|
|
② |
|
|
|
|
③ |
|
|
|
|
④ |
|
|
|
|
⑤ |
|
|
|
|
⑥ |
|
|
|
(2) 若对(1)中某一平衡体系,在温度不变的情况下,设法使容器体积逐渐减小(增大压强),结果发现,平衡先向正反应方向移动,后又向逆反应方向移动。则
x= y= ;后来平衡向逆反应方向移动的原因是 。
[解析]本题是涉及到阿佛加德罗定律、等效平衡的综合性较强的化学平衡题。属较难题。
题(1):根据阿佛加德罗定律,同温同压下两种气体的体积比等于它们的物质的量比,题目中原起始加入的3LA和1LB的体积比为3∶1,其物质的量比也应为3∶1。因此,为了讨论方便,我们就可以将题中的所有体积单位L用mol来代替。
首先分析在什么情况下平衡时D的质量分数不变。
①当C和D的物质的量比恰好等于x∶y,且C和D恰好完全转化为 A和B,此时若A的总物质的量为3mol,B的总物质的量为1mol,则与原起始加入的3molA和1molB等效。反应达平衡时D的质量分数都应为n%.即等效平衡。
②当可逆反应3A(g)+B(g)  xC(g)+yD(g) 两边气态物质前计量数之和相等时,也就是
xC(g)+yD(g) 两边气态物质前计量数之和相等时,也就是
3 + 1 = x + y 。对原起始加入3molA和1molB的平衡体系,设法增大容器体积或减小容器体积(改变压强),显然平衡是不移动的。D的质量分数仍为为n%.若起始加入6molA和2molB当反应达平衡时D的质量分数为多少?同样道理,平衡时D的质量分数还是n%。这就是说,若起始只加入A、B且物质的量之比等于3∶1,达平衡时D的质量分数定是n%。
因此,只要起始加入A、B的物质的量之比等于3∶1,C、D的物质的量之比等于x∶y,反应达平衡时D的质量分数定为n%。
解答本题现在可归结为二种情况:
① 当x + y ≠ 4 时(由等效平衡讨论)
3A(g) + B(g)  xC(g) + yD(g)
xC(g) + yD(g)
3 1 x y
3-0.6 1-0.2 0.8 w
3/2.4= x/0.8 x=1 1/0.8= y/w w=0.8 y
由w=0.8 y讨论:
当 x=1 y=1 时 w=0.8
当 x=1 y=2 时 w=1.6
当 x=1 y≥3 时 w≥2.4>1.6(不合题意)
② 当x + y = 4 时
3A(g) + B(g)  xC(g) + yD(g)
xC(g) + yD(g)
x y
0.8 w
x/0.8= y/w w=0.8 y/ x
讨论:
当 x=1 y=3 时 w≥2.4>1.6(不合题意)
当 x=2 y=2 时 w=0.8
当 x=3 y=1 时 w=0.27
综上所述,题(1)的答案应为四组:
|
组号 |
x |
y |
w |
|
① |
1 |
1 |
0.8 |
|
② |
1 |
2 |
1.6 |
|
③ |
2 |
2 |
0.8 |
|
④ |
3 |
1 |
0.27 |
|
⑤ |
|
|
|
|
⑥ |
|
|
|
题(2):增大压强平衡先向正反应方向移动,说明只有题(1)答案中的组号①②符合题意。即 x=1 y=1和2。后来平衡向逆反应方向移动的原因是:由于压强的不断增大A或A和B液化(可以有如下五种情况:①A液化而B、C、D没有液化 ②A、C液化而B、D没有液化 ③A、B液化而C、D没有液化 ④A、B、D液化而C没有液化 ⑤A、B、C液化而D没有液化)。
[答案](1)
|
组号 |
x |
y |
w |
|
① |
1 |
1 |
0.8 |
|
② |
1 |
2 |
1.6 |
|
③ |
2 |
2 |
0.8 |
|
④ |
3 |
1 |
0.27 |
|
⑤ |
|
|
|
|
⑥ |
|
|
|
(2)x=1 y=1和2 由于压强的不断增大A或A和B液化
[点评]通过以上一道平衡题的解析,我们应该认识到,要使平衡混合气体中某物质的质量分数保持不变,除了要考虑到等效平衡外,还要注意到平衡不发生移动的等效因素。另外,还要能用辩证的观点去分析事物的变化,不可犯教条主义的错误。
例8、在一个容积固定的反应器中,有一个可左右移动的密闭隔板,两侧分别进行如图所示的可逆反应。
各物质的起始加入量如下:A、B和C均为4.0 mol,D为6.5 mol,F为2.0 mol,设E为x mol,当x在一定范围内变化时,均可通过调节反应器温度,使两侧反应都达平衡,并且隔板恰好处于反应器的正中位置。请填写下列空白:

(1)x=4.5,则右侧反应在起始时向 (填“正反应”或“逆反应”)方向进行。欲使起始反应维持向该方向进行,则x的最大取值应小于 。
(2)若x分别为4.5和5.0,则在这两种情况下,当反应达平衡时,A的物质的量是否相等? (填“相等”“不相等”或“不能确定”),其理由是 。
[解析]由题意可知,隔板处于中间,它反映了左右两室有一个等量关系,即物质的量相等,而左室中的反应是一个反应前后气体的物质的量不变的反应,其物质的量之和总保持12 mol不变。这就要求右室达到化学平衡时,其物质的量总和也必为12 mol,才能保证隔板处于中间位置,再根据反应的可逆特点确定x的取值范围。
(1)当x=4.5时,右室中总的物质的量为:4.5+6.5+2=13>12,要想使隔板处于中间,平衡需向正反应方向进行。
设x的最大值为a mol,D的转化量为y mol,则有:
D+ 2E  2F
2F
平衡时 6.5-y?a-2y? ? 2+2y
依题意有:
?(6.5-y)+(a-2y)+(2+2y)=12 ①(根据隔板处于中间,左右两室物质的量相等)
?a-2y>0 ②(根据化学平衡特点,不可极限转化)
联立①②解得:a<7.0,即x的最大值应小于7.0。
[答案]1)正反应 7.0 (2)不相等 因为这两种情况是在两个不同的温度下达到化学平衡的,平衡状态不同,所以物质的量也不同
[点评]此题难度较大,解此类题常用方法为极端假设法和不为0原则。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com