
15.已知下列两个热化学方程式:2H2(g)+O2(g)=2H2O(I);△H=-571.6 kJ/mol
CaH8(g)+5O2(g)=3CO2(g)+4H2O(1);△H=-2220 kJ/mol实验测得氢气和丙烷的混合气体共5 mol完全燃烧时放出3847 kJ的热量,则混合气体中氢气与丙烷的体积比是 ( )
A.l:3 B.3:1 C.1:4 D.1:1
14.下列实验设计和结论相符的是 ( )
A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中
B.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性
C.某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42-
D.在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到较纯净的FeCl3溶液
13.已知反应:(1)10IkPa时;2C(S)+O2( g)=2CO(g) △H=-221kJ/mol
(2)在稀溶液中:H+(aq)+OH-(aq)=H2O(1);△H=-57.3kJ/mol下列结论正确的是 ( )
A.碳的燃烧热大于110.5kJ/mol
B.反应(1)的反应热为221 kJ/mol
C.稀硫酸和稀NaOH溶液反应的中和热为-57.3 kJ/mol
D.稀醋酸和稀NaOH溶液反应生成1 mol水,放出57.3kJ热量
12.含有a mol FeBr2的溶液中,通入x mol C12。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是 ( )
A.x=0.4a,2Fe2++C12=2Fe3++2C1-
B.x=0.6a, 2Br-+Cl2=Br2+2Cl-
C.x=a, 2e2++2Br-+2Cl2=Br2+2Fe3++4Cl-
D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-
11.C3N4和Sl3N4晶体中结构相似,是新型的非金属高温陶瓷材料,下列说法正确的是
( )
A.C3N4和Sl3N4晶体中N的化合价为+3价
B.C3N4和Si3N4 晶体中含有共价键
C.C3N4晶体的硬度比Si3N4晶体的硬度小
D.C3N4和Si3N4晶体均为分子晶体
10.下列有关比较中,大小顺序排列错误的是 ( )
A.物质的沸点:HF<HCI<BBr <HI
B.物质的熔点:汞<冰<食盐<石英
C.结合H+的能力:SO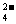 < CH3COO-<CO
< CH3COO-<CO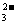
D.分散系中分散质粒子的直径:FeCl3;溶液<Fe(OH3胶体<+Fe(OH3悬浊液
9.下列各组试剂在溶液中反应,当两种试剂的量发生改变时,不能用同一离子方程式表示的是 ( )
A.氢氧化钠和硫酸铝 B.氢氧化钠和氯化镁
C.硫酸钠和氧氧化钡 D.氯化铝和氨水
8.下列离子方程式书写正确的是 ( )
A.NaHCO3溶液中加入少量NaHSO4溶液:HCO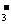 +HSO
+HSO =SO
=SO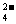 +H2O
+H2O
B.Ca(HCO3)2溶液中辊入少量Ca(OH)2溶液:Ca2++OH-+HCO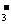 =CaCO3↓+H2O
=CaCO3↓+H2O
C.金属铝溶于氧化钠溶液:2Al+6OH-=2AlO +3H2↑
+3H2↑
D.Fel2溶液中通入少量Cl2:2Fe2++Cl2=2Fe3+=2Cl-
7.下列有关工业生产的叙述正确的是 ( )
A.合成氮生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率
B.硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量
C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室
D.电解精练铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小
6.关于下列反应:14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4说法正确的是( )
A.Cu2S既是氧化产物又是还原产物
B.产物中的SO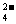 有一部分是氧化产物
有一部分是氧化产物
C.5 mol FeS2发生反应,有10 mol电子转移
D.FeS2只剩还原剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com