
11、(2010·通化模拟)有200mL氯化镁和氯化铝混合液,其中c(Mg2+)为0.2mol/L,c(Cl-)为1.3mol/L。要使Mg2+全部转化为沉淀分离出来,至少需加4mol·L-1NaOH溶液的体积为 ( )
A.40mL B.72mL C.80mL D.128mL
[解析]选C。本题考查镁和铝的性质,简单的计算。由题意可知c(Al3+)为0.3mol/L,要想Mg2+全部转化为沉淀分离出来,Mg2+需要NaOH为0.08mol,Al3+需要NaOH为0.24mol,共需要NaOH为0.32mol 所以至少需加4mol·L-1NaOH溶液的体积为80mL,选C。
10、(2010·河北衡水模拟)室温时,向体积均为1L、pH=2的盐酸中分别加入0.02mol金属M,反应完毕后再分别加入0.01mol金属N,则两次加入金属的全过程中,放出气体最多的是 ( )
|
|
A |
B |
C |
D |
|
第一次加入M |
Zn |
Na |
K |
Mg |
|
第二次加入N |
Al |
Mg |
Al |
Na |
[解析]选C。
9、(2010·广州模拟)下列叙述正确的是 ( )
A.氯水通入SO2后溶液的酸性减弱
B.向明矾溶液中加入过量NaOH溶液会产生大量白色沉淀
C.Na、Mg、Fe等金属在一定条件下与水反应都生成H2和对应的碱
D.浓硫酸、浓硝酸在加热条件下能将木炭氧化为二氧化碳
[解析]选D。本题考查元素化合物的性质,较易题。A项中氯水和SO2反应会生成盐酸和硫酸,使酸性增强。B项中生成的氢氧化铝会溶解在过量的NaOH溶液中生成偏铝酸钠。C项中Fe与水反应生成的是四氧化三铁和H2,不是H2和对应的碱。所以选D。
8、(2010·唐山模拟)下列有关化学用语使用正确的是 ( )
 A.质量数为37的氯原子: Cl
A.质量数为37的氯原子: Cl

 B.Al(OH)3的电离方程式:H++AlO2-+H2O
Al(OH)3 Al3++3OH-
B.Al(OH)3的电离方程式:H++AlO2-+H2O
Al(OH)3 Al3++3OH-
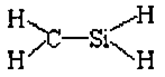
C.CH4Si的结构式:
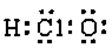
D.次氯酸分子的电子式:
[解析]选B。A项中质子数与质量数位置颠倒;C项C、Si原子间应该为双键;D项Cl、O原子位置颠倒。
7、(2010·三明模拟)不能实现下列物质间直接转化的元素是 ( )

A.碳 B.氮 C.硫 D.铝
[解析]选D。碳氮硫三种元素均可先与氧气生成较低价态的氧化物后还能再和氧气生成较高价态氧化物,然后与水反应生成酸;只有铝元素氧化物只有一种,选D。
6、(2010·南通模拟)某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图像如图所示,下列说法正确的是 ( )
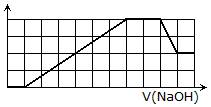
A.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+
B.原溶液中一定含有SO42-和Na+
C.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
D.反应最后形成的溶液中含有的溶质为Na2SO4
[解析]选C。由图像可得原溶液中含有的阳离子有H+、NH4+、Fe3+、Al3+,A项错误;原溶液中一定含有SO42-不一定含有Na+,B项错误;反应最后形成的溶液中含有的溶质为Na2SO4和NaAlO2,D项错误。
5、(2010·湖南师大附中模拟)等质量的下列物质分别与等浓度的NaOH溶液反应至完全溶解,消耗碱量最
多的是 ( )
A.Al B.Al(OH)3 C.AlCl3 D.Al2O3
[解析]选A。
4、(2010·南开中学模拟)下列叙述正确的有 ( )
A、等物质的量IO3-、MnO4- 中加入足量KI,二者产生I2一样多(已知:MnO4-→Mn2+)
B、常温下,C(OH-)=10-12 mol/L的溶液是碱性溶液
C、加入Al,产生H2的溶液,可以大量存在K+、Na+、SO42-、NO3-
D、等体积、等物质的量浓度AlCl3与NaOH溶液混合的离子方程式:Al3++3OH-=Al(OH)3↓
[解析]选D。IO3-中加入足量KI后生成的I2 要比MnO4- 中加入足量KI生成的I2多,A项错误;常温下,C(OH-)=10-12 mol/L的溶液是酸性溶液,B项错误;加入Al,产生H2的溶液可能是酸性溶液,也可能是碱性溶液,如果是酸性溶液,溶液中不可能存在NO3-,C项错误。
3、(2010·济南模拟) 将等物质的量的镁和铝均匀混合,取等质量该混合物四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是 (
)
将等物质的量的镁和铝均匀混合,取等质量该混合物四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是 (
)
A.3 mol·L HCl溶液 B.4 mol·LHNO3溶液
C.5 mol·L NaOH溶液 D.18.4 mol·L H2SO4溶液
[解析]选A。本题考查金属的性质,较易题。B项中硝酸和D项中浓硫酸与金属反应不产生氢气;C项中NaOH溶液只与铝反应而不与镁反应,而A项中HCl溶液与镁和铝均能反应,A项正确。
2、(2010·郑州模拟)Al、Mg混合物与适量的稀硫酸恰好完全反应,将反应后的溶液蒸干,所得固体质量比原固体增加了4.8g,则该混合物的物质的量可能为 ( )
A.0.04mol B.0.03mol C.0.06mol D.0.05mol
[解析]选A。由题意知所得的固体为Al2(SO4)3、MgSO4,SO42-的物质的量为4.8/96=0.05mol,若固体全部是MgSO4则固体的物质的量为0.05mol,若固体全部是Al2(SO4)3则固体的物质的量为0.0333mol。故混合物的物质的量在0.0333mol和0.05mol之间,选A。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com