
7.同温同压下,下列各组热化学方程式中,△H1<△H2是
A.C(s)+ O2(g)=CO(g);△H1
C(s)+O2(g)=CO2(g);△H2
O2(g)=CO(g);△H1
C(s)+O2(g)=CO2(g);△H2
B. H2(g)+
H2(g)+ Cl2(g)=HCl(g);△H1 H2(g)+Cl2(g)=2HCl(g);△H2
Cl2(g)=HCl(g);△H1 H2(g)+Cl2(g)=2HCl(g);△H2
C.2H2(g)+O2(g)=2H2O(g);△H1 2H2(g)+O2(g)=2H2O(l);△H2
D.S(g)+O2(g)=SO2(g);△H1 S(s)+O2(g)=SO2(g); △H2
6.一定温度下,在体积为10L的密闭容器中,2molO2和2molSO2混合气体发生如下反应:2SO2(g)+ O2(g)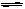 2SO3(g),半分钟后,体系中O2的物质的量变为1.4mol,则此反应的平均速率为
2SO3(g),半分钟后,体系中O2的物质的量变为1.4mol,则此反应的平均速率为
A.v(O2) = 0.002mol/(L•s) B.v(SO2) = 0.002 mol/(L•s)
C.v(O2) = 0.02 mol/(L•s) D.v(SO3) = 0.04 mol/(L•s)
5. 作为应对油气时代过后能源问题的一条解决途径,甲醇受到越来越多的关注。已知在常温常压条件下,1gCH3OH(l)完全燃烧释放出22.7kJ的热量,则表示甲醇燃烧热的热化学方程式为
作为应对油气时代过后能源问题的一条解决途径,甲醇受到越来越多的关注。已知在常温常压条件下,1gCH3OH(l)完全燃烧释放出22.7kJ的热量,则表示甲醇燃烧热的热化学方程式为
A.CH3OH(l) + O2(g) == CO2(g) + 2H2O(l);△H=-726.4kJ/mol
 B.2CH3OH(l) + 3O2(g)
== 2CO2(g) + 4H2O(g);△H=-1452.8kJ/mol
B.2CH3OH(l) + 3O2(g)
== 2CO2(g) + 4H2O(g);△H=-1452.8kJ/mol
C.CH3OH(l) + O2(g) == CO2(g) + 2H2O(l);△H=726.4kJ/mol
D.2CH3OH(l) + 3O2(g) == 2 CO2(g) + 4H2O(l);△H=-1452.8kJ/mol
4. 相同温度条件下,c(H+)均为0.1mol/L的①盐酸②醋酸溶液各100mL分别和0.3g 锌反应,下列说法中正确的是
A.①中锌消失的快 B.②锌消失的快
C.①中产生的氢气多 D.②中产生的氢气多
3.一定温度下,固定体积的容器中充入1molSO2和1molO2,再加入少量的NO,在体系中发生①2NO+O2=2NO2;②SO2+NO2=SO3+NO,下列说法错误的是
A.体系中的总反应是:2SO2+ O2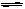 2SO3
2SO3
B.在反应过程中NO是催化剂
C.NO参与反应历程,降低反应活化能,加快反应速率
D.NO的引入可以增加SO2的平衡转化率
2.已知H+(aq)+OH-(aq)=H2O(l) △H=-57.3 kJ/mol。下列关于中和热的说法中正确的是
A.在稀溶液中所有酸和碱反应的中和热数值都相等
B.在稀溶液中1mol酸和1mol碱反应放出的热量都相等
C.在稀溶液中HCl和NaOH反应、HNO3和KOH的反应的中和热相等
D.将浓硫酸滴入稍过量的氢氧化钠溶液中刚好生成1mol水时,产生的热量即中和热
1.下列说法不正确的是
A.化学反应过程中的能量变化除了热能外,也可以是光能、电能等
B.吸热反应一定不能在常温下进行
C.需要加热才能进行的反应不一定是吸热反应
D.反应物总能量高于生成物总能量的反应是放热反应
22.(14分)已知函数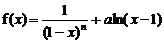 ,其中n∈N+,
,其中n∈N+, 为常数。
为常数。
①当n=2时,求函数f(x)的极值;
②当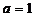 时,证明:对任意的正整数n,当x≥2时,
时,证明:对任意的正整数n,当x≥2时, 。
。



21.(12分)已知二次函数 ,同时满足:①不等式
,同时满足:①不等式 的解集有且只有一个元素;②在定义域内存在x1、x2,使得x1+x2=0,但f(x1) ≠f(x2),设数列
的解集有且只有一个元素;②在定义域内存在x1、x2,使得x1+x2=0,但f(x1) ≠f(x2),设数列 的前n项和Sn=f(n)。
的前n项和Sn=f(n)。
①求f(x)的表达式;
②求数列 的通项公式。
的通项公式。
③若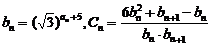 ,数列
,数列 的前n项和为Tn
,Tn>n+m,对n∈N+,n≥2恒成立,求m的范围。
的前n项和为Tn
,Tn>n+m,对n∈N+,n≥2恒成立,求m的范围。
20.(12分)设F1、F2分别是椭圆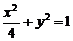 的左、右焦点。
的左、右焦点。
①若P是该椭圆上的一个动点,求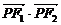 的最大值和最小值;
的最大值和最小值;
②设过定点M(0,2)的直线L与椭圆交于不同的两点A、B,且∠AOB为锐角(其中O为坐标原点),求直线L的斜率k的取值范围。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com