

17.答案:
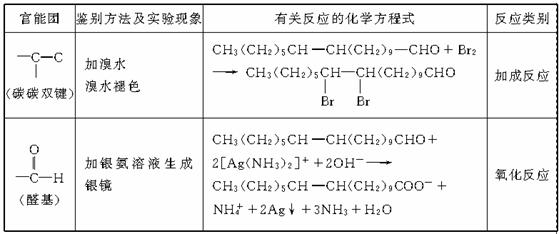
16.答案:D
解析:对各组溶液,分别采用两两混合法进行区分。D组中,硫酸镁遇氢氧化钾、碳酸钾均有白色沉淀,则硫酸镁、硫酸氢钾得以鉴别;再用硫酸氢钾与两个待检液反应,有气体产生的是碳酸钾,余下的是氢氧化钾。
15.答案:D
解析:A、B选项因是干燥的故HCl、Cl2都不作用;C项两者都生成白色沉淀。而D项HCl无变化,Cl2可使其变蓝。
14.答案:A
解析:若将KOH溶液滴加到Al2(SO4)3溶液中,边滴边振荡,所发生的现象是沉淀,然后溶解,最后沉淀消失。若将Al2(SO4)3溶液滴加到KOH溶液中,边滴边振荡,所发生的现象是,起始无沉淀产生,然后沉淀量逐渐增多,继续滴加沉淀不再增多,也不会消失。有关离子方程式为:Al3++4OH-===AlO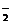 +2H2O,Al3++3AlO
+2H2O,Al3++3AlO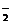 +6H2O===4Al(OH)3↓。
+6H2O===4Al(OH)3↓。
13.答案:CD
解析:对各组溶液,分别采用两两混合法进行区分。选项C中KHCO3加入NaAlO2产生白色沉淀,HCO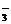 +AlO+H2O===CO
+AlO+H2O===CO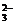 +Al(OH)3↓,加入NaHSO4溶液中产生无色气体,从而加以区分;选项D中首先观察出FeCl3溶液,然后利用FeCl3溶液鉴别出NaOH溶液,再用NaOH溶液鉴别出MgCl2溶液。
+Al(OH)3↓,加入NaHSO4溶液中产生无色气体,从而加以区分;选项D中首先观察出FeCl3溶液,然后利用FeCl3溶液鉴别出NaOH溶液,再用NaOH溶液鉴别出MgCl2溶液。
12.答案:A
解析:选项A是利用三种有机物的溶解性和密度大小加以区分,苯难溶于水比水轻,乙酸能溶于水,四氯化碳难溶于水但比水重。选项B中乙醇、乙醛、乙酸均能溶于水,难以区分;选项C中乙醛、乙二醇和选项D中乙醇、甘油皆能溶于水,无法区分。
11.答案:B
解析:一种盐溶液精制的过程,不可能用金属钠;芒硝的化学式是Na2SO4·10H2O,不能加热脱去结晶水。由此可见,凡是涉及到②、⑤两个操作步骤的选项都是不正确的选项。
10.答案:B
解析:由题给反应,要证明有IO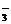 ,应用到I-、淀粉和酸。现给出了KI淀粉试纸,包括前两种试剂,所以再选用食醋(即酸)便可完成上述检验。向待测液中加入醋酸,然后将溶液滴在KI淀粉试纸上,若试纸变蓝,即证明有IO
,应用到I-、淀粉和酸。现给出了KI淀粉试纸,包括前两种试剂,所以再选用食醋(即酸)便可完成上述检验。向待测液中加入醋酸,然后将溶液滴在KI淀粉试纸上,若试纸变蓝,即证明有IO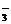 。
。
9.答案:BD
解析:根据滴加的顺序不同,产生的现象不同加以区别。B中若将稀H2SO4滴入Na2CO3溶液中,产生HCO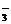 ,无明显现象;若将Na2CO3溶液滴入稀H2SO4中,则有CO2产生。D中NaAlO2溶液滴入盐酸中,无沉淀产生;而将盐酸滴入NaAlO2溶液中,则有Al(OH)3沉淀产生。
,无明显现象;若将Na2CO3溶液滴入稀H2SO4中,则有CO2产生。D中NaAlO2溶液滴入盐酸中,无沉淀产生;而将盐酸滴入NaAlO2溶液中,则有Al(OH)3沉淀产生。
8.答案:C
解析:选项A可利用其在水中溶解性和密度的大小来区分;选项B和选项D可利用其在水中的溶解性加以区分。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com