
16.(10分)现有CO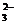 、K+、SO
、K+、SO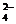 、Cl-、Al3+?、Fe3+、HCO
、Cl-、Al3+?、Fe3+、HCO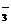 、Ba2+八种离子,试按要求填空:
、Ba2+八种离子,试按要求填空:
(1)只能与H+大量共存,不能与OH-大量共存的有__________________________。
(2)只能与OH-大量共存,不能与H+大量共存的有_______________________。
(3)既能与H+大量共存,又能与OH-大量共存的有______________________________。
(4)既不能与H+大量共存,又不能与OH-大量共存的有_____________________________。
(5)上述离子中,只要有CO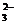 时,________________________离子肯定不能存在。
时,________________________离子肯定不能存在。
答案 (1)Al3+?、Fe3+?(2)CO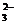 (3)K+、Cl-、SO
(3)K+、Cl-、SO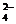 、Ba2+ (4)HCO
、Ba2+ (4)HCO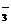 (5)Al3+、Fe3+?、Ba2+
(5)Al3+、Fe3+?、Ba2+
15.用过量的H2SO4、NaOH、NH3· H2O、NaCl等溶液,按下图所示步骤分开五种离子。则溶液①、②、③、④是 ( )
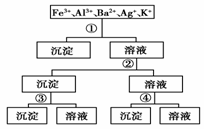 A.①NaCl ②NaOH ③NH3·H2O ④H2SO4
A.①NaCl ②NaOH ③NH3·H2O ④H2SO4
B.①H2SO4 ②NaOH ③NH3·H2O ④NaCl
C.①H2SO4 ②NH3·H2O ③NaOH ④NaCl
D.①NaCl ②NH3·H2O ③NaOH ④H2SO4
答案 D
14.将a克铁粉投入到含b克HNO3的稀硝酸溶液中,二者恰好完全反应,被还原的HNO3占总量的 ,假设HNO3的还原产物只有NO,则b∶a不可能是?
( )
,假设HNO3的还原产物只有NO,则b∶a不可能是?
( )
A.3∶1 B.4∶1 C.9∶2 D.6∶1
答案 D
13.在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+ 2As+
2As+
3SnCl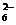 +6M,关于该反应的说法中正确的组合是
( )
+6M,关于该反应的说法中正确的组合是
( )
①氧化剂是H3AsO3;②还原性:Cl->As;
③每生成7.5 g As,还原剂失去的电子为0.3 mol;
④M为OH-;⑤SnCl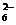 是氧化产物
是氧化产物
A.①③⑤ B.①②④⑤ C.①②③④ D.①③
答案 A
12.根据下表信息,下列叙述中正确的是 ( )
|
序号 |
氧化剂 |
还原剂 |
其他反应物 |
氧化产物 |
还原产物 |
|
① |
Cl2 |
FeBr2 |
|
FeCl3 |
|
|
② |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
MnSO4 |
|
③ |
KClO3 |
浓盐酸 |
|
Cl2 |
Cl2 |
|
④ |
KMnO4 |
浓盐酸 |
|
Cl2 |
MnCl2 |
A.表中第①组反应的氧化产物一定只有FeCl3(Fe3+)
B.氧化性强弱比较:KMnO4>Cl2>Fe3+>Br2>Fe2+?
C.还原性强弱比较:H2O2>Mn2+>Cl-
D.④的离子方程式配平后,H+的化学计量数为16
答案 D
11.(2008·潍坊模拟)某化学兴趣小组欲研究H2SO4、NaCl、KCl、Na2CO3、FeCl3、NaOH的性质,对于如何研究,他们设计了两种研究方案:
方案①:将它们按照酸、碱、盐分类,然后分别溶于水得到溶液,进行实验;
方案②:将它们按照钠盐、钾盐、铁盐和其他化合物分类,然后分别溶于水得到溶液,进行实验。
下列说法正确的是 ( )
A.常温时将少量铜粉分别投入上述溶液中,按照方案①的分类,能够完全溶解铜粉的只有酸(H2SO4)溶液和盐(FeCl3)溶液
B.设计方案②的同学取某种溶液,在其中加入上述的钾盐溶液,有白色沉淀产生,再加入稀硝酸,
沉淀不消失,则该溶液中可能含有Ag+
C.按照方案①的分类,属于碱的有Na2CO3、NaOH
D.这两组同学在研究物质性质时只使用了实验法、观察法
答案 B
10.U常见化合价有+4和+6价,硝酸铀酰[UO2(NO3)2]加热可发生如下分解反应:
 UO2(NO3)2
UxOy+NO2↑+O2↑,在600 K时,将气体产物收集于试管并倒扣水中,水充满试管,则生成的铀的氧化物化学式是
(
)
UO2(NO3)2
UxOy+NO2↑+O2↑,在600 K时,将气体产物收集于试管并倒扣水中,水充满试管,则生成的铀的氧化物化学式是
(
)
A.UO2 B.UO3 C.2UO2·UO3 D.UO2·2UO3
答案 D
9.在100 mL含等物质的量HBr和H2SO3的溶液里通入0 01 mol Cl2,有一半Br-变为Br2(已知Br2能氧化H2SO3)。原溶液中的HBr和H2SO3的浓度都等于 ( )
A.0.007 5 mol/L B.0.008 mol/L C.0.075 mol/L D.0.08 mol/L
答案 D
8.物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关。下列各组物质:
①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液
④Fe与HCl溶液由于浓度不同而能发生不同氧化还原反应的是 ( )
A.①③ B.③④ C.①② D.①③④
答案 A
7.下列反应的离子方程式正确的是 ( )
A.用铂作电极电解MgCl2溶液:2Cl-+2H2O H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
 B.硫氢化钠水解:HS-+H2O S2-+H3O+
B.硫氢化钠水解:HS-+H2O S2-+H3O+
C.硫酸氢钾溶液与过量Ba(OH)2溶液反应:H++SO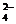 +OH-+Ba2+
+OH-+Ba2+ BaSO4↓+H2O
BaSO4↓+H2O
D.向过量氨水中滴加少量氯化铝溶液:Al3++4OH- AlO
AlO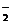 +2H2O
+2H2O
答案 C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com