
8. 碳在氧气中充分燃烧:C + O2 点燃 CO2
7. 硫粉在空气中燃烧: S + O2 点燃 SO2
6. 红磷在空气中燃烧:4P + 5O2 点燃 2P2O5
5. 氢气中空气中燃烧:2H2 + O2 点燃 2H2O
4. 铝在空气中燃烧:4Al + 3O2 点燃 2Al2O3
3. 铜在空气中受热:2Cu + O2 加热 2CuO
2. 铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O4
(1)单质与氧气的反应:
1. 镁在空气中燃烧:2Mg + O2 点燃 2MgO
19.(12分)某研究性学习小组为了验证臭氧的氧化性强于氧气,进行了下述实验,请参与探究并回答相关问题。
[实验目的]验证臭氧的氧化性强于氧气
[实验原理]2KI+O3+H2O 2KOH+I2+O2,淀粉溶液遇单质碘变蓝色。
2KOH+I2+O2,淀粉溶液遇单质碘变蓝色。
[实验用品]臭氧消毒碗柜、a溶液、碘化钾溶液、滤纸、玻璃片、温度计。
[实验步骤] ①取a溶液与碘化钾溶液混合;②取两片用滤纸剪成的纸条,在a和碘化钾的混合液中湿润后分别置于两块洁净的玻璃片上;③将一块玻璃片(Ⅰ)置于臭氧消毒碗柜中并接通电源生成臭氧。将另一块玻璃片(Ⅱ)置于可控温度的温箱里,尽量地使温箱的温度与消毒碗柜中的温度相等;
④观察现象并进行记录:
|
时间(min) |
0 |
15 |
30 |
45 |
60 |
90 |
120 |
|
|
滤纸的颜色变化 |
玻璃片(Ⅰ)上的滤纸 |
白色 |
白色 |
灰色 |
浅蓝色 |
蓝色 |
蓝色 |
浅蓝色 |
|
玻璃片(Ⅱ)上的滤纸 |
白色 |
白色 |
白色 |
白色 |
灰色 |
灰色 |
浅蓝色 |
请根据上述实验原理、步骤及你所学的知识,回答下列问题:
(1)实验原理涉及的反应类型是___________________(填序号)。
A.离子反应 B.氧化还原反应
C.复分解反应 D.置换反应
E.分解反应 F.化合反应
(2)实验药品中的a溶液是_____________________________溶液。
(3)写出在臭氧消毒柜中产生O3的化学方程式:_________________________。
(4)整个实验过程要保持两块玻璃片所在环境的温度相同的原因是______________________。
答案 (1)AB (2)淀粉
(3)3O2 2O3
(4)温度会影响反应速率,保持温度相同,是为了消除温度不同带来的误差
2O3
(4)温度会影响反应速率,保持温度相同,是为了消除温度不同带来的误差
17.(6分)某同学拟用氯化钙固体、碳酸钠溶液和稀硝酸等试剂,先制得碳酸钙,最终制得纯净的硝酸钙晶体。
(1)写出制取过程中反应的离子方程式:______________________________________。
(2)请帮助该同学完成下列实验操作步骤(不要求回答使用的仪器):
①用蒸馏水完全溶解CaCl2后,加入____________________________________;
②将反应后的混合物过滤,并用适量蒸馏水洗涤沉淀至无Cl-;
③加入_________________________________,使沉淀完全溶解;
④____________________________________,得到纯净的硝酸钙晶体。
答案 (1)Ca2++CO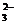
 CaCO3↓
CaCO3↓
CaCO3+2H+ Ca2++CO2↑+H2O
Ca2++CO2↑+H2O
(2)①碳酸钠溶液 ③稀硝酸 ④蒸发、结晶







 18.(12分)(1)配平下列离子方程式: I-x+ Cl2+ H2O
Cl-+
IO
18.(12分)(1)配平下列离子方程式: I-x+ Cl2+ H2O
Cl-+
IO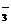 +
+
在反应中,若消耗I-x与Cl2物质的量之比为1∶8,则x=_____________。
(2)向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾),溶液会发生如下反应:
Mn2++S2O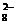 +H2O→MnO
+H2O→MnO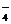 +SO
+SO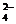 +H+
+H+
该反应常用于检验Mn2+的存在。其特征现象是__________________________,
若反应中有0.1 mol还原剂参加反应,则消耗氧化剂物质的量为_____________________mol。
(3)若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有_______________________________________。
答案 (1)2I-x+(5x+1)Cl2+6x H2O (10x+2)Cl-+2xIO
(10x+2)Cl-+2xIO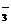 +12x H+ 3
+12x H+ 3
(2)溶液由无色变为紫色 0.25 (3)Cl2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com