
27.(10分)“嫦娥一号“卫星发射成功,标志月球探测成为中国航天的现实。
(1)“嫦娥一号”使用的燃料是液氢,助燃剂是液氧。氧气从淡蓝色液体变成无色气体发生了_________变化,氢气燃烧的化学方程式为__________________________。液态氢作燃料除燃烧时产生较大的推动力外,另一个优点是__________________。对于目前全世界出现能源危机,以及燃烧对环境的影响,我们应该合理开发利用的新能源有(至少填两种)_____________________________。
(2)月球上的3He(3表示相对原子质量)蕴藏量巨大,探月的目标之一是探测核聚变燃料3He的分布。地球上的氦元素主要以4He形式存在。从原子的构成来看,3He、4He两种原子的_________数不同,化学性质____________。
(3)“嫦娥一号”另一个目标是探测下列14种元素的含量和分布:K、Th(钍)、U(铀)、O、Si、Mg、Al、Ca、Fe、Ti(钛)、Na、Mn(锰)、Cr(铬)、Gd(钆)。其中属于金属元素的有_________种。
(4)月球表面富含钛铁矿,钛因其硬度大、熔点高、常温下耐酸碱、耐腐蚀等优良的性能,被誉为“未来金属”。我国四川省有大型钒钛磁铁矿,由钒钛磁铁矿提取金属钛的主要工艺过程如下:

①钛铁矿的主要成分是FeTiO3(钛酸亚铁),其中钛的化合价为__________价。
②TiCl4在高温下与足量Mg反应成金属Ti,该反应属于_____________(填反应类型)
③上述生产过程中得到的金属钛中混有少量金属杂质,可加入___________除去。
26.(4分)金属钠是一种活泼的金属,它能与水反应生成对应的碱和氢
气。将金属钠放入硫酸铁溶中,所发生反应的化学方程式为:
____________________________________________________________________
____________________________________________________________________。
25.(2分)(1)小张用右下图所示的实验装置来探究可燃物的燃烧条件,他能观察到的现象是:
 ___________________________________________________________________。
___________________________________________________________________。
(2)通过此实验的探究,还可推出白磷
与红磷在性质上的一点差异是_______________。
24.(4分)活性炭是防毒面具虑毒罐里的吸附剂,可用来吸附氯气等有毒气体。下表列出了一定温度和压强下每立方厘米活性炭所能吸附的常见气体的体积。
|
气体 |
二氧化碳 |
氢气 |
氧气 |
氮气 |
氯气 |
|
气体的相对分子质量 |
44 |
2 |
32 |
28 |
71 |
|
气体的沸点/℃ |
-78 |
-252 |
-183 |
-195 |
-34 |
|
被吸附体积/mL |
97 |
4.5 |
35 |
11 |
494 |
请你分析表中数据,找出活性炭吸附气体的规律。)
(1)______________________________________________________________________。
(2)________________________________________________________________________。
23.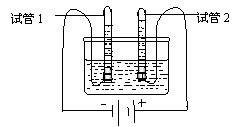 (3分)水是生命之源,人类的日常生活与工农业生产
(3分)水是生命之源,人类的日常生活与工农业生产
都离不开水,右图是实验室电解水装置,试简答:
(1)通电一段时间后,试管1中收集到的气体是_________;
(2)该实验说明水是有氢、氧两种_________组成的,
水分子是由氢、氧两种______构成的(填“分子”
“原子”或“元素”)。
22.(5分)根据Fe、Cu、Ag三种金属在金属活动顺序中的位置简答。
(1)其中金属活动性最强的金属是_________;
(2)其中(除Cu外)不能与CuSO4溶液发生反应的是_________;
(3)其中能与稀硫酸反应产生氢气的是__________;
(4)设计一个实验,证明铁的金属性比铜活泼。
____________________________________________________________________。
21.(6分)化学可以帮助人类认识改造周围的世界,促进社会发展。
(1)糖类、油脂、蛋白质和维生素都是人类的基本营养物质。下表为某品牌燕麦片标签中的一部分。
|
每100g含有营养成分 |
糖类 |
油脂 |
蛋白质 |
维生素C |
钙 |
镁 |
钠 |
锌 |
|
7.6g |
7.8g |
7.4g |
18mg |
201mg |
18.2mg |
30.8mg |
8.1mg |
①燕麦片的营养成分中能与水反应生成氨基酸的营养物质是:___________;
每克营养物质氧化时放出能量最多的是_________;
人体必需的微量元素是_______。
②维生素C易溶于水,向其水溶液中滴入紫色石蕊试液,石蕊变红色,加热该溶液至沸腾,红色消失。因此,烹调富含维生素C的食物时,应该注意_________;在碱性条件下,维生素C易被空气氧化,烧煮时最好加一点______________。
(2)我们穿的衣服通常是由纤维织成的,常见的纤维有棉花、羊毛、涤纶等。用灼烧法可初步鉴别三种纤维,给三种纤维编号后,分别灼烧产生的气味如下:
|
纤维编号 |
① |
② |
③ |
|
灼烧时的气体 |
特殊气味 |
烧纸气味 |
烧焦羽毛气味 |
则羊毛、棉花的编号分别为_________________。
20.(8分)1909年化学家哈伯在实验室首次合成了氨,2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖。
(1)将氢气和氮气在高温、高压和催化剂的条件下合成氨(NH3)。反应的化学方程式为________________________________。
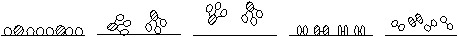
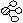
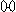
 (2)用 、 、 、分别表示N2、H2、NH3。观察下图,写出符合在催化剂表面合成氨反应过程的顺序______________(将下面五张图按反应过程顺序用序号排列)。
(2)用 、 、 、分别表示N2、H2、NH3。观察下图,写出符合在催化剂表面合成氨反应过程的顺序______________(将下面五张图按反应过程顺序用序号排列)。
① ② ③ ④ ⑤
(3)表面化学对于化学工业很重要,它可以帮助我们了解不同的过程。在潮湿的空气里,铁表面吸附了一层薄薄的水膜,同时由于空气中CO2溶解,水膜呈酸性,写出该反应的化学方程式_____________________________。
(4)在汽车排气管上安装尾气净化装置,可使尾气中的CO和NO在催化剂表面发生反应,产生两种空气组成的气体,写出该反应的化学方程式________________________。
19.(5分)金属锂(元素符号Li)在通信和航天领域中有重要用途。氢氧化锂(化学式LiOH)是一种易溶于水的白色固体,有辣味;化学性质与NaOH相似,有强碱性和腐蚀性。
(1)“辣味”属于氢氧化锂的________性质(填“化学”或“物理”);
(2)LiOH属于________类(填“氧化物”“酸”“碱”或“物理”);
(3)LiOH和NaOH都是呈碱性,是因为它们在水溶液中都能解离出________离子(填“金属”“氢”或“氢氧根”);
(4)载人航天飞船中常用LiOH代替NaOH来吸收航天员呼吸产生的CO2,则LiOH和CO2反应的化学方程式为:___________________________。
18.(6分)某地根据当地资源特点将石灰石的开采,加工和
高炉炼铁建在一起形成联产。
(1)炼铁的固体原料有铁矿石、焦炭和__________。
请写出炼铁过程中CO和Fe2O3的反应的化学方程式:_____________________________________。
(2)高炉炼铁排放的废气中含有大量的高湿一氧化碳,
可作为能源用来煅烧石灰石,请写出煅烧石灰石的
化学方程式:________________________________。
(3)此联产方式的主要优点是:____________(答出一点即可)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com