
15.某溶液含有NH4+、HCO3-、SO32-、Na+ 、HS-、NO3-六种离子。向其中加入足量的Na202粉末后,溶液中浓度变化最小的离子是
A.HCO3- B.SO32- C.Na+ D.NO3-
14.有a、b、c、d四种金属,将a与b用导线连接起来,浸入电解质溶液中,b不易腐蚀;将a、d分别投入等浓度盐酸中,d比a反应激烈;将铜浸入b的盐溶液中,无明显变化;若将铜浸入c的盐溶液中,有金属c析出,据此判断它们的活动性由强到弱的顺序是:
A.dcab B.dabc C.dbac D.badc
13.某溶液滴入甲基橙显红色,在这种溶液中能大量共存的离子是
A.Mg2+、K+、Br-、SO42- B.S2O32-、Na+、H+、Cl-
C.Ca2+、K+、ClO-、I- D.Al3+、K+、AlO2-、Cl-
12.下列叙述正确的是
A、元素的单质不能通过氧化含该元素的化合物制得
B、得电子越多的氧化剂,其氧化性就越强
C、阳离子只能得到电子被还原,只能作氧化剂
D、含有最高价元素的化合物不一定具有强的氧化性
11.下列各装置中都盛有0.1 mol·L-1 的NaCl溶液,放置一定时间后,锌片的腐蚀速率由快到慢的顺序是
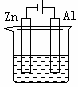
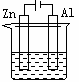
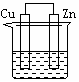
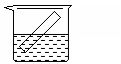
① ② ③ ④
A.③①④② B.①②④③ C.①②③④ D.②①④③
10.为了更好地表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG=lg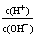 。已知某无色溶液的AG=12,则在此溶液中能大量共存的离子组是
。已知某无色溶液的AG=12,则在此溶液中能大量共存的离子组是
A.Na+、AlO2-、K+、NO3- B.MnO4-、K+、SO42-、Na+
C.Mg2+、SO42-、HCO3-、Na+ D.NH4+、NO3-、Al3+、Cl-
9.在含有Cu(NO3)2、Mg(NO3)2和AgNO3的溶液中加入适量锌粉,首先置换出的是
A.Mg B. Cu C. Ag D. H2
8.为确定某溶液的离子组成,进行如下实验:
①测定溶液的pH,溶液显强碱性。
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体。
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀。
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀。
根据实验以下推测正确的是
A.一定有SO32-离子 B.一定有CO32-离子
C能确定Cl-离子存在 D.不能确定HCO3-离子是否存在
7.下列离子方程式中正确的是
A.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O
B.Ca(HCO3)2与过量Ca(OH)2溶液反应:
Ca2++HCO3-+2OH-=CaCO3↓+CO32-+2H2O
C.Na2CO3溶液中通入少量CO2:CO32-+CO2+ H2O=2HCO3-
D.CH3COOH溶液与NaOH溶液反应:H++ OH-=H2O
6.下列化工生产过程中所发生的主要化学反应不属于氧化还原反应的是 ( )A.用氯气和消石灰制漂白粉 B.铝热法冶炼金属铝
C.用油脂制肥皂 D.电解饱和食盐水制烧碱
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com