
4.pH = 4的盐酸用水稀释100倍、1000倍、10000倍,pH值各为多少?
3.在800C时,纯水的pH小于7,为什么?(因为水的电离过程是吸热过程,所以升高温度,平衡右移,使c(H+)=c(OH-)>10-7 mol/L,所以pH小于7)
2.250C时,10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH与强碱的pH之间应满足的关系是什么?(pH酸+pH碱=15)
(1)两强酸等体积混合 混合后的pH=小的+0.3
(2)两强碱等体积混合 混合后的pH=大的-0.3
(3)当按所给反应物质的量之比计算时,酸碱不论强弱,谁大谁过剩,溶液呈谁性。
(4)酸碱等体积混合①pH = 2 某酸与pH = 12 某碱混合pH难定②pH = 4 某酸与pH = 10 NaOH混合 pH≤7③pH = 4 H2SO4与pH = 10 某碱混合pH≥7④0.01mol/L pH = 2 一元酸与0.1mol/L pH = 12一元碱混合pH = 7
(5) pH 减小一个单位,[H+]扩大为原来的10倍。 PH增大2个单位,[H+]减为原来的1/100
(6)稀释规律:分别加水稀释m倍时,溶液的物质的量的浓度均变为原来的 1/m , 强酸中c(H+)变为原来的1/m ,但弱酸中c(H+)减小 小于m倍,故稀释后弱酸酸性强于强酸。
例1、求下列溶液的pH:
(1)某H2SO4溶液的浓度是0·005mol/L ①求此溶液的pH②用水稀释到原来体积的100倍
③再继续稀释至104倍
(2)pH=3的盐酸与pH=5的硫酸等体积混合
(3)pH=10和pH=12的两种NaOH溶液等体积混合
(4)pH=12的NaOH和pH =4的HCl等体积混合
解析:(1)① c(H+)=0·005mol/L×2=0·01 mol/L ,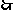 pH=-lg10-2=2
pH=-lg10-2=2
② c(H+)=0·01mol/L÷100=10-4 mol/L ,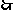 pH=-lg10-4=4
pH=-lg10-4=4
③ pH=7(强调酸稀释后不会变成碱!)
(2)c(H+)=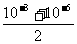 =5×10-4,
=5×10-4, 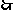 pH=-lg(5×10-4)=4-lg5=3·3
pH=-lg(5×10-4)=4-lg5=3·3
(强调10-3是10-5的100倍,所以10-5可以忽略不计)
(3)因为溶液呈碱性c(OH-)=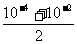 =5×10-3
=5×10-3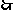 c(H+)=
c(H+)=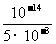 =2×10-12
=2×10-12
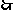 pH=-lg(2×10-12)=12-lg2=11·7
pH=-lg(2×10-12)=12-lg2=11·7
(4)NaOH中c(OH-)=10-2 mol/L HCl中c(H+)=10-4 mol/L二者等体积反应,碱过量,反应后溶液呈碱性。所以反应后c(OH-)=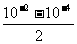 =5×10-3
=5×10-3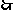 c(H+)=
c(H+)=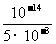 =2×10-12
=2×10-12 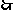 pH=-lg(2×10-12)=12-lg2=11·7
pH=-lg(2×10-12)=12-lg2=11·7
例2、某温度下纯水的C(H+)=2.0╳10-7mol/L,则此时C(OH‑)为多少?若温度不变,滴入稀H2SO4,使C(H+)=5.0╳10-4mol/L,则由水电离产生的C(H+)为多少?
答案: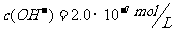 ;
;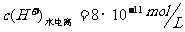 。
。
例3、
常温下,将pH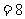 的NaOH与pH=10的NaOH溶液等体积混合后,溶液中氢离子浓度最接近(D)A.
的NaOH与pH=10的NaOH溶液等体积混合后,溶液中氢离子浓度最接近(D)A. 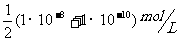 B.
B. 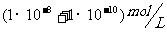
C. 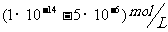 D.
D.
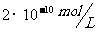
例4、pH=13的强碱溶液与pH=2的强酸溶液混合,所得溶液的pH=11,则强碱与强酸的体积比是
A、11:1 B、9:1 C、1:11 D、1:9
答案:D
例5、常温时某溶液中,测得由水电离出的C(H+)为10-11mol/L,则对此溶液的下列叙述中,正确的是( C D )
A、一定是酸溶液 B、一定是碱溶液 C、可能是pH=3的酸溶液 D、可能是pH=11的碱溶液
例6、将pH=5的盐酸溶液稀释1000倍后,溶液的pH为( C )
A、等于8 B、等于7 C、接近7又小于7 D、大于7而小于8
例7、有PH相等的盐酸和醋酸(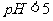 ),如何通过实验的方法证明。
),如何通过实验的方法证明。
解析:经分析可知一为强酸(盐酸),强电解质,另一为弱酸(醋酸),弱电解质。利用二者在电离过程中的区别,可用稀释相同倍数后测pH的方法进行鉴别。
答案:取相同体积的两种酸,加水稀释10倍,用玻璃棒分别蘸取稀释后两种酸,点在PH试纸上,稍后与比色卡比较,其中PH较小的为醋酸,另一为盐酸。

练习:
1.在250C某稀溶液中,由水电离产生的c(H+)=10-13mol/L,下列有关溶液的叙述正确的是(CD) A.该溶液一定呈酸性 B.该溶液一定呈碱性
C.该溶液的pH可能约为1 D.该溶液的pH可能约为13
(1)酸I+酸II [H+]
= 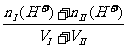
(2)碱I+碱II [OH-]
= 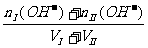
(3)酸I+碱II
完全中和:[H+] = [OH-]
= 1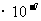 mol/L
mol/L
酸过量: [H+]= 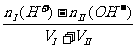
碱过量:[OH-] = 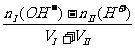
孔子曰:“三人行,必有我师焉。择其善者而从之,其不善者而改之。”其中“择善”含意深刻,使人大有所悟。在生活中我们需择善人而交,择善书而读,择善言而听,择善事而行,“择善”在我们生活中尤其重要,请以“择善”为话题,写一篇作文。题目自拟,立意自定,不少于800字。
3、
2、
1、
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com