
38.(6分)某二价金属氧化物(MO)5g与45g稀硫酸恰好完全反应,测得反应后溶液中溶质的
质量分数为30%.求:
(1)该金属的相对原子质量。
(2)稀硫酸中溶质的质量分数。
37.(3分)目前流行的甲型H1N1流感病毒,使得抗病毒药物达菲(Tamiflu)再次受到人们的“关注”。达菲可由中药八角中提取的莽草酸( shikimicacid)为原料合成,莽草酸的化学式为C7H10O5 。请回答下列问题:
(])莽草酸中碳、氢、氧三种元素的原子个数比为 ▲ 。
(2)莽草酸的相对分子质量为 ▲ 。
(3)莽草酸中碳元素的质量分数为 ▲ (保留一位小数)。
36.(10分)草酸钙(化学式为CaC2O4,相对分子质量为128)是一种难溶于水的白色固体,受热能分解。小红同学为了探究其在加热条件下发生的变化,进行如下实验:取12.8g草酸钙固体在不断加热的条件下测得剩余固体的质量随时间变化如右图所示。请回答下列问题:
(1)t1-t2时问段内固体质量减少的原因是产生了一种极易与血红蛋白结合的有毒气体,该气体的化学式为 ▲ ;同时生成一种白色同体,它与大理石的主要成分相同,则该段时问内反应的化学方程式为 ▲ 。
(2)t2-t3时间段内固体质量不变的原因是 ▲ 。
(3)t3-t4时间段内反应的化学方程式为 ▲ 。
(4)小强和小明两位同学另取12. 8g草酸钙固体加热一段时间后,对剩余固体的成分进行探究。
[查阅资料]CaC2O4能与稀盐酸反应,其反应的化学方程式为:
CaC2O4+2HCl=CaCl2+H2C2O4;草酸(H2C2O4)是一种可溶于水的酸。
[设计方案并实验]
|
同学 |
实验操作 |
实验现象 |
结论 |
|
小强 |
取少量固体放入烧杯中,加适量水并搅拌。静置后,取上层清液于试管中,滴加紫色石蕊溶液 |
溶液变蓝色 |
剩余固体中一定含有
▲
。 一定不含有 ▲ 。 可能含有 ▲ 。 |
|
小明 |
另取少量固体放入试管中,加足量稀盐酸 |
有气体产生 |
剩余固体中一定含有
▲
。 产生气体的化学方程式为 ▲ 。 |
[交流与讨论]三位同学经过交流后认为,该剩余固体与图中 ▲ 时间段的物质成分相同。
35.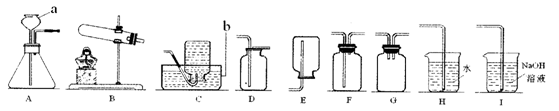 (8分)某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并填空。
(8分)某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并填空。
(1)写出图中有标号的仪器名称:a ▲ ,b ▲ 。
(2)实验室用高锰酸钾制取氧气,应选择的发生装置是 ▲ (填字母),反应的化学方程式为 ▲ 。
(3)实验室制取氢气所用的药品是 ▲ ,应选择的收集装置是 ▲ 或 ▲ (填字母)。
 (4)该小组成员查阅资料知道:硫化氢( H2S )是一种无色、有臭鸡蛋气味的有毒气体,能溶于水,其水溶液叫氢硫酸,具有挥发性。实验室常用硫化亚铁(黑色块状固体,不溶于水)与稀硫酸反应制取:FeS+ H2SO4=FeSO4十H2S↑。根据上述信息可知实验室制取硫化氢气体的最佳装置组合是 ▲ (填字母)。
(4)该小组成员查阅资料知道:硫化氢( H2S )是一种无色、有臭鸡蛋气味的有毒气体,能溶于水,其水溶液叫氢硫酸,具有挥发性。实验室常用硫化亚铁(黑色块状固体,不溶于水)与稀硫酸反应制取:FeS+ H2SO4=FeSO4十H2S↑。根据上述信息可知实验室制取硫化氢气体的最佳装置组合是 ▲ (填字母)。
34.(2分)请根据题意回答下列问题:[在下列(1)(2)两小题中任选一题回答,若两小题都回答.则以第(1)小题的答案评定分数。]
(1)用什么物质能洗净衣服上的油渍?并简述原理。
(2)鉴别羊毛纤维和棉纤维(写出操作名称和现象)。
33.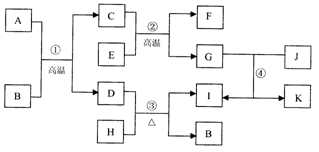 (5分)A-K均是初中化学中常见的物质.它们之间有如下图所示的转化关系。其中A、D、G、I为单质,E是铁锈的主要成分;常温下,C、D、F均为无色气体,B为无色液体,J为蓝色溶液。
(5分)A-K均是初中化学中常见的物质.它们之间有如下图所示的转化关系。其中A、D、G、I为单质,E是铁锈的主要成分;常温下,C、D、F均为无色气体,B为无色液体,J为蓝色溶液。
请回答下列问题:
(1)反应③属于 ▲ 反应(填基本反应类型)。
(2)写出E和F的化学式:E ▲ ;F ▲ 。
(3)反应①的化学方程式为 ▲ 。
反应④的化学方程式为 ▲ 。
31.(5分)A、B、C、D四种元素,A元素的原子核内只含一个质子,B是组成有机化合物不可缺少的元素,C是生物细胞中含量最高的元素,D+离子核外有10个电子。写出A、B、C三种元素的名称或符号:A ▲ 、B ▲ 、C ▲ ;D+离子的符号为 ▲ ;A、B、C、D四种元素组成的一种化合物可用于治疗胃酸过多,其化学式为 ▲ 。
|
|
Na+ |
Mg2+ |
Ca2+ |
|
OH- |
溶 |
难溶 |
微溶 |
|
Cl- |
溶 |
溶 |
溶 |
|
CO32- |
溶 |
微溶 |
难溶 |
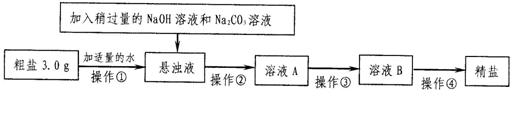 32.(6分)已知某粗盐样品中含有少量MgCl2、CaCl2及不溶性杂质。某研究性学习小组对该粗盐的提纯进行了探究,没汁如下实验流程,请根据图示回答下列问题:( 20℃时,部分物质的溶解性见右表)
32.(6分)已知某粗盐样品中含有少量MgCl2、CaCl2及不溶性杂质。某研究性学习小组对该粗盐的提纯进行了探究,没汁如下实验流程,请根据图示回答下列问题:( 20℃时,部分物质的溶解性见右表)
(1)操作①中需要使用的玻璃仪器有:烧杯、 ▲ 。操作②的名称为 ▲ 。若在操作②结束后发现溶液A仍浑浊,应采取的措施是 ▲ 。
(2)操作③是在加热条件下不断滴加稀盐酸至溶液的pH=7。该操作的目的是 ▲ 。
(3)操作④是将溶液B倒入 ▲ (填仪器名称)中,加热并不断搅拌,直到 ▲ 时(填现象),停止加热。
30. (4分)右图是A、B两种固体物质的溶解度曲线,根据右图回答下列问题:
(4分)右图是A、B两种固体物质的溶解度曲线,根据右图回答下列问题:
(1)10℃时,A、B两种物质的溶解度由大到小的顺序为 ▲ 。
(2)20℃时,将20g B物质加入50g水中充分溶解,所形成溶液的质 ▲ g。
(3)若使A物质从它的饱和溶液中大量析出,最适宜的方法是 ▲ (填“冷却”或“蒸发”)。
(4)50℃时,B物质饱和溶液中溶质的质量分数是 ▲ 。
29.(6分)写出下列反应的化学方程式,并在括号内注明基本反应类型:
(1)硫在氧气中燃烧 ▲ ( ▲ )反应:
(2)实验室用过氧化氢制氧气 ▲ ( ▲ )反应;
(3)澄清石灰水和碳酸钠溶液混合 ▲ ( ▲ )反应。
28.(4分)现有H、N、O、K四种元素,请选用其中的元素写出符合下列要求的化学式各一个:
(1)生命活动中不可缺少的气体 ▲ ; (2)汽车尾气中排出的有毒气体 ▲ ;
(3)能使无色酚酞溶液变红的气体 ▲ ; (4)由三种元素组成的盐 ▲ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com