
1.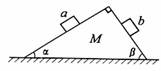 如图所示,一质量为M的楔形木块放在水平桌面上,它的顶角为90°,两底角为α和β;a、b为两个位于斜面上质量均为m的小木块.如果a、b沿斜面匀速下滑,而楔形木块静止不动,那么这时楔形木块对水平桌面的压力等于( )
如图所示,一质量为M的楔形木块放在水平桌面上,它的顶角为90°,两底角为α和β;a、b为两个位于斜面上质量均为m的小木块.如果a、b沿斜面匀速下滑,而楔形木块静止不动,那么这时楔形木块对水平桌面的压力等于( )
A.Mg+mg B.Mg+2mg
C.Mg+mg(sinα+sinβ) D.Mg+mg(cosα+cosβ)
36..有一种气体的质量是14.2g,体积是4.48升(STP),该气体的摩尔质量是
A.28.4 B.28.4g·mol-1 C.71 D.71g·mol-1
35. 设NA为阿伏加德罗常数,下列说法不正确的是 (N 14 O 16 C 12 H 1 )
A.标准状况下的22.4L乙醇完全燃烧,生成二氧化碳分子数为2NA
B.18g水中含有的质子数为10NA
C.46gNO2和44gN2O4含有的原子数均为3NA
D.在1L 2mol/L的硝酸镁溶液中含有的硝酸根离子数为4NA
34.下列离子方程式不正确的是
A.碳酸氢钙溶液跟盐酸反应:Ca(HC03)2+2H+=Ca2+=CH2O+2H20+2C02↑
B.碘化钾溶液跟适量溴水反应:2I一+Br2=I2+2Br-
C.将金属钠加入水中:2Na+2H20=2Na++20H一+H2↑
D.将氯气通人氯化亚铁溶液中2Fe2++C12=2Fe3++2Cl一
33.下列做法能改善空气质量的是
A. 以煤等燃料作为主要生活燃料
B.利用太阳能、风能和氢能等能源代替化石能源
C. 鼓励私人购买和使用汽车代替公交车
D.限制使用电动车
32、在一个密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 mol·L-1和5.4 mol·L-1,在一定的条件下它们反应生成NH3,10min后测得N2的浓度是0.8 mol·L-1,则在这10min内NH3的平均反应速率是
A、0.1mol.L-1.min-1 B、0.2mol.L-1.min-1
C、0.3mol.L-1.min-1 D、0.6mol.L-1.min-1
31、在反应:C + CO2 ≒ 2CO中,可使反应速率增大的措施是:
①增大压强 ②升高温度 ③通入CO2 ④增加碳的量 ⑤降低压强
A、①②③④ B、②③④⑤ C、①②③ D、②③④
30、可逆反应2SO2
+ O2 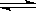 2SO3达到平衡的标志是
2SO3达到平衡的标志是
① 消耗2 mol SO2的同时生成2 mol SO3
② SO2、O2与SO3的物质的量之比为2∶1∶2
③ 反应混合物中,SO3的质量分数不再改变
A、①② B、①③ C、只有③ D、只有①
29、近年来,广州市的大部分公交车及部分出租车已采用LPG(液化石油气)作燃料,其主要的目的在于:
A、解决石油短缺问题 B、降低成本
C、减少对大气的污染 D、加大发动机的动力
28、已知空气――锌电池的电极反应为:
锌片:Zn + 2OH- - 2e- = ZnO + H2O 石墨:O2 + 2H2O + 4e- = 4OH-
根据此判断,锌片是:
A、负极,并被氧化 B、负极,并被还原 C、正极,并被氧化 D、正极,并被还原
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com