
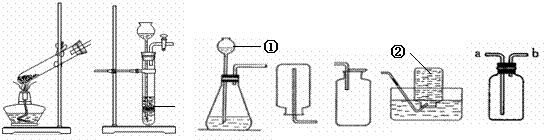
6.(兰州)(14分)实验室常用下列装置制取气体,请你根据所学知识回答下列问题。

A B C D E F G
(1)写出编号所指仪器的名称:① ;② 。
(2)以上装置图中共有两处明显的错误,请你找出错误的地方并把改正的结果填在下列横线上:① ;② 。
上述装置改进后,请继续回答下列问题。
(3)小李在实验室中用氯酸钾和另一种固体制取氧气,他选择上述装置中的A和
(填字母)进行组装。小红在实验室中选用C装置作为氧气的发生装置。在他们的实验中都用到了一种相同的固体药品是 (填化学式),在两个反应中它起 作用。请你写出小红制取氧气的化学反应方程式: 。
(4)实验室选用C和E装置还可以制取的气体是 (填化学式),写出实验室制取该气体的化学方程式 。
(5)装置B、C都可以用来制取(4)中的气体,比较这两个装置的不同,指出B装置的一个突出优点 。
(6)有一名同学欲用G装置收集H2,则H2应从导管口 通入。
答案:(1)①长颈漏斗;②集气瓶 (2)①A图中,给试管中的固体物质加热时,试管口向上倾斜了,应该略向下倾斜;②E图中,用向上排空气法收集气体时,导气管伸入过短,应伸入集气瓶的底部。(3)E或F或G(E或F都填上的满分,只填一个的0.5分。G不填不扣分); MnO2,
催化作用, 2H2O2  2H2O + O2↑(4)CO2 CaCO3 + 2HCl==CaCl2
+ H2O + CO2↑
2H2O + O2↑(4)CO2 CaCO3 + 2HCl==CaCl2
+ H2O + CO2↑
(5)可以随时控制反应的进行,随开随停。(凡叙述合理均可得分);(6)b
5.(河南)右图是实验室常用的制取气体的装置。
(1)采用A装置制取气体时,反应物的状态和反应条件需满足什么要求?
(2)B装置可以制取多种气体,请写出制取其中一种气体的化学方程式。
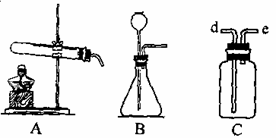 (3)写出可采用C装置(气体由d口进入)收集
(3)写出可采用C装置(气体由d口进入)收集
的一种气体的名称,并用简单的方法验证该气体。
答案:(1)反应物为固体且需要加热
(2)CaCO3 + 2HCl==CaCl2 + H2O + CO2↑
(或2H2O2  2H2O + O2↑)
2H2O + O2↑)
(3)二氧化碳(或氧气等) 向集气瓶中加入澄清石灰水,石灰水变浑浊,即可验证(或将带火星的木条伸入集气瓶中,木条复燃即可验证)
4.(河北)请你和小明一起进行实验室制取二氧化碳的探究。
(1)选择药品。小明对三组药品进行了研究,实验记录如下:
|
组别 |
药品 |
实验现象 |
|
① |
块状石灰石和稀盐酸 |
产生气泡速率适中 |
|
② |
块状石灰石和稀硫酸 |
产生气泡速率缓慢并逐渐停止 |
|
③ |
碳酸钠粉末和稀盐酸 |
产生气泡速率很快 |
从制取和收集的角度分析,一般选择第①组药品,该组药品发生反应的化学方程式
为 ;
不选择第③组药品的原因是 。
(2)选择装置。通过对制取氧气装置的分析,他选择用过氧化氢制取氧气的发生装置。你认为他选择的依据是 。
(3)制取气体。将药品装入所选装置制取气体,并用向上排空气法收集。
验满方法是 。
(4)气体检验。将生成的气体通入石蕊溶液中,溶液变红,因此他确定该气体是二氧化碳。他的检验方法是否正确?请说明理由。
。
答案:(1)CaCO3 + 2HCl==CaCl2 + H2O + CO2↑
(2)固体和液体反应,不需要加热(或反应物状态和反应条件与用过氧化氢制取氧气相同)
(3)将燃着的木条放在机器瓶口,观察火焰是否熄灭
(4)不正确。其他气体也可能使石蕊溶液变红(或应该用澄清的石灰水检验二氧化碳)
3.(黄石)小明、小华和小林三位同学利用下图所示装置在实验室制取O2和CO2,并对它们的有关性质进行研究,请回答下列问题。
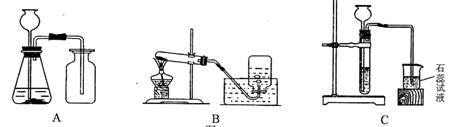
(1) 小明同学用KMnO4固体制取O2,应选用上图中的___________装置(填编号),
该反应的化学方程式为________________________________;当O2收集满并取出集气瓶后,停止该实验的正确操作方法是________________________________。
(2)小华同学用浓HCl与大理石在C装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红,对这一现象的解释不合理是___________________(填序号)。
a.产生的CO2直接使石蕊变红
b.产生的CO2与H2O反应生成H2CO3,使石蕊试液变红
c.挥发出的氯化氢溶于水,使石蕊试液变红
(3)小林同学用A装置制取了一瓶无色无味纯净的气体,他制取的气体可能___________;试用最简便的方法验证他把制取的气体_____________________。
答案:①B 2KMnO4△K2MnO4+MnO2+O2↑ 先把导气管移出水面,再熄灭酒精灯 ②a
③CO2或O2 用带火焰的木条伸入集气瓶中,若木条熄灭为CO2,若木条燃烧更旺为O2
2.(贵港)下图是实验室中用于制取和收集气体的装置图。

(1)写出上图中带标号仪器的名称:①__________,②__________。
(2)用高锰酸钾制取氧气,发生装置选择__________(填序号,下同),反应的化学方程式是______________________________,用C装置收集氧气的依据是______________________________。
(3)实验室制取二氧化碳,应选用的固体药品是__________,收集装置选择__________。
答案:(1)试管 铁架台 (2)A 2KMnO4△K2MnO4 + MnO2 + O2↑ 氧气不易溶于水
(3)大理石(或石灰石) E
1.(肇庆)现有下列仪器或装置,请回答下列问题:
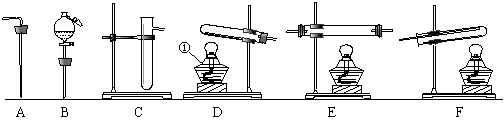
|
(2)草酸(H2C2O4) 固体在浓硫酸作用下发生反应: H2C2O4======CO2↑+CO↑+H2O,若用该反应来制取CO,制气装置应选 (填字母);除去其中的CO2可选仪器AC,C中装入的试剂最好是 (填小写字母): a. 烧碱溶液 b. 浓硫酸 c. 澄清石灰水。
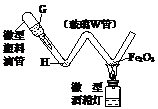 (3)点然CO前应进行的操作是
;若用CO还原氧化铜粉末,应选装置 (填字母),其反应方程式为
。
(3)点然CO前应进行的操作是
;若用CO还原氧化铜粉末,应选装置 (填字母),其反应方程式为
。
(4)右图为某种“微型”实验装置。如果G处装稀盐酸,H处放
少量铁屑,则加热处的现象为 ;
“微型塑料滴管”相当于上图实验装置中的 (填字母);用微
型仪器进行实验,除试剂用量极少以外,还可能具有的优点是
(写1点)。
答案:(1)酒精灯 D 向上排空(或排水) (2)(2分)B C a
(3)检验气体的纯度(或验纯) E CuO+CO△Cu+CO2 (4)暗红色粉末变为黑色 B 产生废物少(或减少污染、或加热需要热量少、或反应时间短、或利于分组及家庭实验)
36.(09年山东理综·31)(8分)(化学-化学与技术)
金属铝的生产是以Al2O,为原料,在熔融状态下进行电解:2Al2O3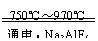
 4Al+3O2↑
4Al+3O2↑
请回答下列问题:
(1)冰晶石(Na3AIF6)的作用是 。
(2)电解生成的金属铝是在熔融液的 (填“上层”或“下层”)。
(3)阴极和阳极均由 材料做成;电解时不断消耗的电极是 (填“阳极”或“阴极”)。
(4)铝是高耗能产品,废旧铝材的回收利用十分重要。在工业上,最能体现节能减排思想的是将回收铝做成 (填代号)。
a.冰晶石 b.氧化铝 c.铝锭 d.硫酸铝
答案:(1)降低Al2O3的熔化温度 (2)下层(3)碳素(或石墨) 阳极(4)c
 解析:Al2O3的熔点很高,熔化得需要较多能量,加入助熔剂就可节约能量,降低熔化温度
解析:Al2O3的熔点很高,熔化得需要较多能量,加入助熔剂就可节约能量,降低熔化温度
 (2)由于冰晶石(Na3AlF6)与氧化铝熔融物密度比铝的小,所以铝在熔融液的下层。
(2)由于冰晶石(Na3AlF6)与氧化铝熔融物密度比铝的小,所以铝在熔融液的下层。
 (3)电解时阳极的碳棒被生成的氧气氧化。
(3)电解时阳极的碳棒被生成的氧气氧化。
 (4)电解产生的铝要尽量以单质形式存在,所以将回收铝做成铝锭最好。
(4)电解产生的铝要尽量以单质形式存在,所以将回收铝做成铝锭最好。
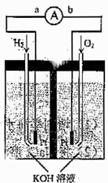
37 .(09年天津理综·10)(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
.(09年天津理综·10)(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
 (1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为
(用a、b表示)。
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为
(用a、b表示)。
 (2)负极反应式为
。
(2)负极反应式为
。
 (3)电极表面镀铂粉的原因为
。
(3)电极表面镀铂粉的原因为
。
 (4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
 Ⅰ.2Li+H2
Ⅰ.2Li+H2
 2LIH
2LIH
 Ⅱ.LiH+H2O==LiOH+H2↑
Ⅱ.LiH+H2O==LiOH+H2↑
 ①反应Ⅰ中的还原剂是
,反应Ⅱ中的氧化剂是
。
①反应Ⅰ中的还原剂是
,反应Ⅱ中的氧化剂是
。
 ②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为
。
②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为
。
 ③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
mol。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
mol。
答案:(1)由化学能转化为电能 由a到b
(2)2H2+4OH--4e-=4H2O或H2+2OH--2e-=2H2O
(3)增大电极单位面积吸附H2、O2分子数,加快电极反应速率
(4)①Li H2O ②或8.71×10-4 ③32
解析:本题考查电化学知识。(1)原电池的实质为化学能转化成电能。总反应为2H2 + O2 =2H2O,其中H2从零价升至+1价,失去电子,即电子从a流向b。(2)负极为失去电子的一极,即H2失电子生成H+,由于溶液是碱性的,故电极反应式左右应各加上OH-。(3)铂粉的接触面积大,可以加快反应速率。(4)I.Li从零价升至+1价,作还原剂。II.H2O的H从+1降至H2中的零价,作氧化剂。由反应I,当吸收10molH2时,则生成20molLiH,V=m/ρ=20×7.9/0.82 ×10-3L=192.68×10-3L。V(LiH)/v(H2)= 192.68×10-3L/224L=8.71×10-4。20mol LiH可生成20mol H2,实际参加反应的H2为20×80%=1.6mol,1molH2转化成1molH2O,转移2mol电子,所以1.6molH2可转移3.2mol的电子。
35.(09年山东理综·29)(12分)Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。
(1)该电池的负极材料是 。电池工作时,电子流向 (填“正极”或“负极”)。
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是
。欲除去Cu2+,最好选用下列试剂中的 (填代号)。
a.NaOH b.Zn c.Fe d.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是 。若电解电路中通过2mol电子,MnO2的理论产量为 。
答案:(1)Zn(或锌) 正极
(2)Zn与Cu2+反应生成Cu,Zn与Cu构成原电池,加快反应速率 b
(3)2H++2e-=H2↑ 87g
 解析:(1) 负极上是失电子的一极 Zn失电子有负极经外电路流向正极。(2)锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀。除杂的基本要求是不能引入新杂质,所以应选Zn将Cu2+
置换为单质而除去。(3)阴极上得电子,发生还原反应, H+得电子生成氢气。因为MnSO4-MnO2-2 e-,通过2mol电子产生1molMnO2,质量为87g。
解析:(1) 负极上是失电子的一极 Zn失电子有负极经外电路流向正极。(2)锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀。除杂的基本要求是不能引入新杂质,所以应选Zn将Cu2+
置换为单质而除去。(3)阴极上得电子,发生还原反应, H+得电子生成氢气。因为MnSO4-MnO2-2 e-,通过2mol电子产生1molMnO2,质量为87g。
 [考点分析] 原电池原理和电解原理综合运用
[考点分析] 原电池原理和电解原理综合运用
34.(09年宁夏理综·37)[化学-选修化学与技术](15分)
请回答氯碱的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k= (要求计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是 (填序号)
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
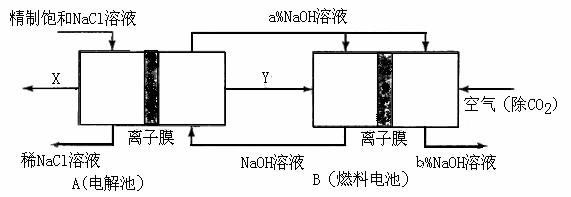 ①图中X、Y分别是 、 (填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小 ;
①图中X、Y分别是 、 (填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小 ;
②分别写出燃料电池B中正极、负极上发生的电极反应正极: ; 负极: ;
③这样设计的主要节(电)能之处在于(写出2处) 、 。
答案:(1)k=M(Cl2)/2 M(NaOH)=71/80=1:1.13或0.89(2)③①② (3)①Cl2 H2 a%小于b% ②O2+4e-+2H2O=4OH- H2-2e-+2OH-=2H2O ③燃料电池可以补充电解池消耗的电能;提高产出碱液的浓度;降低能耗(其他合理答案也给分)
解析:(1)只要了解电解饱和食盐水的化学方程式2NaCl+2H2O 2NaOH+H2↑+Cl2↑即可得到,k=M(Cl2)/2 M(NaOH)=71/80=1:1.13或0.89;(2)只要抓住除钡离子要放在除碳酸根离子前即可得到顺序关系:③①②;(3)本题突破口在于B燃料电池这边,通空气一边为正极(还原反应),那么左边必然通H2,这样Y即为H2 ;再转到左边依据电解饱和食盐水的化学方程式可知唯一未知的就是X,必然为Cl2了;A中的NaOH进入燃料电池正极再出来,依据O2+4e-+2H2O=4OH- 可知NaOH+浓度增大。
2NaOH+H2↑+Cl2↑即可得到,k=M(Cl2)/2 M(NaOH)=71/80=1:1.13或0.89;(2)只要抓住除钡离子要放在除碳酸根离子前即可得到顺序关系:③①②;(3)本题突破口在于B燃料电池这边,通空气一边为正极(还原反应),那么左边必然通H2,这样Y即为H2 ;再转到左边依据电解饱和食盐水的化学方程式可知唯一未知的就是X,必然为Cl2了;A中的NaOH进入燃料电池正极再出来,依据O2+4e-+2H2O=4OH- 可知NaOH+浓度增大。
[点评]本题前半部基本就是课本内容的再现,但后半部很有创意,可以很好的综合考查考生的原电池和电解的相关知识
33.
 (09年江苏化学·16)(8分)以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸钠和氧化铁红颜料,原料的综合利用率较高。其主要流程如下:
(09年江苏化学·16)(8分)以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸钠和氧化铁红颜料,原料的综合利用率较高。其主要流程如下:

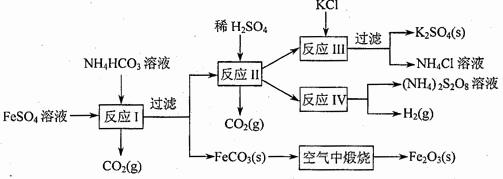
 (1)反应I前需在FeSO4溶液中加入 (填字母),以除去溶液中的Fe3+。
(1)反应I前需在FeSO4溶液中加入 (填字母),以除去溶液中的Fe3+。
 A.锌粉 B.铁屑 C.KI溶液 D.H2
A.锌粉 B.铁屑 C.KI溶液 D.H2
 (2)反应Ⅰ需控制反应温度低于35℃,其目的是
。
(2)反应Ⅰ需控制反应温度低于35℃,其目的是
。
 (3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是
。
(3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是
。
 (4)反应Ⅳ常被用于电解生产(NH4)2S2O8(二硫酸铵)。电解时均用惰性电极,阳极发生地电极反应可表示为
。
(4)反应Ⅳ常被用于电解生产(NH4)2S2O8(二硫酸铵)。电解时均用惰性电极,阳极发生地电极反应可表示为
。
 答案:(1)B
答案:(1)B
 (2)防止NH4HCO3分解(或减少Fe2+的水解)
(2)防止NH4HCO3分解(或减少Fe2+的水解)
 (3)降低K2SO4
的溶解度,有利于K2SO4 析出。
(3)降低K2SO4
的溶解度,有利于K2SO4 析出。
 (4)2SO42-
-2e-
(4)2SO42-
-2e- 2S2O82-
2S2O82-
 解析:(1)在FeSO4溶液中除去溶液中的Fe3+,最好选用铁屑或铁粉,比较简单。(2)如果温度过高会导致NH4HCO3分解同样也会加快Fe2+的水解(温度越高水解速率越快)这样会使原料利用率降低。(3)由题目看出在III反应中生成的K2SO4
为固体,而K2SO4在无机溶剂中溶解度是比较大的,要想使K2SO4析出只能降低其溶解度所以加入醇类溶剂目的降低K2SO4的溶解度。
解析:(1)在FeSO4溶液中除去溶液中的Fe3+,最好选用铁屑或铁粉,比较简单。(2)如果温度过高会导致NH4HCO3分解同样也会加快Fe2+的水解(温度越高水解速率越快)这样会使原料利用率降低。(3)由题目看出在III反应中生成的K2SO4
为固体,而K2SO4在无机溶剂中溶解度是比较大的,要想使K2SO4析出只能降低其溶解度所以加入醇类溶剂目的降低K2SO4的溶解度。
 (4)根据阴阳极反应原理阳极失电子发生氧化反应,此题实质是电解硫酸铵溶液,在根据反应后的产物得出正确的答案。
(4)根据阴阳极反应原理阳极失电子发生氧化反应,此题实质是电解硫酸铵溶液,在根据反应后的产物得出正确的答案。
 [考点分析]此题为化工生产题型,主要考察了化合物性质,电极方程式书写。做此类题要分析清楚每一个环节目的和结果是什么。这样才能判断各反应后的产物分别是什么。
[考点分析]此题为化工生产题型,主要考察了化合物性质,电极方程式书写。做此类题要分析清楚每一个环节目的和结果是什么。这样才能判断各反应后的产物分别是什么。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com