
2、氯气的化学性质
由氯的原子结构示意图可知氯元素的性质如何?进而能否预测氯气的化学性质又怎样?为什么? 。
① 与金属单质的反应:与钠反应方程式 。现象是 。与
铁反应方程式 。现象是 。与铜反应方程式 。现象是 。
② 与氢气的反应:化学方程式: ,反应现象:氢气在氯气中燃烧 ;氯气与氢气的爆炸实验 。
③Cl2 和红磷反应:化学方程式: ,反应现象 。
结论:分析以上反应中氯元素价态的变化也可得知:氯气是一种强氧化性物质,常氧化剂。
思考:在初中我们是如何定义燃烧的?现在通过氢气与氯气的燃烧实验,你有什么新的认识?
④与水的反应:
与水反应的离子方程式: ,说明:氯气与水反应很微弱,且未可逆反应。
1、氯气的物理性质: 色有 气味的 体, 毒, 溶于水。实验室中应怎样闻气体: 。
5.理解卤族元素原子结构及其单质性质的递变性
知识梳理
一、 氯元素的原子结构与自然界的存在
氯元素位于周期表__周期__族,在自然界中的主要存在形态: 。全球海洋中含盐 左右,主要为 、 。
二、 活泼的氯气
4.学会Cl-的检验方法
3.知道氯水的消毒和漂白原理
2.了解氯气及其化合物的性质
1.知道氯气的物理性质。
答案:(1) S+SO2+2OH-=S2O32-+H2O (2) a、2amol (3) 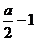
氯及其化合物
考点聚焦
(3)由④式可知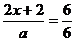 x=
x=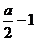

 S2-+(x+1)S Sx2- ………………②
S2-+(x+1)S Sx2- ………………②
SO32-+S △ S2O32- ……………………③
由①②③迭加得:(2x+2)S+6OH- = 2Sx2-+S2O32-+3H2O …………④
SO2+Sx2-+OH-――S2O32-+H2O ………………⑤
由④⑤迭加得:S+SO2+2OH-=S2O32-+H2O …………………………⑥
答第(1)问时,实质不必要这么繁的过程,因Sx2-、SO32-均为中间产物,只要抓住反应物为S和SO2及OH-,生成物为S2O32-和水即可得反应⑥。
由⑥式可知每有1mol硫需1molSO2和2molOH-,则SO2和OH-分别为a、2amol。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com