
1、有关乙炔分子中的化学键描述不正确的是
A.两个碳原子采用sp杂化方式 B. 两个碳原子采用sp2杂化方式
C.每个碳原子都有两个未杂化的2p轨道形成π键 D. 两个碳原子形成两个π键
(2)要使B不析出,B的质量≤b,而A要析出,A的质量应>a。当W<a+b时,只要A>a,即可满足条件,所以A%>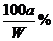 。当W>a+b时,B≤b即可满足条件,所以A%≥
。当W>a+b时,B≤b即可满足条件,所以A%≥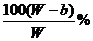
【例4】氯化铁溶液和氢氧化铁胶体具有的共同性质是( )
A.分散系颗粒直径都在1~100nm之间
B.能透过半透膜
C.加热蒸干、灼烧后都有氧化铁生成
D.呈红褐色
解析:溶液中溶质颗粒直径都小于1nm,胶体中胶粒直径都在1~100 nm之间,前者能透过半透膜,后者不能透过半透膜。加热蒸干时,氯化铁水解为氢氧化铁,灼烧后,氢氧化铁分解为氧化铁,氧化铁溶液呈棕黄色,氢氧化铁胶体呈红褐色。
答案:C
 根据公式:100+S(高温)∶S(高温)-S(低温)=高温下饱和溶液质量∶析出晶体质量
根据公式:100+S(高温)∶S(高温)-S(低温)=高温下饱和溶液质量∶析出晶体质量
(100 +a2)∶(a2-a1)=(300-50)∶χ
χ=250(a2-a1)/(100+a2)g
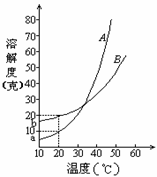
【例3】A、B两种化合物的溶解度曲线如右图。现要用结晶法从A、B混和物中提取A。(不考虑A、B共存时,对各自溶解度的影响。)
(1)取
(2)取W克混和物,将它溶于
当W<a+b时,A%
当W>a+b时,A% 。
解析:(1)因为在
溶液的物质的量浓度=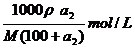
设降温至t1时,析出的晶体的质量为χ
由t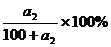 。
。
饱和溶液的溶质质量关分数可用下式计算: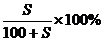
再根据物质的量浓度和溶质质量分数的换算公式,求出溶液的物质的量浓度。
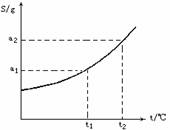 【例2】摩尔质量为M g/mol的某物质的溶解度曲线如图所示,现有t
【例2】摩尔质量为M g/mol的某物质的溶解度曲线如图所示,现有t
解析:由溶解度曲线可知,在t2时,该物质的溶解度为a
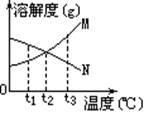 A.t
A.t
B.温度从t
C.M比N的溶解度大
D.N中含有少量M时,可用降温结晶法提纯N
解析:由图可看出,t
答案: A
2.分散系的比较
分散系
种类
溶液
胶体
浊液
水溶液
非水溶液
粒子胶体
分子胶体
悬浊液
乳浊液
分散质粒子
离子或分子
分子
分子或离子的集合体
大分子
巨量分子集合的颗粒
巨量分子集合的液滴
举例
食盐水
碘酒
Fe(OH)3胶体
淀粉溶液
石灰乳
牛奶
分散质粒子直径⑴
1n m
1nm~100n m
100n m
均一性⑵
稳定性⑶
久置沉降
久置分层
能否通过滤纸⑷
能否通过半透膜⑸
有无丁达尔效应⑹
―
试题枚举
【例1】右图是M、N两种不含结晶水的固体物质的溶解度曲线。下列说法中正确的是
1.概念:一种或几种物质分散到另一种物质中形成的混合物叫做分散系。被分散的物质叫做 ,物质分散于其中的物质叫做 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com