
1、全国卷Ⅰ:陕西、河北、河南、山西、广西2009年高考作文题
兔子是历届小动物运动会的短跑冠军,可是不会游泳。一次兔子被狼追到河边,差点被抓住。动物管理局为了小动物的全面发展,将小兔子送进游泳培训班,同班的还有小狗,小龟和小松鼠等。小狗,小龟学会游泳,又多了一种本领,心里很高兴;小兔子和小松鼠花了好长时间都没学会,很苦恼。培训班教练野鸭说:“我两条腿都能游,你们四条腿还不能游?成功的90%来自汗水。加油!呷呷!”评论家青蛙打发感慨:“兔子擅长的是奔跑!为什么只是针对弱点训练而不发展特长呢?”思想家仙鹤说:“生存需要的本领不止一种呀!兔子学不了游泳就学打洞,松鼠学不了游泳就学爬树嘛。”要求选准角度,明确立意,自选文体,自拟标题;不要脱离材料内容及含意的范围作文,不要套作,不得抄袭。
点评:全国的一卷的作文,也是一个寓言故事。寓言故事影射的都是现实,就是现实生活中我们应该怎么样对待人才的培养,是这个问题,怎么认识人的特长,扬长避短,你刚才说一个是取长补短,一个是扬长避短,取长补短,我觉得自己有短处,别人有长处,把别人的长处学来,来取长补短。教练的话,青蛙的话,仙鹤的话都不是靶心,都是自成道理,都有道理,所以你选其中任何一个角度写都可以,但是你不能一会儿站在游泳教练的角度,一会儿又站在青蛙的角度,我觉得一篇好的考场文章,800字左右,它应该角度小一点,这是我一贯讲的,角度要小一点,而且内容要集中一点,你不能这个角度说几句,那个角度说几句,最后你这篇文章就散乱不堪了,杂乱无章了。寓言故事是远距离辐射现实,马上想到现实和它什么能产生一种对应,然后就来写现实生活,这样把内容写得集中一些,我刚才说挖掘深刻一些,这样就可以了,内容新鲜一些。
22.(本小题满分12分)(注意:在试题卷上作答无效)
设函数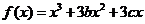 有两个极值点
有两个极值点
(Ⅰ)求b、c满足的约束条件,并在下面的坐标平面内,画出满足这些条件的点(b,c)和区域;
(Ⅱ)证明: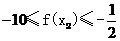
21.(本小题满分12分)(注意:在试题卷上作答无效)
如图,已知抛物线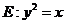 与圆
与圆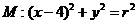
 相交于
相交于 四个点。
四个点。
(I)求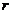 的取值范围:
的取值范围:

(II)当四边形 的面积最大时,求对角线
的面积最大时,求对角线
 的交点
的交点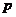 的坐标。
的坐标。
18.(本小题满分12分)
(注意:在试题卷上作答无效)
如图,四棱锥S-ABCD中,底面ABCD为矩形,SD⊥底面ABCD,AD= ,DC=SD=2.点M在侧棱SC上,∠ABM=60
,DC=SD=2.点M在侧棱SC上,∠ABM=60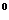 .
.
(Ⅰ)证明:M是侧棱SC的中点;
(Ⅱ)求二面角S-AM-B的大小。
(19)(本小题满分12分)(注意:在试题卷上作答无效)
甲、乙二人进行一次围棋比赛,约定先胜3局者获得这次比赛的胜利,比赛结束,假设在一局中,甲获胜的概率为0.6,乙获胜的概率为0.4,各局比赛结果相互独立。已知前2局中,甲、乙各胜1局。
(1)求甲获得这次比赛胜利的概率;
(2)设 表示从第3局开始到比赛结束所进行的局数,求
表示从第3局开始到比赛结束所进行的局数,求 的分布列及数学期望。(20)(本小题满分12分)(注意:在试题卷上作答无效)
的分布列及数学期望。(20)(本小题满分12分)(注意:在试题卷上作答无效)
在数列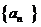 中,
中, 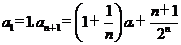 .
.
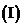 设
设 ,求数列
,求数列 的通项公式;
的通项公式;
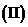 求数列
求数列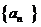 的前
的前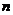 项和
项和 .
.
17.(本小题满分10分)
(注意:在试题卷上作答无效)
在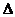 ABC中,内角A、B、C的对边长分别为a、b、c ,已知
ABC中,内角A、B、C的对边长分别为a、b、c ,已知
 ,且
,且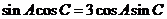 ,求b.
,求b.
(注意:在试题卷上作答无效)
(13)  的展开式中,
的展开式中,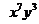 的系数与
的系数与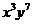 的系数之和等于
.
的系数之和等于
.
(14)设等差数列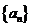 的前n项和为
的前n项和为 .若
.若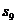 =72,则
=72,则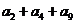 =
.
=
.
(15)直三棱柱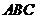 -
-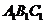 各顶点都在同一球面上.若
各顶点都在同一球面上.若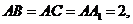 ∠
∠ =
= ,则此球的表面积等于
.
,则此球的表面积等于
.
(16)若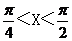 ,则函数
,则函数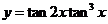 的最大值为
.
的最大值为
.
3.本卷共10小题,共90分.
(1)设集合A={4,5,7,9},B={3,4,7,8,9},全集U=A B,则集合
B,则集合 (A
(A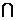 B)中的元素共有
B)中的元素共有
(A)3个 (B)4个 (C)5个 (D)6个
(2)已知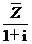 =2+I,则复数z=
=2+I,则复数z=
(A)-1+3i (B)1-3i (C)3+I (D)3-i
(3) 不等式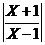 <1的解集为
<1的解集为
(A){x (B)
(B)
(C) (D)
(D)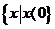
(4)设双曲线 (a>0,b>0)的渐近线与抛物线y=x2 +1相切,则该双曲线的离心率等于
(a>0,b>0)的渐近线与抛物线y=x2 +1相切,则该双曲线的离心率等于
(A) (B)2
(C)
(B)2
(C)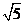 (D)
(D)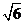
(5) 甲组有5名同学,3名女同学;乙组有6名男同学、2名女同学。若从甲、乙两组中各选出2名同学,则选出的4人中恰有1名女同学的不同选法共有
(A)150种 (B)180种 (C)300种 (D)345种
(6)设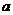 、
、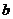 、
、 是单位向量,且
是单位向量,且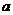 ·
·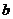 =0,则
=0,则 的最小值为
的最小值为
(A) (B)
(B) (C)
(C) (D)
(D)
(7)已知三棱柱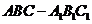 的侧棱与底面边长都相等,
的侧棱与底面边长都相等,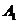 在底面
在底面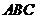 上的射影为
上的射影为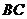 的中点,则异面直线
的中点,则异面直线 与
与 所成的角的余弦值为
所成的角的余弦值为
(A)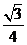 (B)
(B)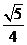 (C)
(C)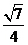 (D)
(D) 
(8)如果函数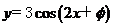 的图像关于点
的图像关于点 中心对称,那么
中心对称,那么 的最小值为
的最小值为
(A)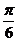 (B)
(B)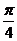 (C)
(C) (D)
(D) 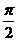
(9) 已知直线y=x+1与曲线 相切,则α的值为
相切,则α的值为
(A)1 (B)2 (C) -1 (D)-2
(10)已知二面角α-l-β为600 ,动点P、Q分别在面α、β内,P到β的距离为 ,Q到α的距离为
,Q到α的距离为 ,则P、Q两点之间距离的最小值为
,则P、Q两点之间距离的最小值为
(A) (B)2
(C)
(B)2
(C)  (D)4
(D)4
(11)函数 的定义域为R,若
的定义域为R,若 与
与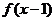 都是奇函数,则
都是奇函数,则
(A)  是偶函数
(B)
是偶函数
(B)  是奇函数
是奇函数
(C) 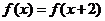 (D)
(D)
 是奇函数
是奇函数
(12)已知椭圆C: 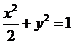 的又焦点为F,右准线为L,点
的又焦点为F,右准线为L,点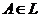 ,线段AF 交C与点B。若
,线段AF 交C与点B。若 ,则
,则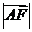 =
=
(A) (B)2
(C)
(B)2
(C)  (D)3
(D)3
2009年普通高等学校招生全国统一考试
理科数学(必修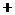 选修Ⅱ)
选修Ⅱ)
第Ⅱ卷
2.第Ⅱ卷共7页,请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,在试题卷上作答无效.
近几年高考几乎每年都设置判断离子共存问题的试题。从历年高考中有关离子共存问题的难度上分析,这类问题都属于中等难度偏易题,但这类题的区分度都比较高。离子共存与离子反应是一个问题的两个方面,离子不能共存必然是离子反应发生的结果,讨论离子共存也就是对离子反应发生条件的判断。另外,离子共存问题又比较综合,往往涉及多种离子之间的反应,有时还要考虑环境因素的影响。
例4.在pH=1的无色透明溶液中不能大量共存的离子组是( )
A.Al3+ Ag+ NO3- Cl- B.Mg2+ NH4+ NO3- Cl-
C.Ba2+ K+ S2- Cl- D.Zn2+ Na+ NO3- SO42-
答案:AC
解题说明:1.首先从化学基本理论和概念出发,理清离子反应的规律和“离子共存”的条件。在中学化学中要求掌握的离子反应规律主要是离子间发生复分解反应和离子间发生氧化反应,以及在一定条件下一些微粒(离子、分子)可形成络合离子等。“离子共存”的条件是根据上述三个方面统筹考虑、比较、归纳整理而得出。因此解决“离子共存”问题可从离子间的反应规律入手,逐条梳理。2.审题时应注意题中给出的附加条件:(1)酸性溶液(H+)、碱性溶液(OH-)、能在加入铝粉后放出可燃气体的溶液、由水电离出的H+或OH-的浓度为
1×10-10mol/L的溶液等。(2)有色离子MnO4-(紫色)、Fe3+(黄色)、Cu2+(蓝色)、Fe2+(浅绿色)、Fe(SCN)2+(血红色)。(3)MnO4-,NO3-等在酸性条件下具有强氧化性。(4)S2O32-在酸性条件下发生氧化还原反应:S2O32-+2H+=S↓+SO2↑+H2O (5)注意题目要求“大量共存”还是“不能大量共存”。3.审题还应特别注意以下几点:(1)注意溶液的酸性对离子间发生氧化还原反应的影响。如:Fe2+与NO3-能共存,但在强酸性条件下(即Fe2+、NO3-、H+相遇)不能共存;MnO4- 与Cl-在强酸性条件也不能共存;S2-与SO32-在钠、钾盐时可共存,但在酸性条件下则不能共存。(2)酸式盐的含氢弱酸根离子不能与强碱(OH-)、强酸(H+)共存。
4.离子反应的应用
(1)物质检验与含量测定:只要对其中特定的离子进行检验或测定即可,不必对物质的所有构成离子进行检验和测定。定量测定的方法包括酸碱中和滴定法、氧化还原滴定法、沉淀滴定法、络合滴定法等。
附:常见离子的检验
|
离子 |
所用试剂或操作 |
现象 |
相关方程式 |
|
NH4+ |
加浓碱液、△ |
产生刺激性气味气体,且使湿润红色石蕊试纸变蓝 |
NH4+ + OH– NH3↑+ H2O NH3↑+ H2O |
|
Mg2+ |
加过量NaOH溶液 |
产生白色沉淀 |
Mg2+ + 2OH– = Mg(OH)2↓ |
|
Al3+ |
加过量氨水,后加NaOH |
产生白色沉淀,加NaOH时沉淀溶解 |
Al3++3NH3•H2O = Al(OH)3↓+3NH4+ Al(OH)3+ OH–= [Al(OH)4]-+ 2H2O |
|
Fe2+ |
加NaOH溶液 |
产生白色沉淀,后迅速变灰绿,最终变红褐色沉淀 |
Fe2+ + 2OH– = Fe (OH)2↓ 4Fe (OH)2 + O2 + 2H2O = 4Fe (OH)3 |
|
Fe3+ |
加KSCN溶液 |
溶液变血红色 |
Fe3+ + SCN– = [Fe(SCN)]2+ |
|
Ag+ |
加NaCl溶液,后加稀HNO3 |
产物白色↓,加稀HNO3后不溶 |
Ag+ + Cl– = AgCl↓ |
|
Cl– |
加稀HNO3酸化的AgNO3溶液 |
产生白色沉淀 |
Ag+ + Cl– =
AgCl↓ |
|
Br– |
加稀HNO3酸化的AgNO3溶液 |
产生淡黄色沉淀 |
Ag+ + Br– =
AgBr↓ |
|
I– |
加稀HNO3酸化的AgNO3溶液 |
产生黄色沉淀 |
Ag+ + I– =AgI↓ |
|
SO42– |
加HCl酸化的BaCl2 |
产生白色沉淀 |
Ba2++SO42–= BaSO4↓ |
|
SO32– |
加盐酸后,产生气体,通入品红试液,加热 |
产生无色刺激性气味气体,且使品红试液褪色,加热后恢复原色 |
2H++ SO32–=SO2↑+H2O |
|
NO3– |
加Cu和浓H2SO4,加热浓缩 |
产生红棕色气体,溶液变蓝 |
Cu+2H2SO4(浓)+2NaNO3 CuSO4+Na2SO4+2NO2↑+2H2O CuSO4+Na2SO4+2NO2↑+2H2O |
|
PO43– |
加AgNO3溶液,后加稀HNO3 |
产生黄沉淀,加酸后沉淀溶解 |
3Ag++ PO43–=
Ag3PO4↓Ag3PO4+3H+=3Ag++H3PO4 |
|
CO32– |
加盐酸后,产生的气体通入澄清石灰水 |
产生无色气体,此气体能使澄清石灰水变浑浊 |
2H++CO32–=CO2↑+H2O Ca2++2OH–+CO2=CaCO3↓+H2O |
|
HCO3– |
加热,产生的气体通入澄清石灰水 |
产生无色气体,此气体能使澄清石灰水变浑浊 |
2NaHCO3 Na2CO3+CO2↑+H2O Ca2++2OH–+CO2=CaCO3↓+H2O Na2CO3+CO2↑+H2O Ca2++2OH–+CO2=CaCO3↓+H2O |
(2)物质的制备与纯化
(3)生活中的应用
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com