
1.76×10―5
H2CO3
CH3COOH CH3COO―+H+
CH3COO―+H+
若25℃时有HA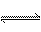 H++A―,则K==
H++A―,则K==
式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25℃)。
酸
电离方程式
电离平衡常数K
CH3COOH
21.(10分)对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系。
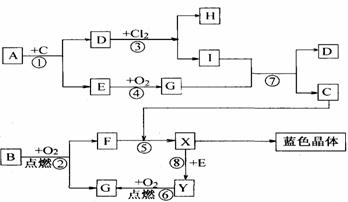 20.(10分)下图是中学化学中一些常见的物质之间发生的一系列转化的框图(反应所需和所产生的水及某些反应条件已略),其中A、B、F、Y为黑色的固体,E、G在常温常压下是气体。
20.(10分)下图是中学化学中一些常见的物质之间发生的一系列转化的框图(反应所需和所产生的水及某些反应条件已略),其中A、B、F、Y为黑色的固体,E、G在常温常压下是气体。
(1)写出下列物质的化学式:D____________,E____________。
(2)写出G通入I溶液发生反应⑦的离子方程式___________________________。
(3)以惰性电极电解X溶液的离子方程式_________________________________。
(4)试根据B、Y与氧气反应过程中的量的变化关系,设计一个实验,不用实验室里的任何试剂,只用常用的仪器,区分B、Y两种物质(简要说明实验方法和实验结论)
__________________________________________________________________________。
五.(本题包括1小题,共10分)
 |
①ⅡA族元素的价电子数 ;②第3周期元素的最高化合价 ;
(3)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3:4;M元素原子的最外层电子数与电子层数之比为4:3;N-、Z+、X+离子的半径逐渐减小;化合物XN常温下为气体。据此回答:
①N的最高价氧化物的水化物的化学式为 。
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1:1:1,A溶液中水的电离程度比B溶液中水的电离程度小。则化合物A中的化学键类型为 ,B的化学式为 。
③工业上制取单质M的化学方程式为 。
19.(8分)(1)若AgC1在水中、0.01 mol?L-1 CaCl2溶液中、0.01 mol?L-1 NaCl溶液中及0.05 mol?L-1AgNO3溶液中的溶解度分别为S1、S2、S3、S4,则S1、S2、S3、S4由大到小的顺序为 。
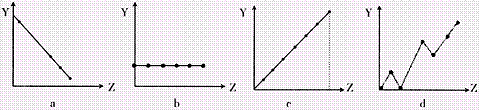
(2)下列曲线分别表示元素的某种性质与核电荷的关系(Z为核电荷数,Y为元素的有关
性质)。把与下面元素有关的性质相符的曲线标号填入相应的空格中:
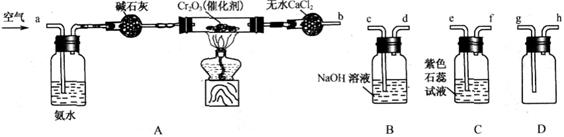 (1)装置的连接顺序为(用a、b、c、d等字母表示):b接( ),( )接( ),( )接( )。
(1)装置的连接顺序为(用a、b、c、d等字母表示):b接( ),( )接( ),( )接( )。
(2)写出氨气催化氧化的化学方程式______________________。
(3)进行实验时,装置A中碱石灰的作用是_________;D中的现象是__________________。
(4)能证明有硝酸生成的现象是__________________________________________。
(5)实验开始时,下列操作顺序最合理的是______________。
a.先加热A装置中的催化剂.再由导管a通入空气
b.先由导管a通入空气,再加热A装置中的催化剂
c.在由导管a通入空气的同时,加热A装置中的催化剂
18.(12分)某化学兴趣小组参考工业制硝酸的化学原理,在实验室用下列各装置进行组合来制备硝酸并验证硝酸的性质(所给装置必须用到并且只能用一次,各装置中的试剂均足量。已知常温下CaCl2能吸收氨气)。
 (3)在步骤③测量气体体积时,必须待试管和量筒内的气体都
(3)在步骤③测量气体体积时,必须待试管和量筒内的气体都
冷却到室温时进行,应选用下图装置中 ,理由是 ;此时量筒内的液面高于水槽中液面,立即读数会使Na2O2的纯度 (填“偏高”“偏低”或“不变”);应进行的操作是 ;
(4)在步骤⑤中滴定达到终点时,溶液的颜色变化是 ;
(5)该过氧化钠的纯度为 (实验中得到的气体体积均看作为标准状况下)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com