
17.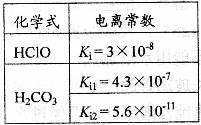
 根据右表提供的数据,判断在等浓度的
根据右表提供的数据,判断在等浓度的 、
、 混合溶液中,各种离子浓度关系正确的是
混合溶液中,各种离子浓度关系正确的是
 A.
A.
 B.
B.
 C.
C.
 D.
D.
答案:A
[解析]由表中数据可知,H2CO3的酸性大于HClO,HClO的酸性大于HCO3-的酸性,则ClO-的水解程度大于HCO3-,故A项正确, B项错误。根据物料守恒和电荷守恒判断,C项和D项等式右边都漏掉了CO32-的浓度,故均错误。
16. 物质的鉴别有多种方法。下列能达到鉴别目的的是
物质的鉴别有多种方法。下列能达到鉴别目的的是
 ①用水鉴别苯、乙醇、溴苯
①用水鉴别苯、乙醇、溴苯
 ②用相互滴加的方法鉴别
②用相互滴加的方法鉴别 和
和 溶液
溶液
 ③点燃鉴别甲烷和乙炔
③点燃鉴别甲烷和乙炔
 A.①②
B.①③ C.②③
D.①②③
A.①②
B.①③ C.②③
D.①②③
答案:B
[解析]苯、溴苯不溶于水,当二者与水混合时,苯在上层,溴苯在下层,乙醇和水互溶,①能达到鉴别目的。Ca(OH)2和NaHCO3相互滴加的反应方程式虽然不同,但现象都是生成白色沉淀,所以②达不到鉴别目的。甲烷燃烧产生淡蓝色火焰,乙炔燃烧产生明亮的火焰,并且伴有浓烟,③能达到鉴别目的。
15.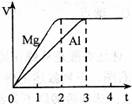
 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生
 气体的体积(V)与时间(t)关系如右图。反应中镁和铝的
气体的体积(V)与时间(t)关系如右图。反应中镁和铝的
 A.物质的量之比为3:2
B.质量之比为3:2
A.物质的量之比为3:2
B.质量之比为3:2
 C.摩尔质量之比为2:3
D.反应速率之比为2:3
C.摩尔质量之比为2:3
D.反应速率之比为2:3
答案:A
[解析]由图象可知,两个反应中生成的氢气一样多,说明两种金属提供的电子数目一样多,则镁、铝的物质的量之比为3:2,质量之比为4:3,故A项正确,B项错误。 镁、铝的摩尔质量之比为8:9,C项错。由图象镁、铝与硫酸反应需要的时间之比为2:3,则二者的速率之比为3:2,D项错。
14. 根据以下事实得出的判断一定正确的是
根据以下事实得出的判断一定正确的是

 A.HA的酸性比HB的强,则HA溶液 pH比HB溶液的小
A.HA的酸性比HB的强,则HA溶液 pH比HB溶液的小
 B.
B. 和
和 的电子层结构相同,则A原子的核电荷数比B原子的大
的电子层结构相同,则A原子的核电荷数比B原子的大
 C.A盐的溶解度在同温下比B盐的大,则A盐溶液的溶质质量分数比B盐溶液的大
C.A盐的溶解度在同温下比B盐的大,则A盐溶液的溶质质量分数比B盐溶液的大
 D.A原子失去的电子比B原子的多,则A单质的还原性比B单质的强
D.A原子失去的电子比B原子的多,则A单质的还原性比B单质的强
答案:B
[解析]A项中由于两种酸的浓度不知,无法比较pH大小,故错误。C项没有限定是饱和溶液,C项也错误。单质还原性强弱与失电子难易有关,与数目没有必然关系, 故D错误。
13.
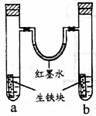 右图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间。下列有关描述错误的是
右图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间。下列有关描述错误的是
 A.生铁块中的碳是原电池的正极
A.生铁块中的碳是原电池的正极
 B.红墨水柱两边的液面变为左低右高
B.红墨水柱两边的液面变为左低右高
 C.两试管中相同的电极反应式是:
C.两试管中相同的电极反应式是:
 D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀
D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀
答案:B
[解析]a为中性环境,发生吸氧腐蚀,氧气被消耗,气体压强减小;b中酸性较强,发生析氢腐蚀,有氢气放出,气体压强增大,所以红墨水柱两边的液面变为左高右低,故B项错。
12. NA代表阿伏加德罗常数。下列有关叙述正确的是
NA代表阿伏加德罗常数。下列有关叙述正确的是
 A.标准状况下,2.24LH2O含有的分子数等于0.1NA
A.标准状况下,2.24LH2O含有的分子数等于0.1NA
 B.常温下,
B.常温下, 溶液中阴离子总数大于0.1NA
溶液中阴离子总数大于0.1NA
 C.分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g
C.分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g
 D.3.4
D.3.4 中含N-H键数目为
中含N-H键数目为
答案:B
[解析]标准状况下,水是液体,A项错。由碳酸根离子水解的离子方程式可知,水解引起阴离子数目增多,B项正确。C项没有指明条件,22.4L并不一定是1mol,但该混合气体的质量为28g是正确的,故C错误。1分子NH3中含3个N-H共价键,3.4g氨气中含N-H数目为0.6NA ,D项错。




11. 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度
1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度
 为115-125℃,反应装置如右图。下列对该实验的描述错误的是
为115-125℃,反应装置如右图。下列对该实验的描述错误的是
 A.不能用水浴加热
A.不能用水浴加热
 B.长玻璃管起冷凝回流作用
B.长玻璃管起冷凝回流作用
 C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
 D.加入过量乙酸可以提高1-丁醇的转化率
D.加入过量乙酸可以提高1-丁醇的转化率
答案:C
[解析]该酯化反应需要的温度为115-125℃,水浴的最高温度为100℃,A项正确。长导管可以起到冷凝回流酸和醇的作用,B项正确。乙酸丁酯在氢氧化钠溶液中容易发生水解,C项错。在可逆反应中,增加一种反应物浓度可以提高另一种反应物的转化率,D项正确。
10. 9.2g金属钠投入到足量的重水中,则产生的气体中含有
9.2g金属钠投入到足量的重水中,则产生的气体中含有
 A.0.2mol中子
B.0.4mol电子
A.0.2mol中子
B.0.4mol电子
 C.0.2mol质子
D.0.4mol分子
C.0.2mol质子
D.0.4mol分子
答案:C
 [解析]9.2g金属钠可以与重水反应生成0.2mol氢气,这样的0.2mol氢气含有0.4mol中子,0.4mol电子,,0.4mol质子和0.2mol分子,故C项正确。
[解析]9.2g金属钠可以与重水反应生成0.2mol氢气,这样的0.2mol氢气含有0.4mol中子,0.4mol电子,,0.4mol质子和0.2mol分子,故C项正确。
9.
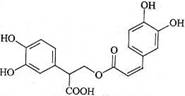 迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构
迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构
 如右图。下列叙述正确的是
如右图。下列叙述正确的是
 A.迷迭香酸属于芳香烃
A.迷迭香酸属于芳香烃
 B.1mol迷迭香酸最多能和9mol氢气发生加成反应
B.1mol迷迭香酸最多能和9mol氢气发生加成反应
 C.迷迭香酸可以发生水解反应、取代反应和酯化反应
C.迷迭香酸可以发生水解反应、取代反应和酯化反应
 D.1mol迷迭香酸最多能和含5mol NaOH的水溶液完全反应
D.1mol迷迭香酸最多能和含5mol NaOH的水溶液完全反应
答案:C
[解析]烃是指只含碳、氢两种元素的有机物,迷迭香酸中含有氧元素,故A项错。1分子迷迭香酸中含2个苯环,1个碳碳双键,最多能和7mol氢气发生加成反应,B项错。1分子迷迭香酸中含有3个酚羟基,1个羧基,1个酯基(1mol酯基水解消耗2mol),最多能和6mol氢氧化钠发生反应,D项错。
8. 在通常条件下,下列各组物质的性质排列正确的是
在通常条件下,下列各组物质的性质排列正确的是
 A.熔点:
A.熔点: B.水溶性:
B.水溶性:
 C.沸点:乙烷>戊烷>丁烷
D.热稳定性:
C.沸点:乙烷>戊烷>丁烷
D.热稳定性:
答案:D
[解析]一般地,原子晶体熔点很高,离子晶体熔点较高,分子晶体熔点较低,A项错。二氧化硫的溶解度大于硫化氢,B项错。随着碳原子数增多,烷烃的沸点升高,故C项错。非金属元素的得电子能力越强,即非金属性越强,其氢化物越稳定,D项正确。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com