
20、(12分)
(1)
(2)
(3) (4) (5)
19、(10分)
(1)_____________
(2) 原因是____________________________________________
(3) 原因是
18、(6分)
(1) (2) (3)
17、(10分)
(1) (2)
(3) (4)
(5)
22.(4分)在一个密闭容器中,有一个左右可滑动隔板,两边分别进行可逆反应,各物质的量如下:M、N、P为2.5mol、3.0mol、1.0mol。A、C、D各为0.50mol,B的物质的量为x,当x的物质的量在一定范围内变化,均可以通过调节反应器的温度,使两侧反应均达到平衡,且隔板在反应器的正中位置。达到平衡后,测得M的转化率为75%,填写空白:

(1)若要使右室反应开始时V正>V逆,x的取值范围 。
(2)若要使右室反应开始时V正<V逆,x的取值范围 。
|
 2012届高二年级第一次月考化学试卷答题卡
2012届高二年级第一次月考化学试卷答题卡21.(10分)已知反应Fe(s)+CO2(g)  FeO(s)+CO(g); DH=akJ·mol-1
FeO(s)+CO(g); DH=akJ·mol-1
测得在不同温度下,该反应的平衡常数K值随温度的变化如下:
|
温度/℃ |
500 |
700 |
900 |
|
K |
1.00 |
1.47 |
2.40 |
(1)该反应的化学平衡常数表达式为 ,a 0(填“大于”、“小于”或“等于”)。若在500℃2L密闭容器中进行该反应,CO2起始量为4mol,则CO的平衡浓度为 。
(2)若700℃该反应达到平衡,要使该平衡向右移动,其它条件不变时,可以采取的措施有 (填序号)。
A.缩小反应器体积 B.通入CO2 C.升高温度到900℃ D.使用合适的催化剂
(3)下列图像符合该反应的是
(填序号)(图中v是速率、 为混合物中CO含量,T为温度)。
为混合物中CO含量,T为温度)。
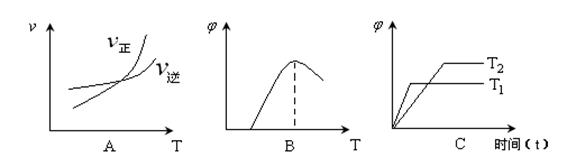
20、 (12分)已知氯水中有如下平衡:Cl2+H2O
(12分)已知氯水中有如下平衡:Cl2+H2O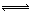 HCl+HClO。常温下,在一个体积为50 mL的针筒里(如图)吸入40 mL氯气后,再吸进10 mL水,放在光亮处。
HCl+HClO。常温下,在一个体积为50 mL的针筒里(如图)吸入40 mL氯气后,再吸进10 mL水,放在光亮处。
(1)写出针筒中可能观察到的现象
(2)若将此针筒长时间放置,又可能看到何种变化? ,试用平衡观点加以解释 。
(3)若把针筒中氯水分成I、II、III份。第I份加少量固体NaHSO3, 第Ⅱ份加少量固体NaHCO3, 则三份氯水中c(HClO) 的大小是
(4)若用原针筒吸入20mLCl2和10mL水及20mLAr气(与Cl2和水均不反应),在原温度及原光亮处,将活塞由50mL压到30mL处(保证气体不外逸),此时Cl2的反应速度比(1)中起始时 (大、小、相等)。
(5)预测上述正反应的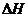 应 0。
应 0。
19、 (10分)某反应A(g)+B(g)
(10分)某反应A(g)+B(g)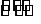 C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
(1)该反应是____________________反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,C的百分含量______(填“增大”“减小”“不变”),
原因是____________________________________________;
(3)反应体系中加入催化剂对反应热是否有影响?_______________,原因是_________:
18、(共6分)在一定条件下,反应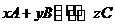 达到平衡。
达到平衡。
(1)若A、B、C都是气体,在增压后平衡向逆反应方向移动,则x,y,z之间的关系是
。
(2)若C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则A的转化率将
(填“增大”、“减小”或“不变”)
(3)若A为固体,B、C为气体,且y>z,则增大压强时混和气体的平均相对分子质量将 (填“增大”“减小”或“不变”)
17、(共10分)在下列事实中,什么因素影响了化学反应速率?
(1)集气瓶中有H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸: 。
(2)同浓度、同体积的盐酸中放入同样大小的锌粒和镁块,产生气体有快有慢:
。
(3)同样大小的石灰石在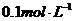 盐酸和
盐酸和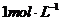 盐酸中反应速率不同: 。
盐酸中反应速率不同: 。
(4)夏天食品易变霉,冬天就不易发生该现象: 。
(5)葡萄糖在空气中燃烧需要较高的温度,可是在人体里,在正常体温(37℃)时,就可以被氧化,这是因为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com