
20.有一包固体粉末,可能由CaCO3、Na2SO4、KNO3、CuSO4、BaCl2中的一种或几种组成,做实验得以下结果:(1)将此固体粉末加到水中,得到白色沉淀,且上层清液为无色;(2)该白色沉淀部分溶于稀硝酸,并有无色气体产生。据此实验,得出的下列判断中正确的是
A.粉末中一定含有CaCO3、Na2SO4、BaCl2 B.该粉末中一定不含有KNO3、CuSO4
C.该粉末的组成中可能含有Na2SO4、KNO3 D.该粉末中一定含有Na2SO4、KNO3、BaCl2

18.下列有关操作及实验现象的描述正确的是
A.铁丝在氧气中燃烧生成四氧化三铁 
B.用湿润的蓝色石蕊试纸检验氨气时,试纸变为红色
C.向蛋清溶液中滴几滴浓硝酸,微热,出现黄色 
|

19.铜与浓硫酸共热的条件下可以发生化学反应Cu + 2H2SO4===CuSO4
+ SO2↑ + 2H2O,但
是在工业上制取硫酸铜不是直接利用浓硫酸与铜反应,而是将铜屑在空气中加热氧化,然
后浸入稀硫酸中反应过滤,并反复加热和浸入操作,你认为这样的优点是
A.节约能源 B.不产生污染大气的二氧化硫
C.提高硫酸的利用率
D.提高铜的利用率
17.下列各组物质的溶液,不另加任何试剂就能将它们区别开来的是
A.Na2CO3、Na2 SO4、HNO3、BaCl2 B.KCl、AgNO3、HCl、HNO3
C.Fe(NO3)3、NaOH、H2SO4、KCl D.HNO3、NaOH、Na2CO3、HCl
每题2分,共10分)
16.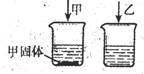 常温下,在两支各盛有100mL水的烧杯中,分别加入相同质量的甲、乙两种物质,使其充分溶解,结果如图所示。下列说法正确的是
常温下,在两支各盛有100mL水的烧杯中,分别加入相同质量的甲、乙两种物质,使其充分溶解,结果如图所示。下列说法正确的是
A.甲溶液是不饱和溶液

B.常温下,甲、乙两种物质的溶解度相同
C.升高温度,剩余的甲固体一定能继续溶解 
D.乙溶液可能是饱和溶液,也可能是不饱和溶液
15.t℃时,向一支盛有0.1g熟石灰的试管内加入10mL水,充分振荡后,静置,试管底部仍有未溶解的白色固体。对于试管内上层澄清液体的叙述正确的是
A.溶液是t℃时的饱和溶液 B.升高温度溶液变为不饱和溶液
C.溶液中溶质的质量等于0.1g D.溶液中溶质的质量分数等于1%
14.一定质量的某种物质X在足量的氧气中燃烧,生成44g二氧化碳和36g水,则X的质量
至少为多少
A.16g
B.32g
C.48g D.12g
13.根据氨碱法用食盐制纯碱的反应原理是: (1)NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl
(2)2NaHCO3 △ Na2CO3+CO2↑+H2O下列对上述信息的有关理解中,错误的是
A.用食盐制纯碱需要含碳、氧元素的物质 B.纯碱属于盐类物质
C.因生成气体,反应不遵循质量守恒定律 D.副产品氯化铵是一种氮肥
12.下表中,除去物质所含杂质的方法正确的是 
|
|
物质 |
所含杂质 |
除去杂质的方法 |
|
A |
NaCl溶液 |
NaOH |
加入稀硫酸至pH等于7 |
|
B |
CuO粉末 |
C |
加入过量稀盐酸,充分反应 |
|
C |
N2气体 |
O2 |
将气体缓缓通过灼热的铜网 |
|
D |
KCl溶液 |
CuCl2 |
加入适量铁粉 |
11.下列化学方程式符合题意且书写正确的是
A.用适量的稀盐酸除铁锈:Fe2O3+6HCl=2FeCl2+3H2O
B.医疗上用氢氧化镁中和过多胃酸:Mg(OH)2+HCl=MgCl2+H2O
C.工业上用高温煅烧石灰石的方法制生石灰:CaCO3 高温 CaO+H2O
D.工业上用氢氧化钠溶液吸收SO2:SO2 + 2NaOH == Na2SO3 + H2O
10.下列有关叙述中错误的是:

A.可以用加热的方法对医疗器械进行消毒
B.稀释浓硫酸时,把浓硫酸沿玻璃棒慢慢倒进水里,并不断搅拌
C.某溶液中加入BaCl2溶液后产生白色沉淀,原溶液中一定有SO42-
D.生铁和钢的性能不同,是因为两者的含碳量不同

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com