
5.下列符号中可表示一种元素,又可表示这种元素的一个原子,还可表示这种元素的单质的是 ( )
A.O B.H C.Fe D.N
4.下列变化中,前者是化学变化,后者是物理变化的是 ( )
A.气球爆炸、纸条燃烧 B.铁生锈、食物腐烂
C.鸡蛋变质、滴水成冰 D.铜丝导电、日光灯发亮
3.古代字画能长期保存是由于书写用墨中的碳单质在常温时有 ( )
A.稳定性 B.还原性 C.可燃性 D.催化性
2.自来水厂净水流程为:天然水――沉降――过滤――吸附――自来水。常用除臭味的试剂是 ( )
A.漂白粉 B.活性炭 C.氯气 D.明矾
1.全球气候变暖成为倍受瞩目的环境问题,温室气体主要是 ( )
A.N2 B.NH3 C.NO D.CO2
⑹待实验完毕后,若实验测得N2的体积(折算成标准状况)a L,则被还原的氧化铜的物质的量为:
⑺上述实验中,如果省去B装置,测定氨分子组成的N、H原子个数的比值将会(填“增大”、“减少”或“无影响”)减少 ,理由是:因为由N入D装置,导致H原子的个数增加。
2009届江苏省苏中四市二区联考高三化学试题
(4)根据以上实验,该同学经分析解释了以上实验中的反常现象,请你用一个化学方程式表示:
。这一反应在上述实验中 (填“是”或“否”)能确定反应完全。
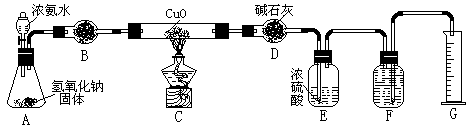
氨气与灼热的氧化铜反应生成铜、氮气和水。利用下图所示实验装置可测定氨分子的组成(图中夹持、固定装置部分均略去)。回答下列问题:
⑴写出氨气与氧化铜反应的化学方程式:2NH + 3CuO 3Cu + N+ 3HO 。
⑵在A的锥形瓶中放入NaOH固体的目的是利用NaOH的碱性和遇水放热的性质,使NH?HO 分解后逸出 。
⑶在干燥管B中不能选用的干燥剂是 C (填序号);
A.碱石灰 B.生石灰 C.五氧化二磷 D.氢气化钠
⑷在C的玻璃管中观察到的现象是:黑色固体变成了亮红色 。
⑸E装置中盛装浓硫酸的目的是:吸收多余的NH ;
某学生取纯净的Na2SO3?7H2O
50.
(1)他将恒重后的样品溶于水配成溶液,为加速溶解,可采取 的措施,观察发现样品全部溶解,溶液澄清。
(2)取少量(1)中所配溶液,加入足量的用 (填一种酸)酸化的氯化钡溶液有白色沉淀,说明产物中含有 (填离子符号)。
(3)另取少量(1)中所配溶液于试管中,滴加少量盐酸,看到气泡产生,通过 方法闻到臭鸡蛋气味,说明生成 气体,写出生成该气体的离子反应方程式: ;同时发现溶液变浑浊,原因是:(用离子方程式表示) 。
 II.在Ti的化合物中,可以呈现+2、+3、+4三种化合价,
II.在Ti的化合物中,可以呈现+2、+3、+4三种化合价,
其中以+4价的Ti最为稳定;
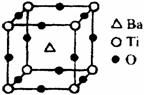
①偏钛酸钡的热稳定性好,介电常数高,在小型变压器、
话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结
构示意图如右图,它的化学式是 ;
晶体内与每个“Ti”紧邻的氧原子数为 个。
②已知Ti3+可形成配位数为6的配合物。现有含钛的两种颜色的晶体,一种为紫色,
另一种为绿色,但相关实验证明,两种晶体的组成皆为TiCl3?6H2O。为测定这
两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶
液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的。
则绿色晶体配合物的化学式为 。
21B.实验化学
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com